Clear Sky Science · ar
نهج البروتيوميات والبروتيوميات المؤكسدة لفهم تغايرية متلازمة الضائقة التنفسية الحادة
لماذا يهم هذا لمرضى العناية المركزة
متلازمة الضائقة التنفسية الحادة (ARDS) هي شكل مهدد للحياة من فشل الرئة قد يصيب الأشخاص المصابين بعدوى شديدة أو إصابة أو أمراض حرجة أخرى. كثير من المرضى الذين يعانون من ARDS يبدون متشابهين عند السرير، ومع ذلك يتعافى بعضهم بينما لا ينجو آخرون، ولا يوجد دواء ثبت أنه يعكس المتلازمة تحديدًا. تطرح هذه الدراسة سؤالًا بسيطًا لكنه مهمًا: هل يمكننا، إذا نظرنا عن كثب إلى البروتينات والتفاعلات الكيميائية داخل رئتي ودمى مرضى ARDS، اكتشاف "أنواع" بيولوجية خفية للمرض تشرح سبب اختلاف مسارات المرض لدى المرضى؟
النظر داخل الرئتين، وليس في مجرى الدم فقط
لاستكشاف ذلك، تبع الباحثون 16 بالغًا في وحدة العناية المركزة كانوا يعانون من ARDS وكانوا موصولين بأجهزة التنفس. في غضون الأيام الثلاثة الأولى بعد التشخيص، جمعوا عينات دم وسائل خاصة تسمى سائل غسيل القصبات الرئوي (BAL)، وهو شطف لطيف للحويصلات الهوائية في الرئتين. كرروا جمع هذه العينات على مدى عدة أيام عندما أمكن. باستخدام مطياف الكتلة المتقدم، قاسوا مئات البروتينات في كل عينة (بروتيوميات) وبشكل حاسم، فحصوا أيضًا مدى تأكسد بعض هذه البروتينات (بروتيوميات أكسدة/ريدكس)، ما يعكس مقدار الضرر أو التنظيم الذي تلحقه الجزيئات المؤكسدة تفاعلات الأكسجين التفاعلية، وهي نواتج كيميائية عدوانية للالتهاب.
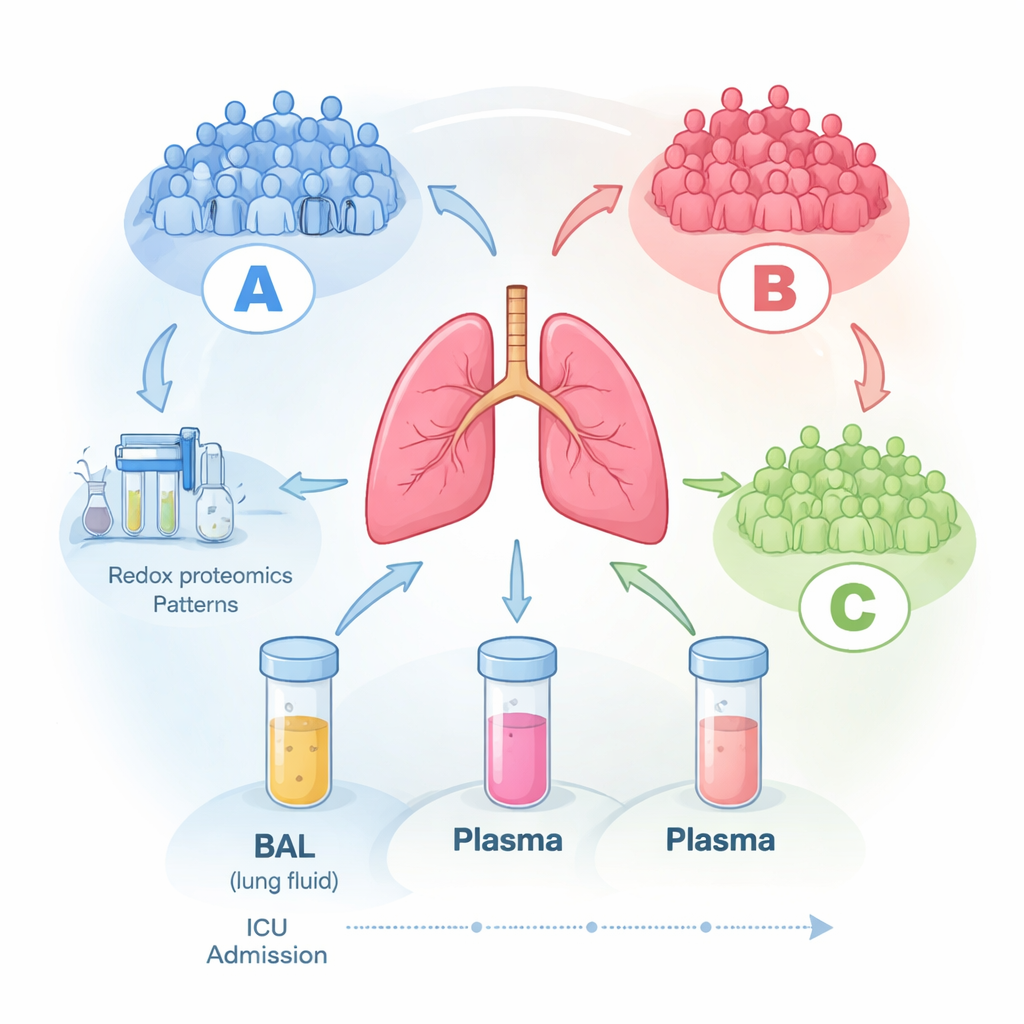
تظهر ثلاث مجموعات خفية من المرضى
عندما ترك الفريق البيانات تتجمع دون تزويد الحاسوب بأي معلومات عن المرضى، ظهر نمط واضح في عينات سائل الرئة: ثلاث مجموعات جزيئية مميزة، وُسمت A وB وC. كانت مجموعة A تميل إلى أن تكون أكثر مرضًا عند التسجيل، بينما كانت المجموعتان B وC أخف مرضًا. ومن اللافت أن هذه البصمات الجزيئية ظلت مستقرة إلى حد كبير لما يصل إلى ستة أيام في وحدة العناية المركزة، ما يوحي بأن كل مريض يندرج ضمن نمط بيولوجي نسبيًا ثابت بدلاً من تقلب عشوائي يوميًا. لم تتطابق مقاييس السرير الاعتيادية—مثل مستويات الأكسجين أو مدة البقاء أو درجات شدة المرض العامة—جيدًا مع هذه التجمعات الجزيئية، مما يلمح إلى أن الأدوات السريرية المعتادة تفوت بيولوجيا مهمة تحدث داخل الرئتين.
الإجهاد التأكسدي ودفاعات الجسم
موضوع رئيسي عبر البيانات كان التوازن بين الجزيئات المؤكسدة الضارة والدفاعات المضادة للأكسدة في الجسم. في المجموعة A، الأشد مظهرًا للمرض، وُجد أن العديد من بروتينات الرئة المشاركة في إنتاج الطاقة وصيانة الخلية كانت بمستويات أقل. والأكثر دلالة أن إنزيمات مضادة للأكسدة مهمة مثل البيروكردوكسينات، والبروتينات المرتبطة بالجلوتاثيون، والثيوردوكسين، والكاتالاز كانت منخفضة بشكل ملحوظ. في المقابل، كانت المجموعتان B وخصوصًا C تحتويان على مستويات أعلى من هذه البروتينات الواقية، مما يوحي بأن رئتيهم كانت أكثر تجهيزًا لإزالة السموم من المؤكسدات الضارة والحد من الأضرار الجانبية للالتهاب. وأضافت أنماط حالة تأكسد البروتينات طبقة إضافية، مظهرة مجموعات فرعية مختلفة من البروتينات المؤكسدة متراكزة في المجموعات الأكثر والأقل شدة.
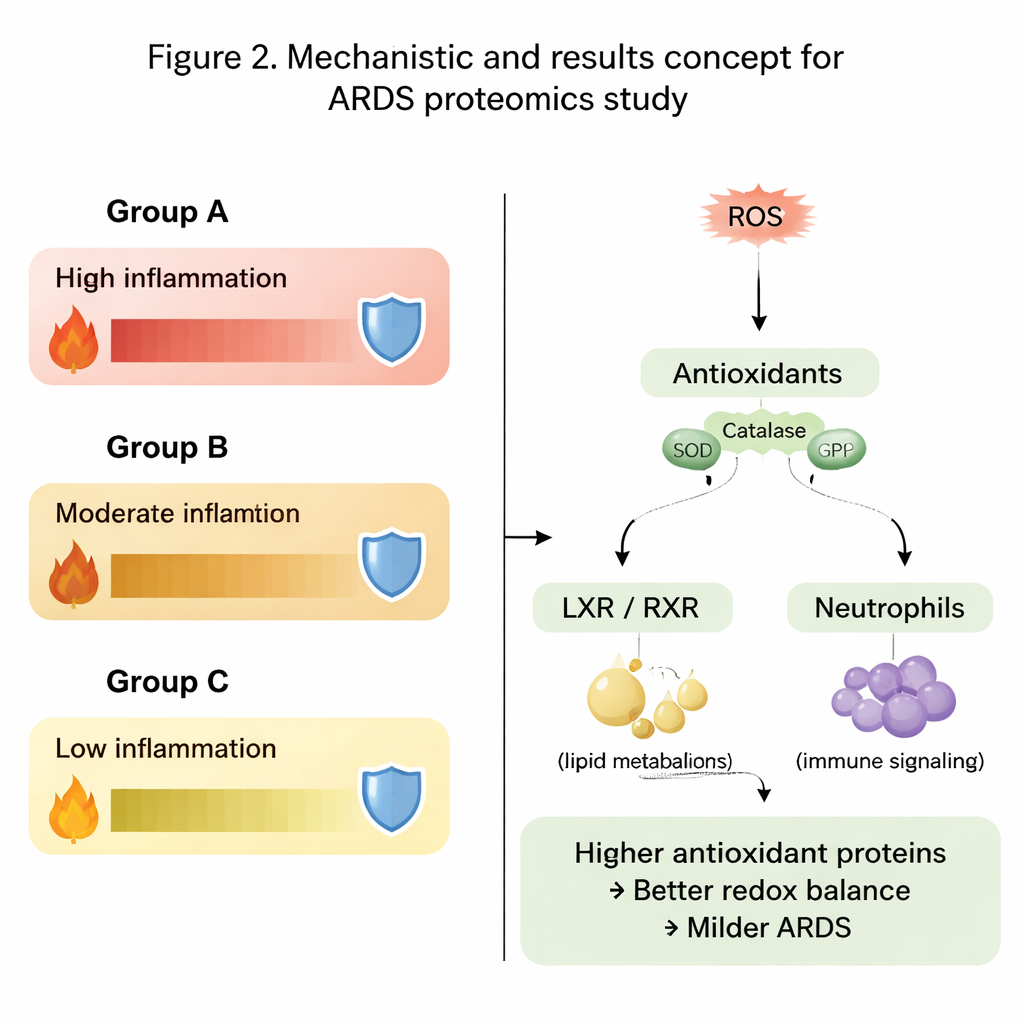
مسارات الإشارة التي تشكل الالتهاب
بعيدًا عن البروتينات الفردية، فحص المؤلفون مسارات بيولوجية كاملة. وجدوا أن المسارات المرتبطة بالالتهاب، والتعامل مع الكوليسترول والدهون، ونشاط خلايا المناعة تصرفت بشكل مختلف عبر المجموعات الثلاث. كانت الإشارات المرتبطة بمسار مستقبلات X الكبدي–مستقبلات X الريتينويد (LXR/RXR) وإنزيم يسمى DHCR24، اللذين يساعدان معًا في تنظيم أيض الدهون والاستجابات المناعية، بارزة بشكل خاص. في المجموعة الأكثر شدة، تَوَقَّع الباحثون أن هذه المسارات كانت أكثر نشاطًا، مقترنة بانخفاض إشارة الرسول المناعي إنترلوكين-12. في الوقت نفسه، أظهرت المسارات التي تنطوي على تفاعلات الأكسجين التفاعلية وإزالتها ونشاط العدلات (خلايا الدم البيضاء) أنماطًا متباينة بين سائل الرئة والدم، مما يؤكد أن ما يحدث محليًا في الرئة قد يختلف عما يُرى في الدورة الدموية.
ما قد يعنيه هذا للرعاية المستقبلية
هذه الدراسة الاستكشافية الصغيرة لا تغير العلاج اليوم، وتحتاج نتائجها إلى تأكيد في مجموعات أكبر بكثير من المرضى. ومع ذلك، تُظهر أنه من خلال تحليل دقيق للبروتينات وحالتها المؤكسدة مباشرة في سائل الرئة—بدلًا من الاعتماد فقط على فحوص الدم أو درجات السرير—يمكننا تمييز أنواع فرعية ذات مغزى بيولوجي من ARDS. تختلف هذه الأنماط الفرعية في الإجهاد التأكسدي، والقدرة المضادة للأكسدة، والأيض، وإشارات المناعة، وتبقى مستقرة نسبيًا خلال الأيام الحرجة الأولى من المرض. في المستقبل، قد تساعد مثل هذه البصمات الجزيئية الأطباء على تصنيف مرضى ARDS إلى مجموعات أكثر دقة، واختيار علاجات مستهدفة ملائمة لكل نمط، وتصميم تجارب سريرية أذكى تزيد احتمالات إيجاد علاجات فعالة بالفعل.
الاستشهاد: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
الكلمات المفتاحية: متلازمة الضائقة التنفسية الحادة, بروتيوميات, الإجهاد التأكسدي, غسل القصبات الرئوي, العناية المركزة