Clear Sky Science · ar
خلل الميتوكوندريا واضطراب Ca2+ في الخلايا العصبية البشرية المشتقة من iPSC الحاملة لطفرة بريسينيلين‑1 يظهران تحت الضغط عبر آلية مستقلة عن MCU‑1
لماذا يهم هذا بالنسبة لمرض ألزهايمر
غالباً ما يُوصف مرض ألزهايمر من منظور تراكم لويحات البروتين اللاصقة في الدماغ، لكن قبل فقدان الذاكرة بفترة طويلة، قد تبدأ "محطات الطاقة" الصغيرة داخل الخلايا العصبية — الميتوكوندريا — وتعامل أيونات الكالسيوم في الخروج عن النظام. تستخدم هذه الدراسة خلايا عصبية بشرية مشتقة من خلايا جلدية لشخص حامل لطفرة عائلية معروفة لألزهايمر لطرح سؤال بسيط لكنه جوهري: متى، وبأي طريقة، يبدأ إنتاج الطاقة وتوازن الكالسيوم في الفشل؟
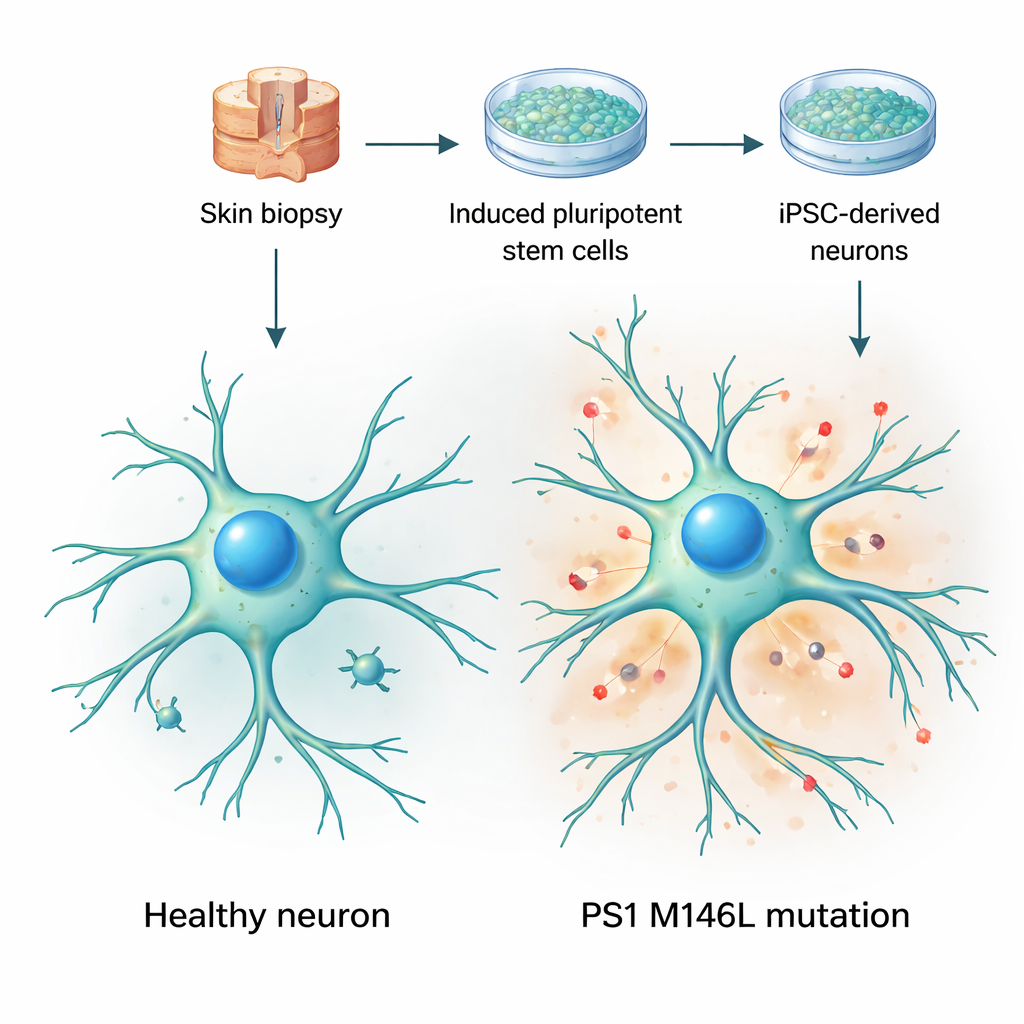
تحويل خلايا الجلد إلى نماذج دماغية حية
بدأ الباحثون بخزعات جلدية من امرأتين: متطوعة صحية وآخرى حاملة لطفرة بريسينيلين‑1 المعروفة باسم M146L، والتي تنتشر في عائلة أرجنتينية تعاني من بداية مبكرة لمرض ألزهايمر. أعادوا برمجة خلايا الجلد إلى خلايا جذعية مستحثة متعددة القدرات — قادرة على التحول إلى معظم الأنسجة — ثم حثّوها على التمايز إلى خلايا عصبية. خلال أسابيع من الزراعة، اكتسبت هذه الخلايا أشكالاً عصبية نموذجية، ومدت محاور متفرعة طويلة، وعبرت عن مؤشرات عصبية قياسية. والأهم أن خلايا التحكم والخلايا الحاملة للطفرات نمت بمعدلات مماثلة وبدا أنها بصحة عامة جيدة، ما سمح للفريق بالتركيز على التغيرات الوظيفية الطفيفة بدلاً من فقدان الخلايا الواضح أو التلف.
الإشارات الكهربائية والكالسيوم تحت الضغط
تعتمد الخلايا العصبية على ضبط محكم للكالسيوم، ذلك الذرّة المشحونة التي تعمل كمفتاح تشغيل/إيقاف سريع للعديد من العمليات الخلوية. باستخدام صبغات متوهجة، تتبع الفريق كيف تتغير مستويات الكالسيوم داخل الخلايا عند تحفيزها كهربائياً بالبوتاسيوم أو تنشيطها بجزيئات إشارية. تحت تحفيز بسيط مسبب لإزالة الاستقطاب، أظهرت الخلايا الحاملة لطفرة M146L زيادات أضعف في الكالسيوم مقارنة بخلايا التحكم، ما يشير إلى مشكلة في المحافظة على تدرجات الجهد واليونات التي عادة ما تدفع دخول الكالسيوم. ومع ذلك، عندما أثار الباحثون حالة أكثر إجهاداً — بإجبار تسرب الكالسيوم من مخازن داخلية في الشبكة الإندوبلازمية — أصبح الفرق أوضح. استجابةً لهذا الضغط، أخذت الميتوكوندريا في الخلايا الطافرة كمية أقل بكثير من الكالسيوم مقارنة بخلايا التحكم، مما يدل على قدرة مخفضة ع على عزل موجات الكالسيوم الخطيرة.
فصل استخدام الطاقة عن توازن الكالسيوم
لفهم كيف يؤثر هذا التعامل المعدّل مع الكالسيوم على أيض الخلايا، قاس الباحثون كمية الأكسجين التي تستهلكها الخلايا العصبية — مقياس مباشر لنشاط الميتوكوندريا. بشكل مفاجئ، بدت الخلايا الحاملة لطفرة M146L تتنفس أكثر: كانت معدلات استهلاك الأكسجين الأساسية والقصوى، ومقدار الأكسجين المرتبط بإنتاج ATP، كلها أعلى من خلايا التحكم. ومع ذلك، بدا أن كفاءة ربط استهلاك الأكسجين بإنتاج ATP متشابهة، ولم يكن هناك زيادة في عدد الميتوكوندريا أو في الأنزيمات الرئيسية لصناعة ATP. بدل ذلك، كانت الميتوكوندريا في الخلايا الطافرة أطول وأكثر أنبوبة، مع مستويات أعلى لبروتين الاندماج المسمى ميتوفوسين‑1، نمط يُرى غالباً في الخلايا المتعرضة لإجهاد مزمن منخفض المستوى. كما أنتجت هذه الميتوكوندريا المفرطة النشاط والمطولة المزيد من أنواع الأكسجين التفاعلية، وهي جزيئات غير مستقرة يمكن أن تتلف البروتينات والحمض النووي إذا لم تُضبط بشكل صحيح.
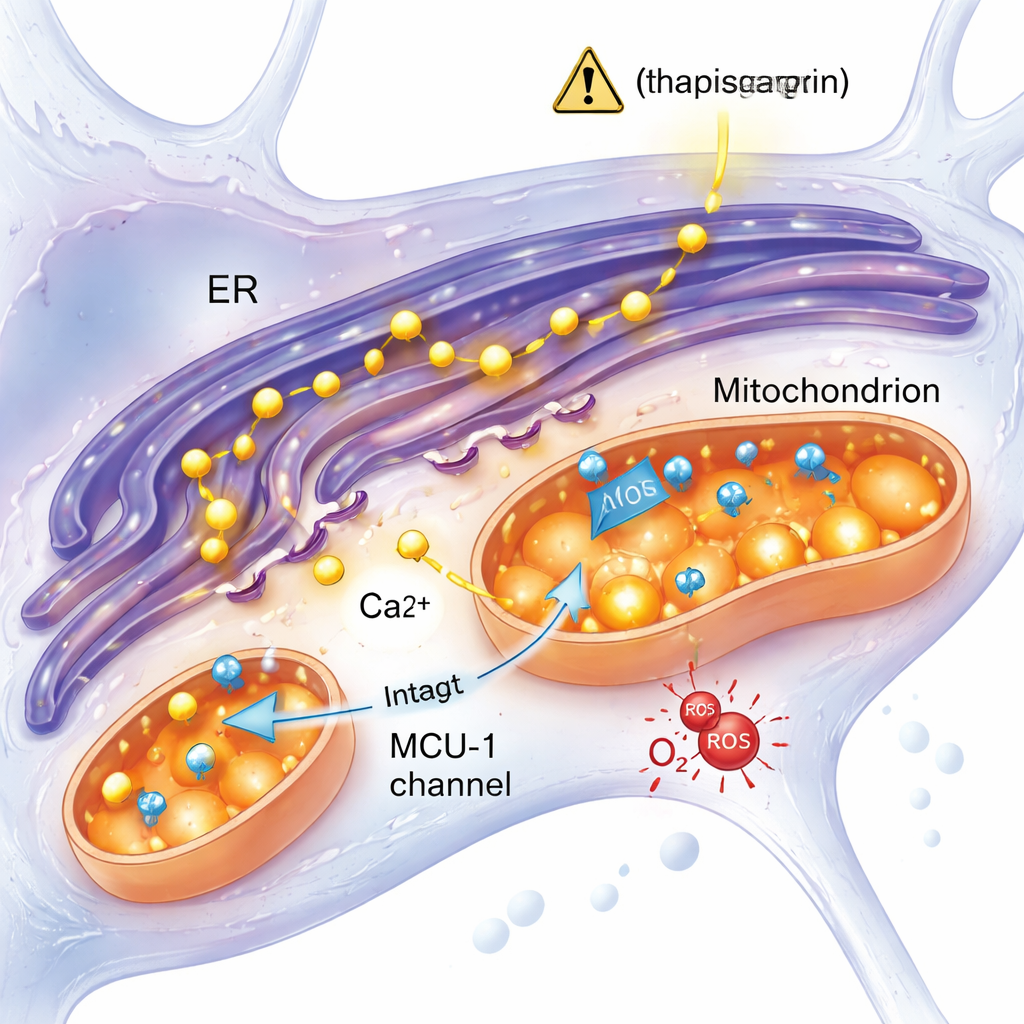
استجابة للضغط مستقلة عن قناة كالسيوم رئيسية
تتمثل إحدى الأفكار الرائدة في أبحاث ألزهايمر في أن فائض الكالسيوم من الشبكة الإندوبلازمية يندفع إلى الميتوكوندريا عبر قناة تسمى موحد ناقل الكالسيوم الميتوكوندري (MCU‑1)، فيغمرها ويدفعها إلى الخلل. اختبرت هذه الدراسة تلك الفكرة مباشرة. عندما قام الفريق بحجب MCU‑1 بمثبط محدد، أظهرت كل من خلايا التحكم والطافرة انخفاضات قوية في امتصاص الميتوكوندريا للكالسيوم، مؤكدة أن القناة نفسها تعمل في كلتا المجموعتين. علاوة على ذلك، عندما تم تحفيز إطلاق الكالسيوم عبر مسار أكثر فسيولوجية يشمل مستقبل IP3 — بوابة كالسيوم أساسية أخرى — استجابت الخلايا الطافرة والخلايا الضابطة بطريقة متشابهة. تشير هذه النتائج إلى ابتعاد الفكرة عن قناة MCU‑1 المعيبة وباتجاه احتمال أن تكون الاتصالات الفيزيائية والوظيفية بين الشبكة الإندوبلازمية والميتوكندريا، أو جوانب أخرى من تفاعلهما، مُعدلة في الخلايا الحاملة للطفرات.
ما الذي يعنيه هذا لفهم المرض وعلاجه
مجتمعة، تُصوّر النتائج خلايا عصبية بشرية حاملة لطفرة PS1 M146L في ألزهايمر على أنها خلايا تظهر طبيعية أثناء السكون لكنها تتفاعل بشكل غير طبيعي تحت الضغط. تفشل ميتوكوندرياتها في امتصاص كمية كافية من الكالسيوم عند إطلاق المخازن الداخلية فجأة، ومع ذلك تعمل بشكل أكثر نشاطاً — تستهلك مزيداً من الأكسجين وتنتج مزيداً من أنواع الأكسجين التفاعلية — كما لو أنها محبوسة في وضع تعويضي مكلف. لأن هذا يحدث في خلايا بشرية مشتقة حية قبل أية أعراض سريرية، يدعم العمل الفكرة القائلة بأن اضطراب إشارات الكالسيوم والإرهاق المبكر للميتوكوندريا هما أحداث مبكرة في مرض ألزهايمر، وليس مجرد نتاجات لاحقة. للقراء غير المتخصصين، الرسالة الأساسية هي أن الحفاظ على التوازن بين إشارات الكالسيوم وإنتاج الطاقة الميتوكوندرية قد يكون بنفس أهمية الوقاية من المرض مثل استهداف لويحات الأميلويد المعروفة أكثر.
الاستشهاد: Wilson, C., Galeano, P., Remedi, M.M. et al. Mitochondrial dysfunction and Ca2+ dysregulation in human iPSC-derived neurons carrying presenilin-1 mutation arise under stress via an MCU-1-independent mechanism. Sci Rep 16, 6002 (2026). https://doi.org/10.1038/s41598-026-35597-0
الكلمات المفتاحية: مرض ألزهايمر, الميتوكوندريا, إشارة الكالسيوم, طفرة بريسينيلين‑1, الخلايا العصبية المشتقة من iPSC