Clear Sky Science · ar
التطوير المدعوم هيكليًا وحاسوبيًا لمشتقات 2,5-ثنائية الاستبدال-1,3,4-أوكساديازول كمثبطات فعالة لـ LOX واليورياز وألفا-غلوكوزيداز
أدوات كيميائية جديدة لمواجهة أمراض شائعة
تدفع العديد من المشكلات الصحية اليومية — من التقرحات وحصى الكلى إلى السكري والالتهاب المزمن — بواسطة إنزيمات مفرطة النشاط في أجسامنا. تستكشف هذه الدراسة عائلة من الجزيئات الصغيرة المصممة حديثًا التي تعمل كفرامل صغيرة لثلاثة من هذه الإنزيمات. من خلال ضبط هياكلها واختبارها في المختبر وعلى الحاسوب، يسعى الباحثون إلى تمهيد الطريق لأدوية أكثر فاعلية وأمانًا في المستقبل. 
لماذا تهم هذه الإنزيمات
ركز الفريق على ثلاثة أهداف إنزيمية تلعب أدوارًا مختلفة ولكنها متساوية الأهمية في الصحة. يساعد اليوريز على تفكيك اليوريا؛ عندما يصبح مفرط النشاط في بعض البكتيريا أو الأنسجة، يمكن أن يساهم في تقرحات المعدة والمجاري البولية، وحصى الكلى، وحتى ارتفاع ضغط الدم. يجلس ألفا-غلوكوزيداز على سطح خلايا الأمعاء ويقطع الكربوهيدرات المعقدة إلى جلوكوز؛ ويُعد حظره طريقة راسخة للمساعدة في التحكم في سكر الدم في داء السكري من النوع الثاني. يحول الليبوكسجيناز (LOX) الدهون إلى جزيئات إشارات تدفع الالتهاب والربو وبعض العمليات المرتبطة بالسرطان. لذلك، تُعد الأدوية التي تبطئ هذه الإنزيمات دون الإضرار بأنظمة أخرى مطلوبة بشدة.
بناء مكتبة من الجزيئات المرشحة
للبحث عن مثل هذه الأدوية، أنشأ الباحثون سلسلة من 15 مركبًا مرتبطًا تعتمد على نظام حلقي يُدعى 1,3,4-أوكساديازول مرتبطًا بوحدة بيبيريدين. يظهر هذا السقالة الكيميائية بالفعل في عدة أدوية حديثة ومعروف أنها تتفاعل جيدًا مع الأهداف البيولوجية. نوَّع الفريق "الزينة" المرفقة بهذا اللب — مجموعات صغيرة مثل الميثيل، الإيثيل، الميثوكسي، البنزيل، والسيكلوهكسيل — في مواضع مختلفة، مكوِّنين مكتبة صغيرة من المرشحين الموسومين 7a حتى 7o. أكدوا كل هيكل باستخدام أدوات تحليلية معيارية مثل طيف الأشعة تحت الحمراء والرنين المغناطيسي النووي، ضامنين أن ما صنعوه يتوافق مع تصميماتهم.
اختبار مدى قدرة الجزيئات على حجب الإنزيمات
ثم اختبر كل مركب ضد LOX واليورياز وألفا-غلوكوزيداز المنقى لمعرفة مدى قدرته على إبطاء نشاط الإنزيم. برزت عدة جزيئات. ضد ألفا-غلوكوزيداز، كان المركبان 7a و7n فعّالين بشكل خاص، متفوقين على دواء السكري القياسي أكاربوز في اختبارات المختبر من حيث تحقيق نسب عالية من التثبيط عند تراكيز ميكرومولارية منخفضة. بالنسبة لـ LOX، أظهر المركبان 7a و7h و7n نشاطًا قويًا جدًا، في بعض الحالات أفضل من مثبط المرجع الطبيعي الكيرسيتين. في تجارب اليوريز، نافس المركبان 7a وخاصة 7l المثبط القياسي ثييويوريا، بل وتفوقا عليه قليلًا في بعض الاختبارات، مما يشير إلى إمكاناتهما كقواعد لمعالجات مضادة للقرحة أو مضادة لحصى الكلى في المستقبل. 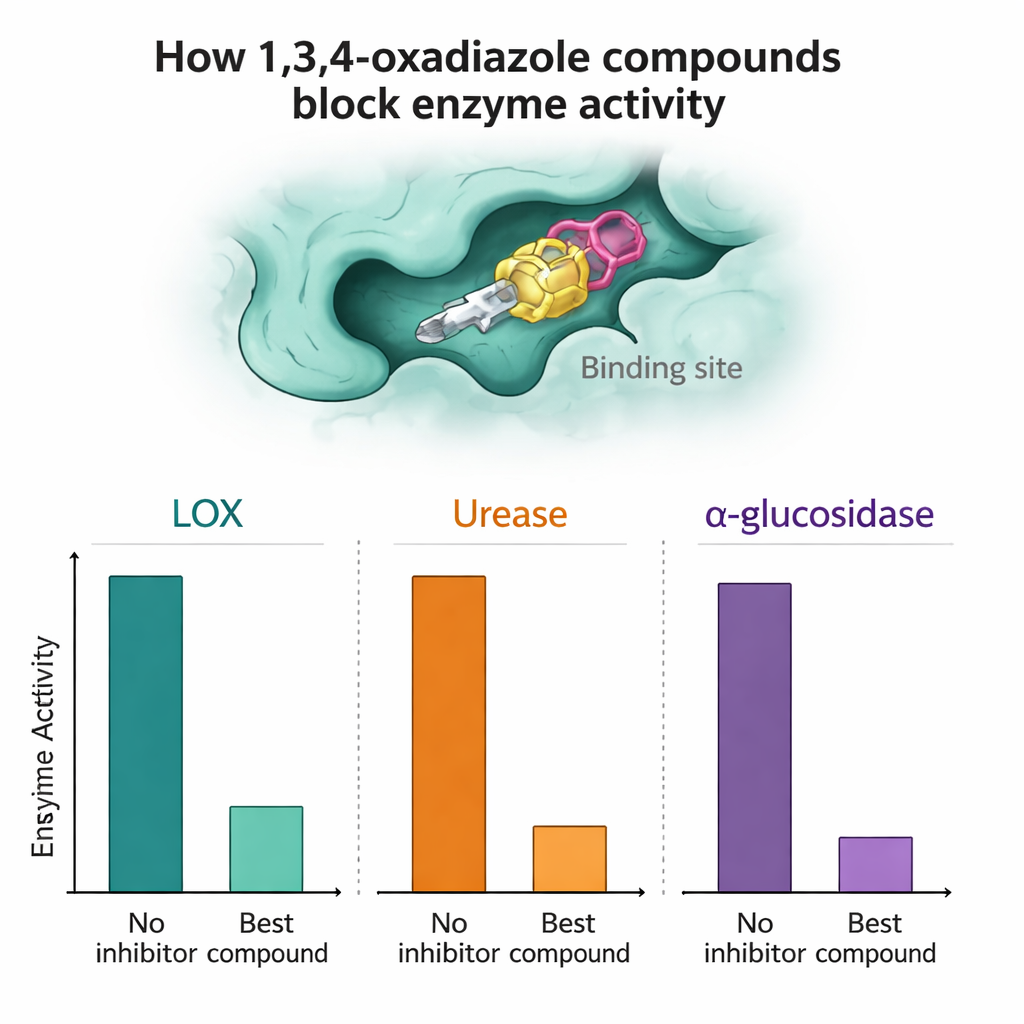
ربط البنية بالأداء
بما أن الاختلافات بين المركبات 7a–7o تتلخص في تغييرات صغيرة حول نظام الحلقة الأساسية، تمكن الباحثون من البدء في رسم علاقات بنية-نشاط بسيطة. على سبيل المثال، أدت إضافة مجموعات كربونية صغيرة في مواضع "أورثو" معينة على حلقة ملحقة إلى تعزيز القدرة على حجب ألفا-غلوكوزيداز أو LOX في كثير من الأحيان. أما الاستبدالات الأخرى، مثل بعض مجموعات الميثوكسي أو الإستر الموضوعة في مواضع أقل ملاءمة، فتميل إلى إضعاف النشاط. لفهم السبب، استخدم الفريق محاكاة حاسوبية. أظهرت الحسابات الكمومية الكيميائية أن جميع الجزيئات كانت مستقرة من حيث الثرموديناميكا ومرنة بما يكفي لتتكيف مع تجاويف الإنزيمات. كشفت دراسات الركن — الملاءمة الافتراضية لكل جزيء داخل نماذج ثلاثية الأبعاد للإنزيمات — أن المركبات الأكثر نشاطًا أحرزت اتصالًا أوثق من خلال مزيج من روابط الهيدروجين والتفاعلات الكارهة للماء (شبيهة بالزيوت) في نقاط رئيسية في مواقع الفاعلية، بينما جلست المرشحات الأضعف أقل إحكامًا أو فاتتها نقاط اتصال حرجة.
ماذا يعني هذا للأدوية المستقبلية
بعبارات بسيطة، تحدد الدراسة عددًا من "المفاتيح" الواعدة التي تتناسب جيدًا مع ثلاثة "أقفال" مرتبطة بالأمراض وتبدأ في تفسير، على مستوى ذري، لماذا تدور بعض المفاتيح أفضل من غيرها. لا أي من هذه الجزيئات جاهز ليصبح دواءً بعد — فهي لا تزال بحاجة إلى اختبارات سلامة، وتحسين للسلوك داخل الجسم، وتجارب على الحيوانات والبشر. لكن العمل يبيّن أن إطار 1,3,4-أوكساديازول–بيبيريدين يمثل نقطة انطلاق خصبة لعلاجات مستقبلية تستهدف السكري والحالات الالتهابية والاضطرابات المرتبطة باليورياز. توفر مقاربة الجمع بين قياسات مخبرية دقيقة ونمذجة حاسوبية مفصلة خارطة طريق لصقل هؤلاء المرشحين إلى أدوية أكثر دقة وفاعلية.
الاستشهاد: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
الكلمات المفتاحية: مثبطات الإنزيم, اكتشاف الأدوية, مركبات الأوكساديازول, السكري والالتهاب, اليوريز والليبوكسجيناز