Clear Sky Science · ar
SHP2 يعزز سرطان العظام عن طريق تنظيم إشارات STAT3/TET3/HOXB2
لماذا تهم هذه الدراسة لسرطان العظام
سرطان العظام العظمي (أوستيوبلاستوما) هو أكثر سرطانات العظام الأولية شيوعًا لدى الأطفال والمراهقين، وعلى الرغم من العلاج الكيميائي والجراحة الحديثة، فلم يتحسّن البقاء على قيد الحياة لدى المرضى الذين لديهم مرض متقدّم أو متكرر إلا قليلًا على مدار عقود. تتعمق هذه الدراسة في البنية الداخلية لخلايا الورم لتحديد الجزيئات التي تعمل كـ"مفاتيح رئيسية" تساعد على نمو الورم وانتشاره ومقاومته للعلاج. من خلال كشف مسار تحكم رئيسي يتمحور حول بروتين يُسمى SHP2، تشير الدراسة إلى أهداف دوائية جديدة قد تجعل علاجات السرطان العظمي أكثر فعالية ودقة في المستقبل.
اتباع الأدلة في نشاط جينات الورم
بدأ الباحثون بالتعامل مع سرطان العظام كمشكلة بيانات. استخرجوا مجموعات بيانات عامة لتعبير الجينات تقارن عينات الأورام بنسيج العظم الطبيعي، ثم استخدموا أدوات إحصائية لتمييز الجينات التي تظهر تغيّرًا ثابتًا في السرطان. اختلفت مئات الجينات، وكان كثير منها مرتكزًا في مسارات سرطانية معروفة تدفع النمو الخلوي والبقاء والحركة. من بينها، برز بروتين واحد، SHP2، كمركز مرتبط بقوة بعدد من العوامل الأخرى: عامل الإشارة STAT3، وإنزيم تعديل الحمض النووي TET3، والمنظم التطوري HOXB2. وقد اقترح هذا أن هذه الجزيئات قد تشكل سلسلة مترابطة تساعد خلايا الورم على التصرف بشكل عدواني. 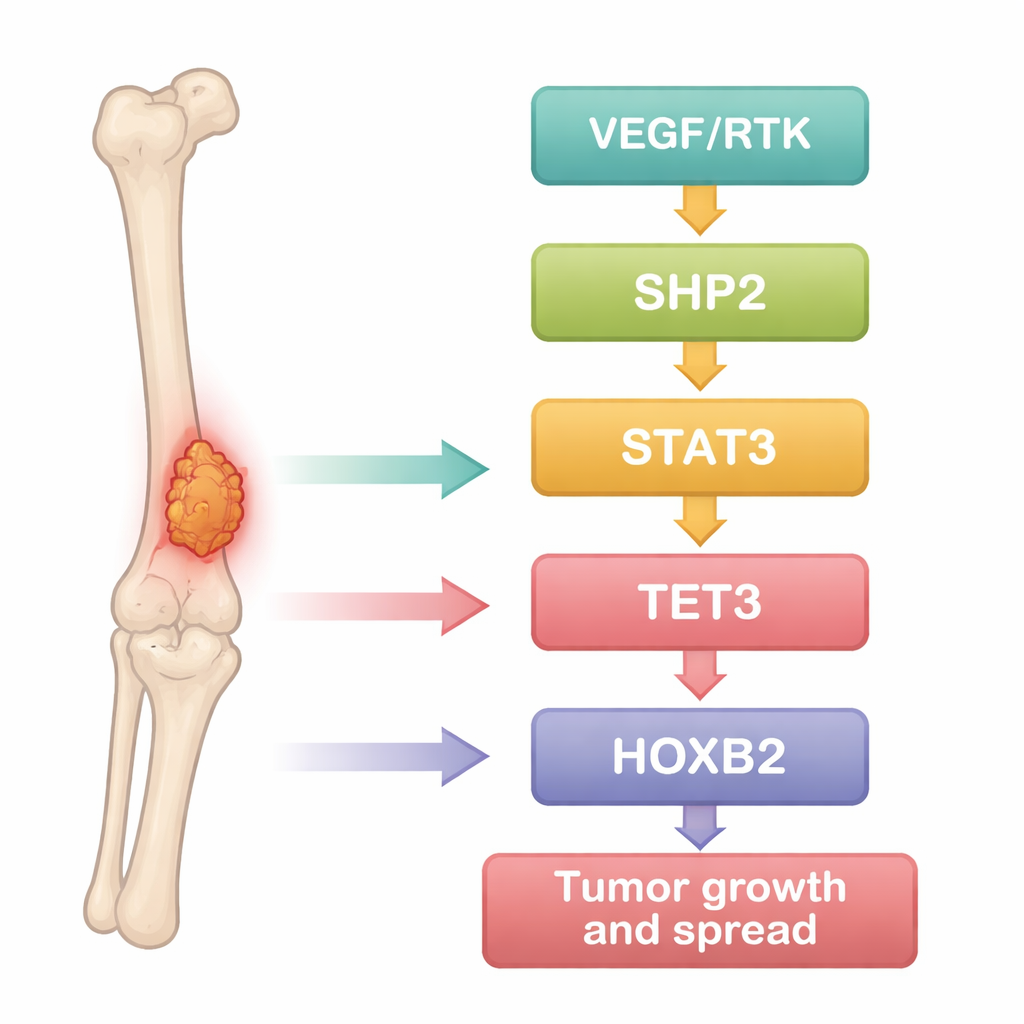
اختبار دور SHP2 في خلايا السرطان
للانتقال من الارتباطات إلى السببية، مهَّد الفريق خطوط خلايا سرطانية بشرية لعظام (143B وMG63) لتقليل أو زيادة تعبير SHP2. عند خفض مستوى SHP2، انخفضت قدرة الخلايا على التكاثر والهجرة عبر سطح والغزو عبر غشاء بشكل ملحوظ. كما انخفضت مستويات بروتينات STAT3 وTET3 وHOXB2، بالإضافة إلى مؤشرات مرتبطة بالسرطان مثل c-Myc وNANOG وNUSAP1. عند إعادة تنشيط STAT3 أو زيادة تعبير HOXB2، انقلبت كثير من هذه التأثيرات، مما يدل على أن SHP2 يقع في موقع علوي لسلسلة تؤثر في نهاية المطاف على جينات تتحكم في انقسام الخلايا وخصائص شبيهة بالخلايا الجذعية وآليات الانقسام الخلوي.
بناء مسار سرطاني خطوة بخطوة
بجمع نتائج التجارب، يصف المؤلفون نموذجًا تدريجيًا. في بيئة الورم، تحفز مستويات مرتفعة من عامل نمو بطانة الأوعية الدموية (VEGF) مستقبلات التيروزين كيناز (RTKs) على سطح الخلية. هذه المستقبلات تنشط بدورها SHP2 داخل الخلية. يقوم SHP2 النشط بتشغيل STAT3، وهو عامل نسخي ينتقل إلى النواة ويساهم في زيادة إنتاج TET3. يقوم TET3 بعد ذلك بتحرير العلامات الكيميائية على الحمض النووي، وبالأخص إزالة مجموعات الميثيل من منطقة جين HOXB2. تعمل هذه إزالة الميثلة كما لو أنها ترفع فرملة، مما يسمح بتعبير أقوى لـ HOXB2. وبدوره، يعزز HOXB2، وهو جين يوجه التطور عادة، نشاط c-Myc وNANOG وNUSAP1، التي تغذي معًا نموًا متسارعًا للخلايا الورمية، وتزيد السلوك الغازي، وتدعم ميزات مرتبطة بالانبثاث.
من طبق بتري إلى حيوانات حية
للتحقق مما إذا كان هذا المسار ذو أهمية في الأورام الكاملة، زرع العلماء خلايا سرطان عظام معدّلة تحت جلد الفئران. نمت الأورام المتكوّنة من خلايا تفرز SHP2 بكثرة لتصبح أكبر وأثقل من أورام الضبط. عندما تم إسكات TET3 في هذه الخلايا الغنية بـ SHP2، تباطأ نمو الورم وانخفضت مستويات HOXB2، رغم استمرار نشاط SHP2 وSTAT3. أعادت إعادة إدخال HOXB2 النشاط الورمي. على طول المسار، عكست قياسات مستويات البروتين في نسيج الورم نتائج تجارب الزراعة الخلوية السابقة، مما عزز الفكرة بأن SHP2 وSTAT3 وTET3 وHOXB2 تعمل كمحور مترابط يدفع سرطان العظام نحو سلوك أكثر خبيثة. 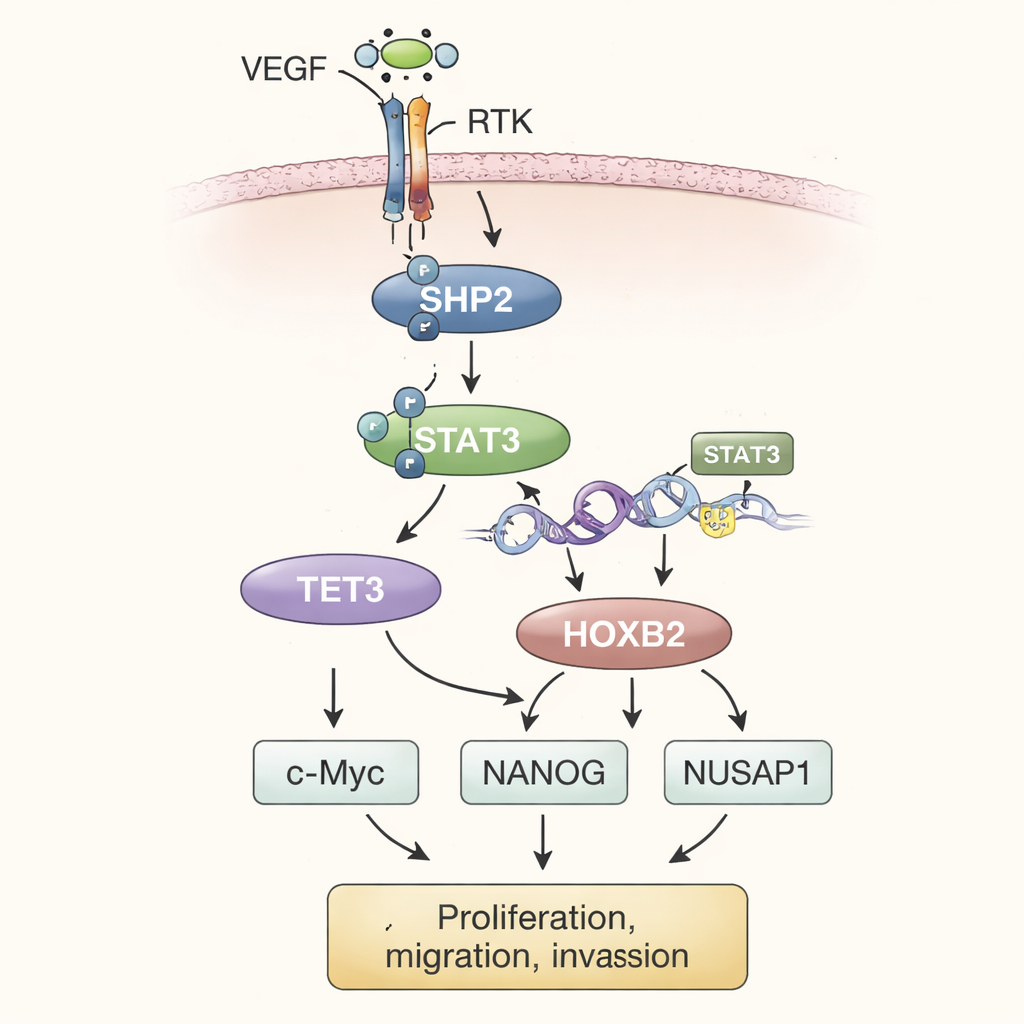
ما الذي يعنيه هذا لعلاجات المستقبل
للقارئ العادي، الخلاصة هي أن الباحثين تتبعوا سلسلة إشارية واضحة — من VEGF ومستقبلاته السطحية، عبر SHP2 وSTAT3، وصولًا إلى TET3 وHOXB2 وعدد من جينات النمو القوية — تشرح سبب نمط نمو سرطان العظام السريع وانتشاره المبكر. وبما أن SHP2 وSTAT3 إنزيمات يمكن نظريًا حجبها بواسطة أدوية جزيئية صغيرة، بينما يمثل TET3 وHOXB2 خطوات لاحقة في نفس الطريق، يوفر هذا المسار عدة نقاط يمكن للعلاجات المستقبلية التدخل عندها. ومع أن الدراسة أُجريت في خطوط خلوية وفي فئران، فإنها تزود مطوّري الأدوية بخريطة تفصيلية لتصميم علاجات مركبة تهدف إلى إيقاف مفاتيح التحكم المركزية للورم بدلاً من مجرد مهاجمة نتائجها النهائية.
الاستشهاد: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
الكلمات المفتاحية: سرطان العظام, SHP2, مسار STAT3, إشارات الورم, العلاج الموجَّه