Clear Sky Science · ar
تطوير نظام فحص عالمي للكشف عن تداخلات البروتين–بروتين بواسطة إكمال التلألؤ في خميرة الانشطار
إضاءة الحياة الخفية للبروتينات
كل نبضة قلب أو فكرة أو نفس في أجسامنا يعتمد على تعاون البروتينات داخل الخلايا. هذه الشراكات الصغيرة، المسماة تداخلات البروتين–بروتين، تتحكم في كل شيء من طريقة قراءة الجينات إلى استجابة الخلايا للإجهاد. ومع ذلك، فإن العديد من هذه الشراكات عابرة أو حساسة، مما يجعل الكشف عنها صعبًا باستخدام الأدوات الحالية. تصف هذه الدراسة نظام فحص جديد عالي الحساسية «قائم على الضوء» مبني في كائن نموذجي بسيط، خميرة الانشطار، ليكشف آلافًا من هذه الاتصالات البروتينية الخفية دفعة واحدة.
لماذا من الصعب رؤية شراكات البروتين
نادرًا ما تعمل البروتينات بمفردها. فهي ترتبط بشركاء مختلفين في أوقات مختلفة، أحيانًا لبرهة فقط، ويمكن أن يتغير سلوكها بواسطة تعديلات كيميائية أو بموقعها داخل الخلية. تميل الطرق التقليدية لدراسة هذه التداخلات إلى سحب البروتينات من بيئتها الطبيعية أو تعتمد حِيَلًا جينية لا تلتقط كل الاقترانات. ونتيجة لذلك، فإن خرائط التفاعل الحالية غير مكتملة. سعى المؤلفون لتحسين هذه الصورة بإنشاء نظام أكثر مرونة وحساسية يمكنه مسح تقريبًا كل بروتين في خميرة الانشطار داخل خلايا حية.
تحويل اللمس إلى ضوء
في قلب النهج الجديد يوجد إنزيم مقسّم يصدر ضوءًا. يُربَط جزء واحد، يُسمى LgBiT، ببروتين «طُعم» يرغب الباحثون في دراسته. ويُربَط الجزء الآخر، SmBiT، بالعديد من الشركاء المحتملين «فريسة»، واحدًا في كل سلالة خميرة. بمفردهما، تكاد هاتان القطعتان تتفاعلان. ولكن عندما يرتبط بروتين الطُعم بالبروتين الفريسة داخل الخلية، تنضم القطعتان معًا مجددًا، مُشكِّلتين إنزيمًا يعمل ويُضيء بوجود وقود كيميائي. بقياس كمية الضوء التي تنتجها كل سلالة خميرة، يمكن للفريق تحديد أي البروتينات تلتقي فعليًا داخل الخلية ومدى قوة تفاعلها. ولتجنب فقدان شركاء لأن الوسم يمنع الوظيفة الطبيعية، يُصنع بروتين الطُعم بنسختين، مع LgBiT مربوطًا إما بالطرف الأميني أو الطرف الكربوكسيلي، ما يزيد كثيرًا من احتمالية أن تعمل على الأقل واحدة من الاتجاهين. 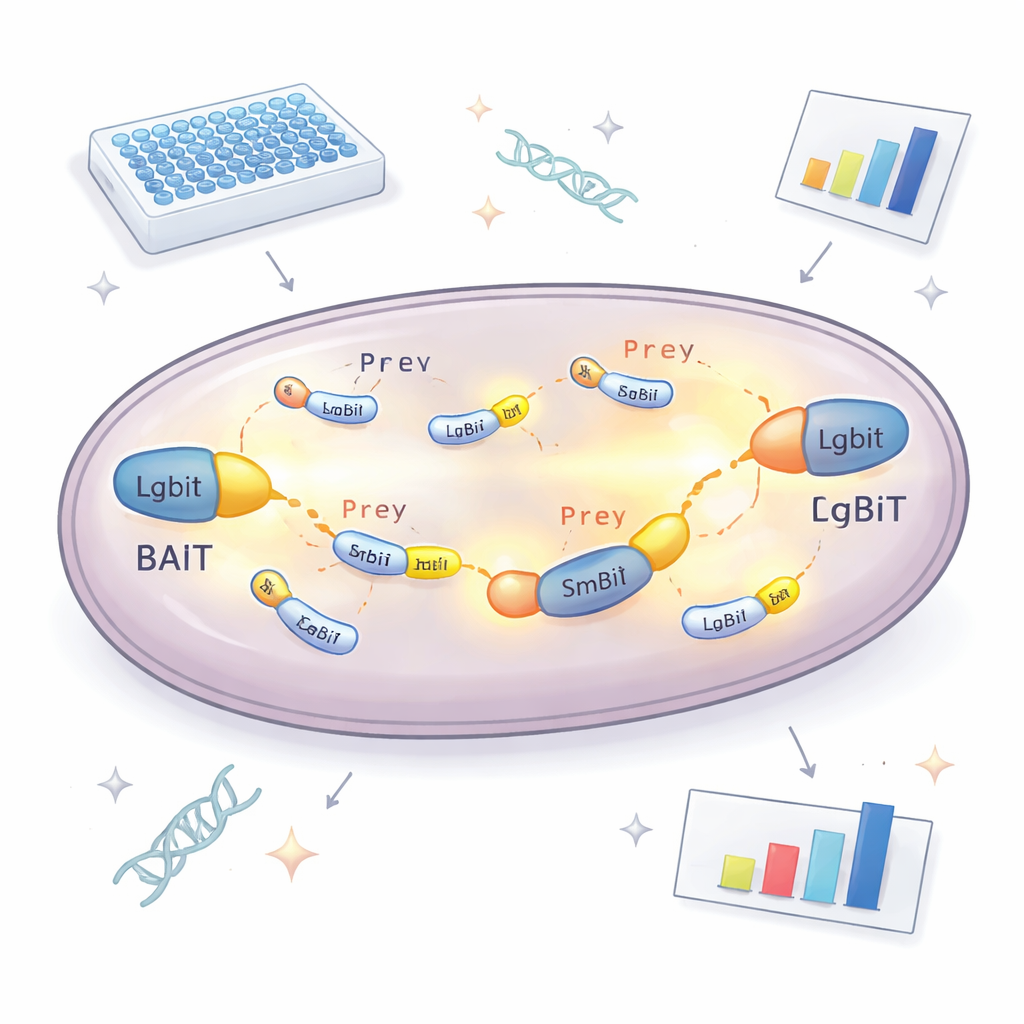
هندسة مكتبة خميرة ونظام سلالات
لم يتطلب بناء هذه المنصة إنزيمًا ذكيًا فحسب. كان على الباحثين أيضًا إدخال آلاف بروتينات الفريسة إلى الخميرة بطريقة مسيطرة وعلى نسخة واحدة فقط. صمموا ناقل DNA خاصًا لبروتينات الفريسة يندمج في موقع معرف في جينوم الخميرة ويحمل علامة فلورية حمراء. يعكس توهج هذه الإشارة الحمراء عدد النسخ المدرجة، ما يسمح للفريق باختيار المستعمرات التي تحتوي بالضبط على نسخة واحدة بسهولة، وهو أمر حاسم للمقارنات الموثوقة. كما أنشأوا ناقلات طُعم مخصصة تضع LgBiT في بداية أو نهاية بروتين الطُعم، مفصولة بوصلات مرنة حتى يظل البروتين قادرًا على الطي والحركة طبيعيًا. ثم بُنيت سلالات خميرة مصممة بعناية لاستضافة بنائي طُعم ومركب فريسة واحد في آن واحد، باستخدام علامات غذائية لضمان بقاء الخلايا المجمعة بشكل صحيح فقط.
اختبار النظام
للتحقق مما إذا كان تصميمهم حسّن الكشف فعلاً، فحص العلماء أولًا بروتينات ذات شركاء معروفين جيدًا. أكدوا أن شدة الإشارة كانت تعتمد بقوة على مكان إرفاق الوسم المضيء: بعض التداخلات ظهرت فقط عندما كان LgBiT على طرف واحد من الطُعم، وليس على الطرف الآخر. وأدى تعبير النسختين معًا إلى تعزيز إشعاع الضوء، مما يثبت أن استراتيجية الطُعم المزدوج تجعل التداخلات الضعيفة أو الحساسة للاتجاه أسهل في الالتقاط. كشف النظام أيضًا عن تواصل يشمل بروتينات مرتبطة بالغشاء، وهي فئة يصعب كشفها عادةً بأساليب خميرة الهايبرد التقليدية. ومع هذا التحقق، قام الفريق بتوسيع النطاق إلى فحص على مستوى الجينوم، مستخدمين بروتينًا مرتبطًا بالنسخ يُدعى Tfs1 كطُعم. بفحص أكثر من 4600 بروتين فريسة، وجدوا 31 مرشحًا قويًا، بما في ذلك عدة شركاء معروفين وبعض الشركاء الجدد، بعضهم يقع خارج النواة في مواقع مثل الميتوكوندريا وسطح الخلية. 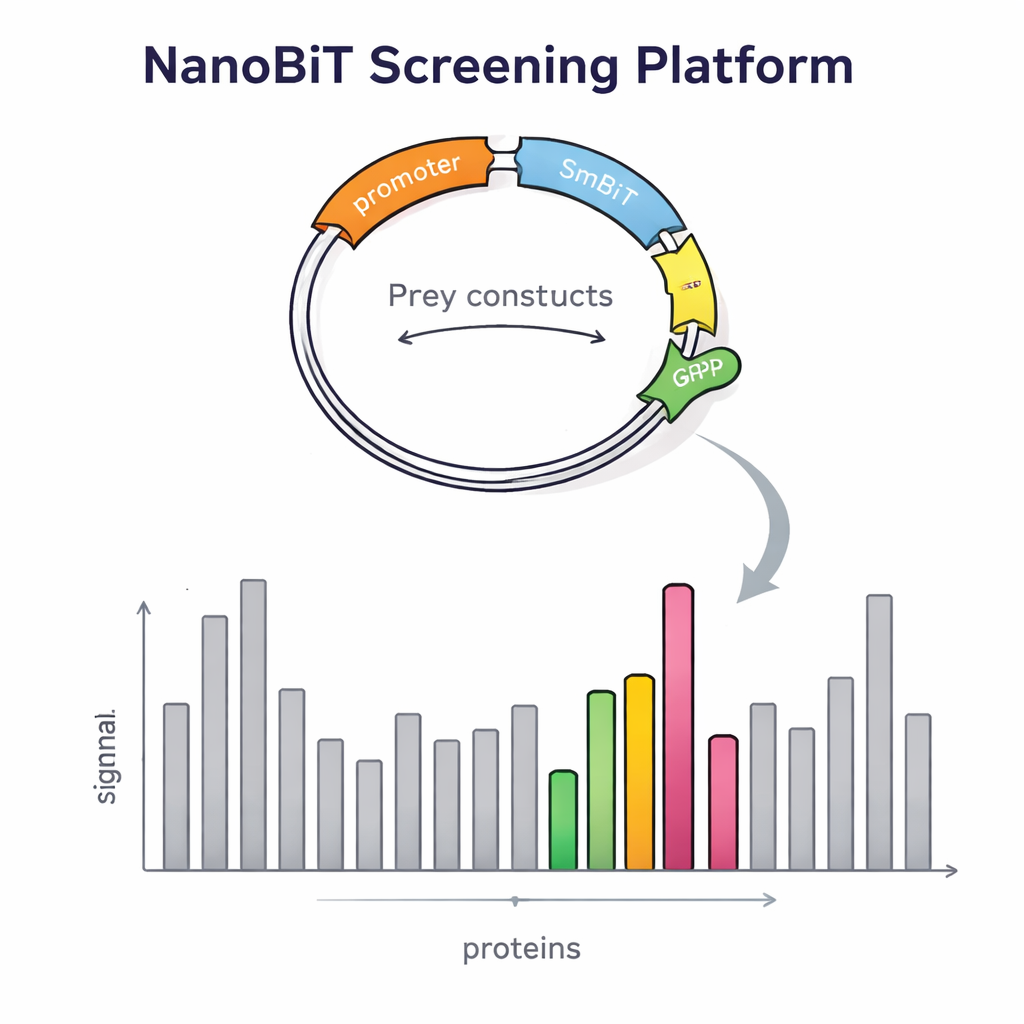
ما معنى هذا للأحياء واكتشاف الأدوية
لغير المتخصص، الرسالة الأساسية هي أن المؤلفين بنوا «رادار تفاعل» داخل خلايا الخميرة أكثر حساسية. بتحويل مصافحات البروتين القصيرة إلى ومضات ضوئية قابلة للقياس، وبترتيب الجينات بشكل ذكي بحيث يمكن التعبير عن ثلاثة بروتينات موسومة معًا، يكشف نظامهم عن شركاء بروتينيين معروفين وسابقًا غير مرئيين. وبينما لا تزال هناك حاجة لتحقق إضافي باستخدام تقنيات أخرى لتأكيد كل اقتران جديد، يملأ هذا النظام فراغات مهمة في خرائطنا للشبكات الخلوية. وبما أن السلالات صممت أيضًا لتكون أكثر حساسية للجزيئات الصغيرة، يمكن تكييف نفس الإعداد للبحث عن أدوية تعطل شراكات بروتينية ضارة أو تثبت شراكات مفيدة، مما يوفر أداة قوية لكل من علم الأحياء الأساسي واكتشاف الأدوية في مراحلها الأولية.
الاستشهاد: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
الكلمات المفتاحية: تفاعلات البروتين, خميرة الانشطار, قياس التلألؤ, الفحص عالي الإنتاجية, أدوات اكتشاف الأدوية