Clear Sky Science · ar
السرِيليّة المعتمدة على جسيم التعرف على الإشارة في البشر
كيف تقرر الخلايا أي البروتينات تترك الخلية
ترسل خلايانا باستمرار بروتينات تشكل هرمونات وأجسامًا مضادة والهيكل بين الأنسجة. لكن ليس كل بروتين مُعدًّا للسفر. تطرح هذه الدراسة سؤالًا أساسيًا لم يُجب عنه بالكامل بعد: كيف تقرر الخلايا البشرية أي البروتينات تعتمد على مساعد رئيسي يُدعى جسيم التعرف على الإشارة (SRP) للوصول إلى مركز الشحن الداخلي للخلية، وأيها يمكن أن يصل بدونه؟ من خلال تتبُّع هذا القرار عبر آلاف البروتينات في آن واحد، يكشف المؤلفون من يعتمد على SRP ومن لا يعتمد، وماذا يحدث عندما ينهار هذا النظام — وهو موضوع ذو صلة بالعديد من الأمراض المرتبطة بالبروتينات الموجهة بشكل خاطئ أو المفقودة.
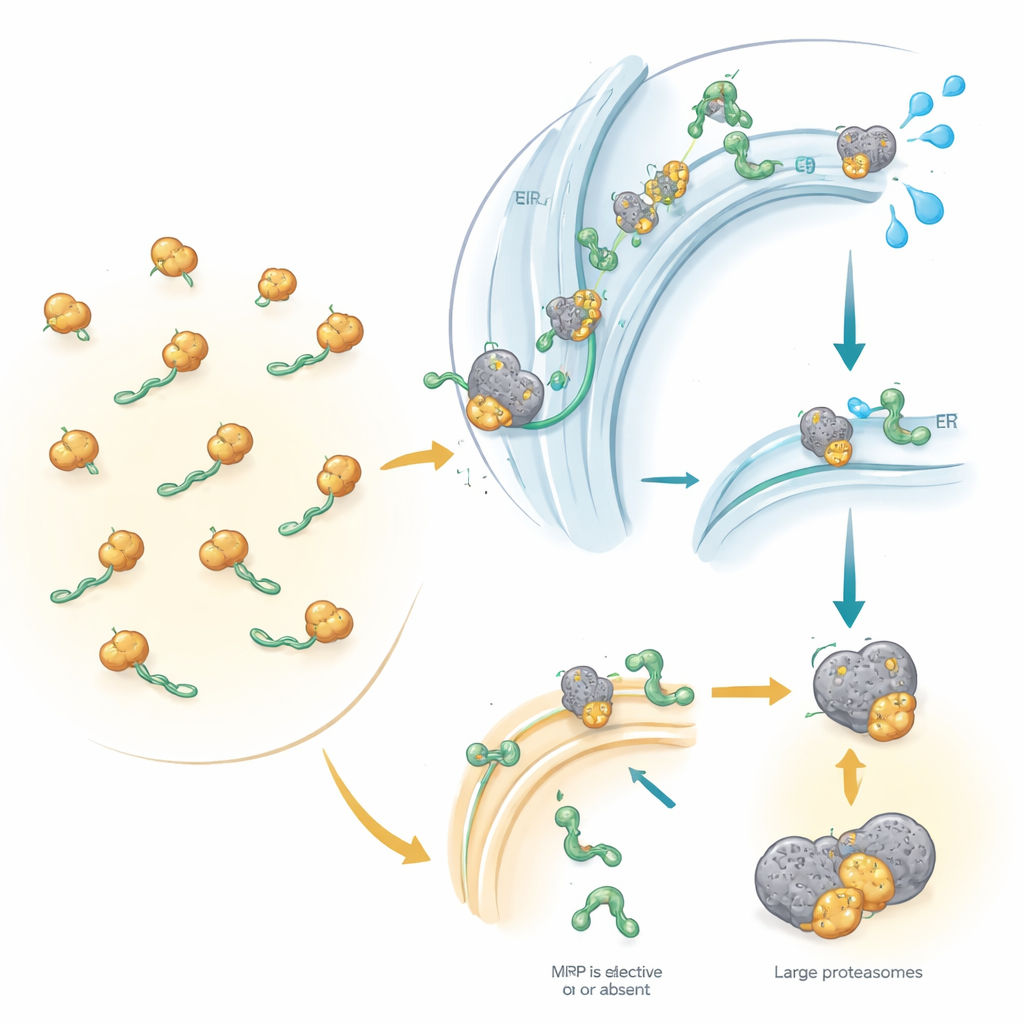
رصيف شحن الخلية ومرشده الرئيسي
حوالي واحد من كل ثلاثة بروتينات بشرية موجه إما لسطح الخلية أو أغشية الخلايا أو للإفراز خارج الخلية. للوصول إلى المكان الصحيح، يجب أن تدخل معظم هذه البروتينات أولًا شبكة من الأغشية الداخلية تُدعى الشبكة الإندوبلازمية، وهي رصيف شحن الخلية. يعمل SRP كمرشد: يتعرف على "علامة عنوان" صغيرة في بداية البروتينات المصنعة حديثًا ويوقف إنتاجها مؤقتًا. تمنح هذه الوقفة الريبوسوم — ماكينة صنع البروتين — وقتًا للتشبُّث بالشبكة الإندوبلازمية، حيث يستأنف الإنتاج ويُدفع البروتين النامي إلى داخل الغشاء أو من خلاله. مع ذلك، من المعروف أن بعض البروتينات تستخدم مسارات بديلة لا تتطلب SRP، خاصة البروتينات الصغيرة جدًا أو تلك المثبتة من نهاياتها الذيلية. وحتى الآن، لم يعرف العلماء على نطاق واسع أي البروتينات البشرية تحتاج فعلاً إلى SRP وأيها يمكن أن تتجاوزه.
خفض SRP لرؤية ما يتعطّل
للإجابة عن ذلك، خفّض الباحثون انتقائيًا مستويات أحد مكونات SRP الأساسية، SRP54، في خلايا هِيلا البشرية. ثم استخدموا تقنية حساسة تُدعى مطيافية الكتلة لقياس أكثر من 6000 بروتين داخل الخلايا وحوالي 2000 بروتين موجود في السائل المحيط، المعروف بالمُحَلّية المشروطة. سمحَ مقارنة الخلايا ذات مستويات SRP54 الطبيعية بتلك التي نُقِصت فيها SRP54 برؤية البروتينات التي انخفضت مستوياتها، والتي ارتفعت، والتي لم تتغير. اعتُبر الانخفاض القوي في مستوى البروتين — خصوصًا داخل الخلية وفي الوسط الخارجي — علامة على أن هذا البروتين يعتمد على SRP ليُصنع ويُوجَّه بشكل صحيح.
من يعتمد على SRP ومن يدبر أموره بدونه
أظهرت التحليلات أن معظم البروتينات التي تُفرَز عادةً إلى الوسط تعتمد بوضوح على SRP. عندما نُقِصَ SRP54، انخفضت غالبية هذه البروتينات المفرزة، خصوصًا تلك التي تحمل "علامة عنوان" إشارية تقليدية. كما تراجعت العديد من بروتينات الغشاء داخل الخلية، مما كشف عنها كعملاء لـ SRP. كانت هناك مجموعة أصغر من البروتينات ذات علامات عنوان مشابهة دون تأثير كبير، مما يجعلها مستقلة عن SRP؛ من المحتمل أنها تستخدم طرقًا بديلة للوصول إلى الشبكة الإندوبلازمية. كما اكتشف الباحثون أن خواصًا محددة في علامة العنوان — مثل منطقة مشحونة إيجابيًا في بدايتها — كانت أكثر شيوعًا بين البروتينات المعتمدة على SRP، مشيرةً إلى قواعد دقيقة تساعد SRP في اختيار حمولةه. وفي الوقت نفسه، ارتفع مستوى بعض البروتينات المشاركة في وضع علامات على البروتينات التالفة للتخلص منها وفي وظائف الميتوكوندريا، ما يشير إلى أن الخلايا تُفعّل أنظمة احتياطية وإنتاج الطاقة عندما يتعرض مرشد الشحن الرئيسي للمشكلات.
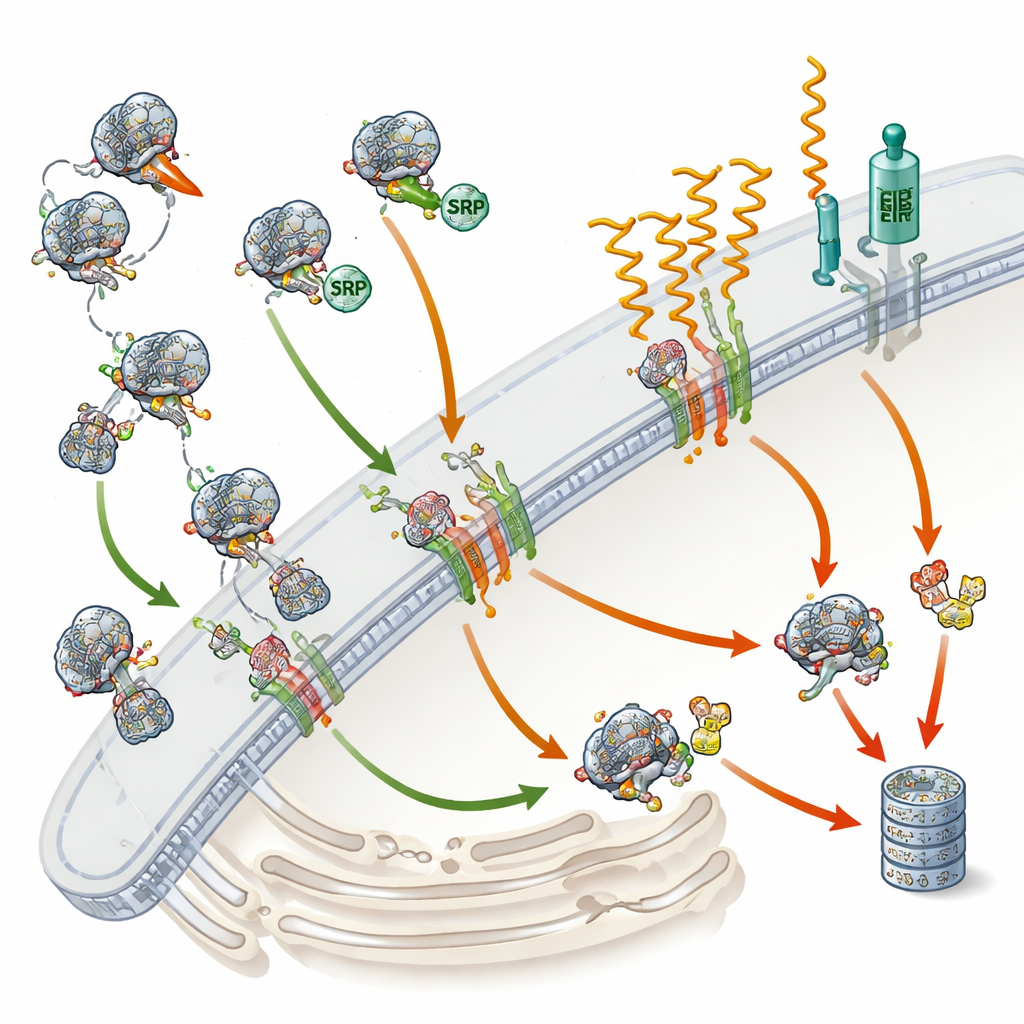
مراقبة الجودة عندما يخطئ الاستهداف
لم تقتصر الدراسة على عد البروتينات فحسب: بل قارنت هذه التغيرات بتحولات في الحمض النووي الريبي الرسول (mRNA)، المخططات المستخدمة لصنع البروتينات. فقد فقدت العديد من البروتينات المعتمدة على SRP ليس البروتين فحسب بل أيضًا مخططاتها النّسخية، مما يورط مسار مراقبة جودة معروفًا باسم RAPP. عندما لا يستطيع SRP أن يتعامل بشكل صحيح مع بروتين سكري أو غشائي ناشئ، يبدو أن هذا المسار يحفّز تحلل الـ mRNA المقابل، مانعًا استمرار إنتاج بروتين مُسيّء التوجيه. وفي الوقت نفسه، يُحتمل أن تُعلَّم البروتينات غير المكتملة التي تفشل في الوصول إلى الشبكة الإندوبلازمية بعلامات صغيرة وتُقدَّم إلى "الشارِدات" الخلوية المسماة البروتيازومات. ومن المثير أن مسارات الإجهاد الكلاسيكية في الشبكة الإندوبلازمية لم تُفعّل بقوة، ما يوحي بأن خللاً في SRP يثير نوعًا مميزًا من استجابة الإجهاد الخلوية.
ما الذي يعنيه هذا للصحة والمرض
من خلال رسم خريطة، لأول مرة في خلايا بشرية، للبروتينات المفرزة والغشائية المعتمدة على SRP وتلك المستقلة عنه، توفر هذه الدراسة خريطة مرجعية لقواعد شحن الخلية. تُظهر النتائج أن معظم البروتينات المصدَّرة تعتمد فعلاً على SRP وأنه عندما يتعطل SRP تستجيب الخلايا بتدمير البروتينات ومخططاتها النّسخية وتشغيل آليات مواجهة بديلة. وبما أن العديد من الطفرات المسببة للأمراض تؤثر على "علامات العنوان" في البروتينات المفرزة، فقد يساعد فهم كيف يتعرف SRP على عملائه وكيف يزيل RAPP العناصر المعيبة في تفسير سبب تسبب طفرات معينة في نقص هرمونات أو اضطرابات مناعية أو تنكس عصبي — وقد يشير في النهاية إلى طرق جديدة لضبط توجيه البروتين في الصحة البشرية.
الاستشهاد: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
الكلمات المفتاحية: إفراز البروتين, جسيم التعرف على الإشارة, السرِكتوم, مراقبة جودة البروتين, الشبكة الإندوبلازمية