Clear Sky Science · ar
التثبيط المتسلسل للبلاتين وPARP يعزز فعالية علاج المناعة PD1 في سرطان البنكرياس الفأري المطوَّر بطفرة Brca2
لماذا يهم هذا البحث للمرضى
يعد سرطان البنكرياس واحداً من أكثر السرطانات فتكاً، وحتى عندما يعرف الأطباء أن الورم يحمل نقطة ضعف مفيدة — مثل طفرة في جين BRCA2 — فإن العلاجات الحالية نادراً ما تحافظ على السيطرة على المرض لفترة طويلة. تستخدم هذه الدراسة نموذج فأري واقعي لطرح سؤال عملي يواجهه الآن العديد من المرضى والأطباء: بعد العلاج الكيميائي القوي ومثبط PARP، هل يمكن لإضافة علاج مناعي حديث أن تطيل البقاء بصورة ذات معنى، ولماذا تعود الأورام كثيراً؟
سرطان عنيد مع نقطة ضعف وراثية
سرطان غدد البنكرياس القنوي صعب العلاج بشكل ملحوظ، مع بقاء على قيد الحياة لخمس سنوات ما زال في خانة الأرقام الأحادية. يحمل جزء صغير من المرضى عيوب موروثة أو خاصة بالورم في BRCA2، وهو جين ضروري لإصلاح الحمض النووي المكسور. تكون هذه الأورام حساسة بشكل غير عادي للأدوية التي تتلف الحمض النووي، مثل العلاج الكيميائي القائم على البلاتين، ولـمثبطات PARP التي تضعف قدرة الخلايا السرطانية على إصلاح الحمض النووي بشكل أكبر. الرعاية القياسية الحالية لسرطان البنكرياس المتحور في BRCA المتقدم هي شهور من العلاج الكيميائي بالبلاتين تليها معالجة صيانة بمثبط PARP. ومع ذلك، في التجربة السريرية الرئيسية POLO، لم تُطِل هذه الاستراتيجية البقاء الإجمالي، مما يبرز الحاجة لفهم آليات المقاومة وتصميم أساليب صيانة أفضل.
بناء نموذج فأري أكثر واقعية
تجرد العديد من النماذج المخبرية الحالية المكونات المناعية والُنخاعية التي تحيط بالأورام الحقيقية لدى المرضى. وللتغلب على ذلك، صنع الباحثون فئراناً تطور أورام بنكرياس ناقصة BRCA2 في سياق جهاز مناعي يعمل بكامل طاقته. ومن هذه الأورام التلقائية استخلصوا خطوط خلايا استنسالية يمكن زرعها في فئران متطابقة جينياً. بدت هذه الأورام المتحورة في Brca2 وتصرّفت كثيراً مثل سرطانات البنكرياس البشرية: كانت ليفية بكثافة، ومعظمها يستبعد الخلايا التائية، وأبدت مستويات عالية من الضرر التلقائي في الحمض النووي. والأهم أن هذه الأورام كانت حساسة للغاية لتوليفة بلاتينية شائعة (جيمسيتابين مع سيسبلاتين)، بينما كان لمعالجة مثبط PARP وحدها تأثيرات متواضعة ومؤقتة لدى الحيوانات، بالرغم من نشاط قوي ضد نفس الخلايا في طبق الزرع. 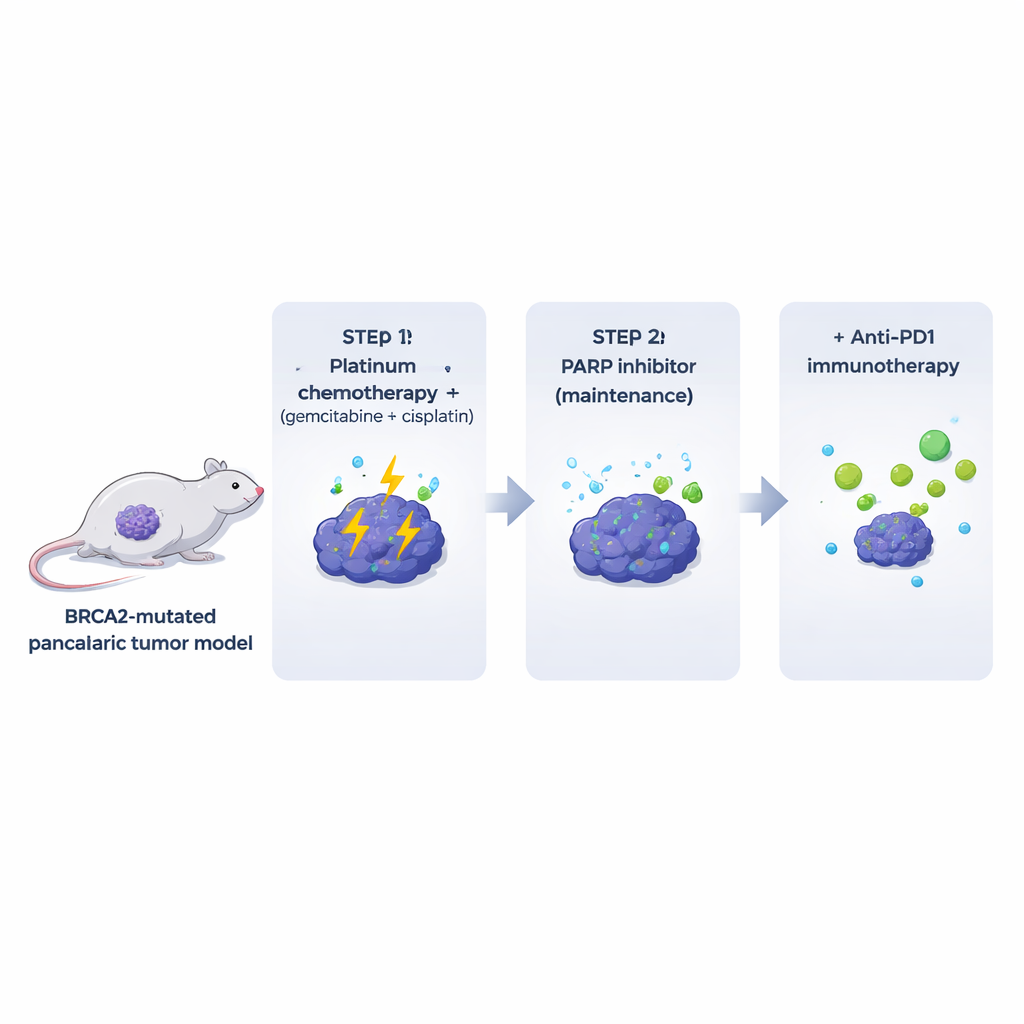
العلاج الكيميائي يعيد تشكيل محيط الورم
بعد ذلك سأل الفريق ماذا يحدث داخل الورم بعد العلاج بالبلاتين. بعد عشرة أيام من العلاج انكمشت الأورام لكنها لم تُقضَ عليها تماماً. كشفت تحليلات التعبير الجيني تحوّلاً لافتاً نحو نشاط متعلق بالمناعة: تم تشغيل المسارات المرتبطة بتنشيط الخلايا التائية والمناعة التكيفية. وُجدت خلايا تائية أكثر داخل الأورام المعالجة، وحملت العديد من هذه الخلايا علامات الإنهكا — دلالات على أنها تم تنشيطها لكنها بدأت تفقد فعاليتها. رُصدت أنماط مماثلة لزيادة وجود الخلايا التائية في سرطانات بنكرياس بشرية ذات طفرات في BRCA أو الجين ذي الصلة PALB2 بعد أن تلقى المرضى علاجاً بالبلاتين قبل الجراحة. وفي الوقت نفسه، زادت خلايا الورم مستويات PD-L1، وهو بروتين سطحي يمكنه إيقاف الخلايا التائية عبر التفاعل مع مستقبل PD-1، مما يوحي بأن الأورام كانت تدافع عن نفسها ضد هذا الضغط المناعي الجديد.
لماذا PARP وحده لا يكفي — وأين تنشأ المقاومة
مراعاةً لرعاية المرضى، أعطى الباحثون للفئران دورة أولية من جيمسيتابين وسيسبلاتين، تلاها صيانة بمثبط PARP أولاباريب. حسَّن هذا الترتيب التحكم في الورم والبقاء مقارنة بالعلاج الكيميائي وحده، مؤكداً أن العلاج الكيميائي السابق يمكن أن يجعل الأورام أكثر عرضة لتأثير مثبطات PARP. ومع ذلك، لم تُشفى أي فئران: في نهاية المطاف نمت الأورام مجدداً أثناء صيانة PARP. أظهرت الأورام المقاومة مظهراً أكثر تمايزاً وزيادة قوية في مستويات منظّم التطور CDX2. وهذا يقترح أن المقاومة، على الأقل في هذا النموذج، لا تنبثق ببساطة من إصلاح العيب الأصلي في إصلاح الحمض النووي، بل قد تنطوي على تحول في هوية خلايا الورم. قد يخدم CDX2 كعلامة حيوية محتملة على نشوء المقاومة لدى المرضى.
إطلاق العنان للعلاج المناعي بالتسلسل الصحيح
حوّلت أدوية تثبيط نقاط التفتيش المناعية مثل أضداد PD1 العلاج لعدة سرطانات، لكن سرطان البنكرياس ظل إلى حد كبير غير مستجيب. واتساقاً مع ذلك، فشل مضاد PD1 (مع أو بدون دواء آخر لموقع التفتيش، مضاد CTLA4) في المساعدة عندما أعطي للأورام المتحولة في BRCA2 دون علاج سابق، ولم يفعل الكثير كذلك عندما أضيف ببساطة إلى علاج مثبط PARP. تغيرت الصورة عندما استخدمت التسلسل الكامل: العلاج بالبلاتين أولاً، ثم مثبط PARP مع مضاد PD1 كعلاج صيانة. في هذا السياق انكمشت الأورام بعمق أكبر وعاشت الفئران فترة أطول مقارنة بالعلاج الكيميائي مع مثبط PARP أو مضاد PD1 بمفردهما. إضافة مضاد CTLA4 إلى صيانة PARP لم تؤدِّ إلى فوائد مماثلة، مما يوحي أن بيئة الورم الممهدة بالعلاج الكيميائي مهيَّأة على نحو خاص للاستجابة لحجب PD-1. 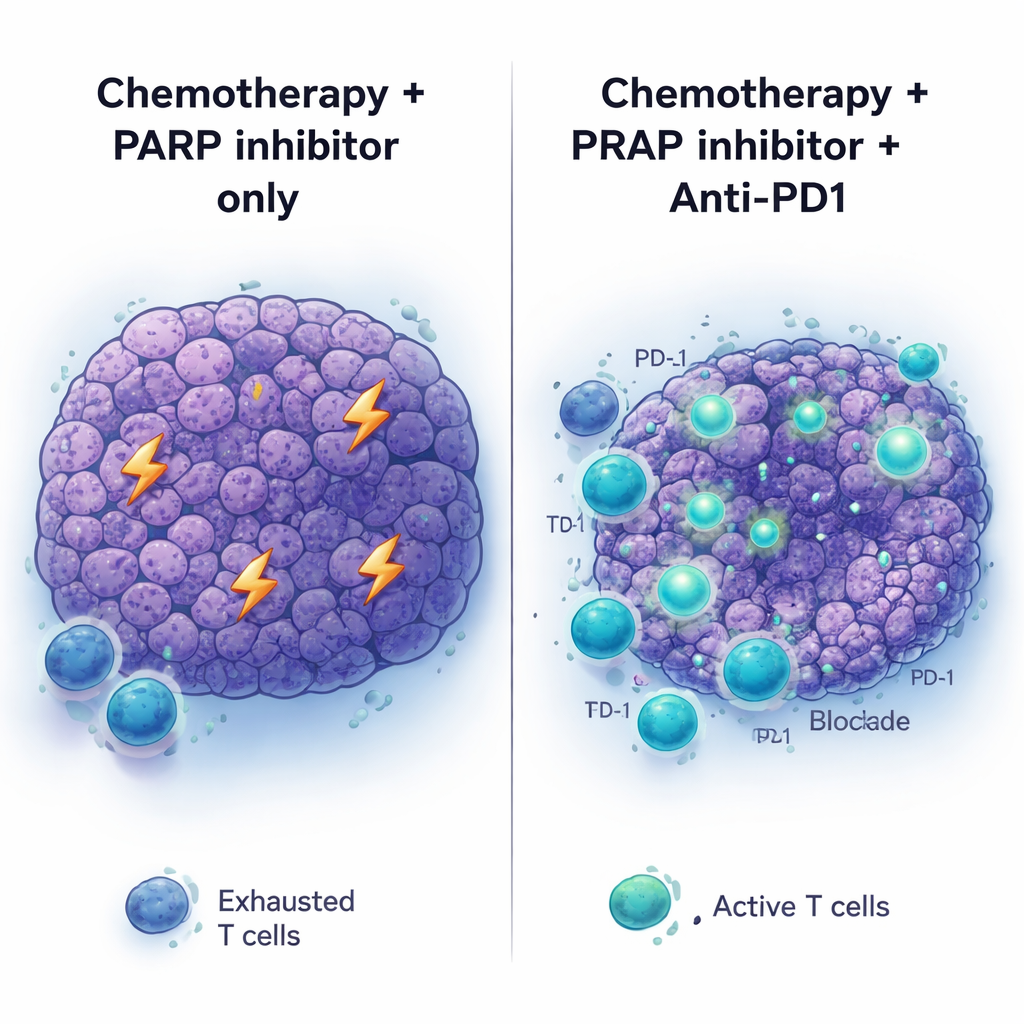
ما الذي قد يعنيه هذا للرعاية المستقبلية
تجتمع النتائج لتؤكد أن ترتيب وتركيب العلاجات لهما أثر كبير في سرطان البنكرياس المتحور في BRCA. لا يهاجم العلاج الكيميائي القوي المضر بالحمض النووي خلايا الورم مباشرة فحسب، بل يثير أيضاً استجابة مناعية، حتى لو كان ذلك الاستجابة مثبتة في البداية بالإرهاق ودفاعات PD-L1. يمكن لمثبطات PARP إطالة الفائدة لكنها على الأرجح لن تكون علاجاً شافياً بمفردها وقد تدفع الأورام نحو حالة مقاومة ذات مستويات عالية من CDX2. من خلال وضع علاج مضاد PD1 فوق صيانة PARP بعد العلاج بالبلاتين، قد يصبح من الممكن تحويل هذا المشهد المناعي الملتهب والمؤثَّل بالإنهاك إلى هجوم مضاد أقوى وأكثر ديمومة ضد الورم. ستكون التجارب السريرية الجارية التي تجمع مثبطات PARP مع العلاج المناعي في سرطان البنكرياس المرتبط بـBRCA محورية لمعرفة ما إذا كان يمكن لهذه الاستراتيجية الموقوتة بعناية أن تُترجم إلى حياة أطول وأفضل للمرضى.
الاستشهاد: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
الكلمات المفتاحية: سرطان البنكرياس, طفرة BRCA2, العلاج الكيميائي بالبلاتين, مثبط PARP, علاج المناعة PD-1