Clear Sky Science · ar
تخليق أميد فعال دون مذيبات عبر تفاعل ريتر محفَّز بمركب نانوي Fe3O4/g-C3N4/NTMPA قابل لإعادة الاستخدام
لماذا تهم الكيمياء الأنظف
الكثير من الأدوية التي نتناولها، والبلاستيك المحيط بنا، وحتى الألياف عالية الأداء مبنية على نوع بسيط من الروابط الكيميائية يُسمى رابطة الأميد. إعداد هذه الروابط على نطاق صناعي غالباً ما يتطلب أحماضاً قوية ومسببة للتآكل وكميات كبيرة من المذيبات، مما يولد نفايات ويطرح مشاكل أمان. يصف هذا المقال محفزًا صلبًا جديدًا يستجيب للمجال المغناطيسي ويمكنه تكوين الأميدات بعائد عالٍ دون استخدام أي مذيبات، مما يشير إلى مسار أكثر أمانًا واستدامة لصناعة الأدوية والمواد.
حلقة رئيسية في الأدوية والمواد
الأميدات هي الروابط التي تجمع البروتينات كما توجد في عدد لا يحصى من الأدوية ومبيدات المحاصيل والبوليمرات مثل النايلون. لدى الكيميائيين عدة طرق لبناء روابط الأميد، لكن معظم الطرق تتطلب مواد بداية مفعلة مسبقًا أو ظروف قاسية. يبرز تفاعل ريتر لأنه يربط كحولًا بسيطًا (أو ألكينًا) مع نيتريل مباشرة في خطوة واحدة. ومع ذلك، في شكله الكلاسيكي يعتمد تفاعل ريتر على أحماض معدنية مركزة مثل حمض الكبريتيك أو الهيدروكلوريك. هذه الأحماض السائلة مسببة للتآكل، وصعب فصلها عن المنتجات وإعادة تدويرها، مما يجعلها غير ملائمة للكيمياء الخضراء.
مغناطيس صغير يمكنك تحريكه بمحرّاك
صمّم الباحثون محفزًا صلبًا يمكن فصله مغناطيسيًا ليحل محل هذه الأحماض السائلة. يجمع مادتهم بين ثلاثة مكونات: نانوجسيمات أكسيد الحديد (Fe3O4) التي تمنح خواصًا مغناطيسية؛ مادة صلبة طبقية غنية بالكربون والنتروجين (نتريد الكربون الغرافيتي، g‑C3N4) تعمل كدعم واقٍ؛ وجزيء حمضي قوي يُسمى نيتريلوتري(ميثلفسفونيك أسيد) (NTMPA) الذي يوفر الحموضة اللازمة لدفع التفاعل. تُجمَع هذه الأجزاء بحيث يرتكز NTMPA على سطح g‑C3N4، بينما تُضمن جسيمات Fe3O4 الصغيرة في المِركب الكلي. ولأن المركب يستجيب للمغناطيس، يمكن استخراجه من مزيج التفاعل ببساطة بوضع مغناطيس خارج القارورة.
إثبات بنية المحفز
لتأكيد أنهم بنوا ما قصدوه، استخدم المؤلفون مجموعة من أدوات علم المواد. أظهرت أطياف الأشعة تحت الحمراء إشارات من مجموعات الفسفونك أسيد، وإطار الكربون–النتروجين، وروابط الحديد–الأكسجين، كلها موجودة معًا في المركب النهائي. أشارت حيود الأشعة السينية إلى أن أكسيد الحديد المغناطيسي حافظ على شكله البلوري، بينما بقي نتريد الكربون كمادة طبقية ذات ترتيب جزئي غير منتظم. كشفت المجهر الإلكتروني عن جسيمات شبيهة بالألواح مزينة بكرات متناثرة بالتساوي في نطاق 10–20 نانومتر، وأظهر التوزيع العنصري وجود الحديد والكربون والنيتروجين والأكسجين والفوسفور موزعة بشكل موحّد. أكدت قياسات مساحة السطح وحجم المسام وجود بنية مسامية وسطية—مليئة بقنوات على مقياس النانومتر تسمح للمتفاعلات بالوصول إلى المواقع النشطة—بينما أظهرت التحليلات الحرارية أن المادة تظل مستقرة حتى مئات الدرجات المئوية.
تفاعلات سريعة بدون مذيبات
مع إثبات البنية، اختبر الفريق المحفز في تفاعل ريتر بين كحولات ونيتريلات مختلفة. وجدوا أن أفضل الشروط كانت بسيطة بشكل مدهش: مقادير متساوية من الكحول والنيتريل، جرعة صغيرة من المحفز الصلب، تسخين إلى 80 °م، ودون إضافة مذيبات. تحت هذه الظروف، تحولت العديد من مواد البداية المختلفة إلى الأميدات المقابلة بعوائد عالية إلى ممتازة، غالبًا فوق 90%. تفاعلت الكحولات الثلاثية والبنزيلية (التي تشكل بالأساس الوسيط التفاعلي اللازم لتفاعل ريتر بسهولة أكبر) في غضون 1–4 ساعات فقط، بينما احتاجت الركائز الأكثر صعوبة إلى وقت أطول قليلاً. نجحت كل من النيتريلات العطرية والأليفاتية، مع أن المجموعات الشاردة للإلكترونات بقوة على النيتريلات العطرية حسّنت الكفاءة بشكل أكبر. بشكل عام، أظهرت الدراسة أن المحفز الصلب يمكن أن يضاهي أو يتفوق على الكثير من الأحماض السائلة، مع تجنب الوسط المسبّب للتآكل والمذيبات الإضافية.
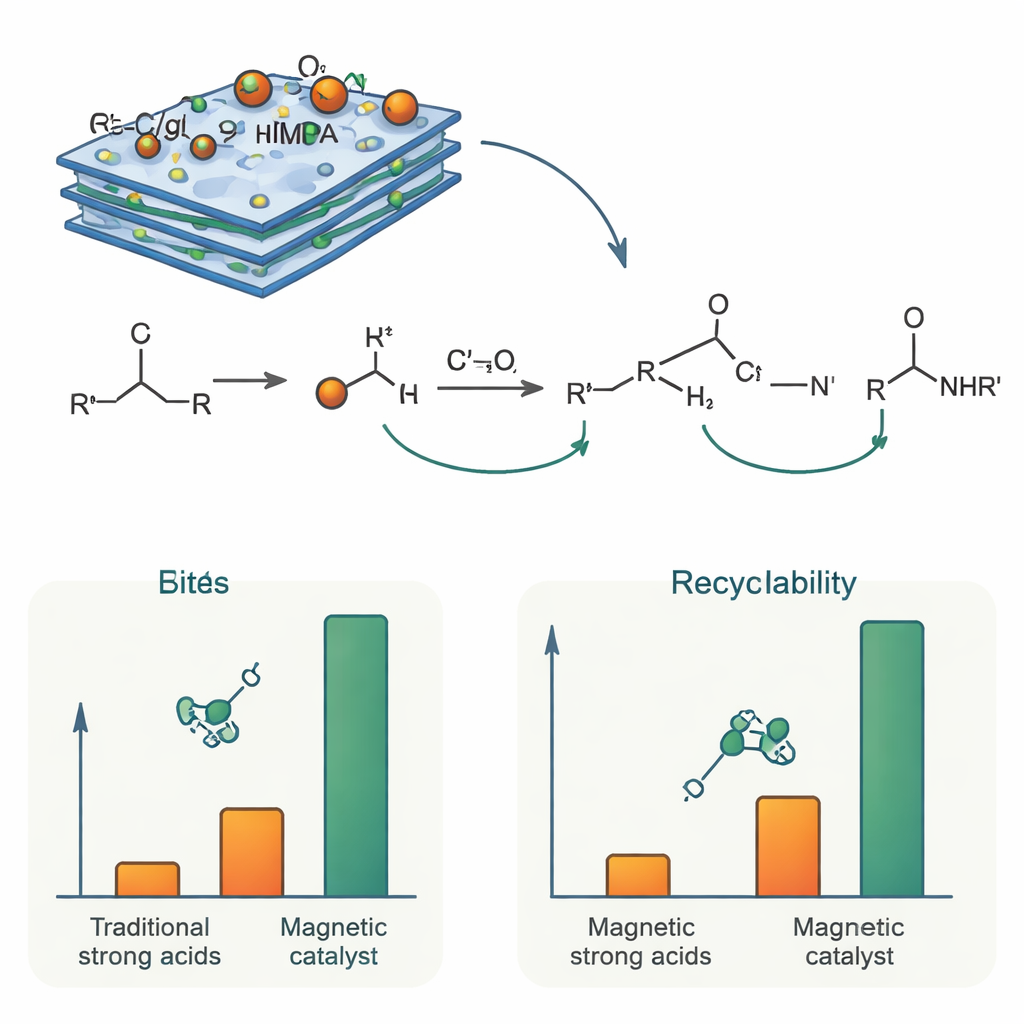
كيف يعمل ولماذا يدوم
كيميائيًا، دور المحفز هو إحداث بروتنة مؤقتة للكحول ومساعدته على فقدان الماء، مولّدًا نوعًا موجَبًا قصير العمر. يهاجم جزيء نيتريل هذا الوسيط لتكوين رابطة جديدة بين الكربون والنيتروجين، والتي تتحول لاحقًا إلى أميد بالتفاعل مع الماء المتكوّن أثناء العملية. توفر مجموعات الفسفونك أسيد في NTMPA حموضة متحكمًا بها، قوية بما يكفي لدفع هذه الخطوات ولكنها معتدلة بواسطة سطح نتريد الكربون المحيط بحيث تُقلّل التفاعلات الجانبية غير المرغوب فيها. وبما أن وحدات NTMPA النشطة مرفوقة كيميائيًا بالدعم الصلب، فإنها لا تُغسل خلال التفاعل. أكدت قياسات المغناطيسية أن الجسيمات تظل شديدة المغناطيسية، مما يسمح بإزالة المحفز المستهلك بسرعة باستخدام مغناطيس. في اختبارات إعادة الاستخدام، استُخدمت نفس دفعة المحفز ست مرات على الأقل مع انخفاض طفيف فقط في الفعالية، وأظهرت التحليلات بعد الاستخدام أن تركيبته ومورفولوجيته لم تتغير إلى حد كبير.
ماذا يعني هذا للتصنيع الأخضر
للقارئ غير المتخصص، الخلاصة الأساسية هي أن المؤلفين طوروا مسحوقًا قابلاً لإعادة الاستخدام يستجيب للمجال المغناطيسي ويمكن أن يساعد الكيميائيين في تجميع روابط أميد مهمة دون الاعتماد على الأحماض السائلة القاسية والمذيبات الإضافية المطلوبة عادةً. تقصُّ هذه المقاربة من النفايات، وتبسط تنقية المنتجات، وتسهل إعادة تدوير المحفز، وكلها أمور مهمة للكيمياء الصناعية الأكثر خضرة. وبينما تركز الدراسة على نوع واحد من التفاعلات، يمكن تطبيق مبادئ التصميم نفسها—تثبيت مجموعات حمضية قوية على دعم متين ومغناطيسي—على العديد من التحولات الأخرى التي تشكل أساس إنتاج الأدوية والمواد المتقدمة.
الاستشهاد: Karimitabar, H., Sardarian, A.R. Efficient solvent-free amide synthesis via Ritter reaction catalyzed by a reusable Fe3O4/g-C3N4/ NTMPA nanocomposite. Sci Rep 16, 6494 (2026). https://doi.org/10.1038/s41598-026-35371-2
الكلمات المفتاحية: تخليق الأميدات, تفاعل ريتر, محفز نانوي مغناطيسي, كيمياء بدون مذيبات, التحفيز الأخضر