Clear Sky Science · ar
اضطراب التوازن الداخلي للحديد بسبب خلل في الميتوكوندريا مرتبط بكبت تعبير ATP13A2
لماذا يهم الحديد داخل خلايا الدماغ
يشتهر مرض باركنسون بالرجفات وحركات الانقباض، لكن داخل الخلايا الدماغية المصابة تدور دراما أخرى: الحديد، وهو معدن ضروري، يبدأ بالتراكم في أماكن لا ينبغي أن يكون فيها. تطرح هذه الدراسة سؤالاً بسيطاً لكنه مهمّاً: كيف يحدث هذا التراكم، وكيف قد يضر بالمحطات الصغيرة للطاقة ومراكز إعادة التدوير داخل الخلايا العصبية؟ بالإجابة على ذلك، تقدم الدراسة دلائل تبيّن لماذا تتدهور مناطق دماغية معينة في باركنسون واضطرابات ذات صلة، وتشير إلى أنواع جديدة من العلاجات تتجاوز مجرد استبدال الدوبامين.
نظرة أقرب على دليل جيني نادر
يركز الباحثون على شكل وراثي نادر من مرض باركنسون يُسمى PARK9، الناجم عن خلل في جين يُدعى ATP13A2. يصنع هذا الجين بروتيناً موجوداً في الجسيمات الحالّة، وهي مقصورات الخلية لمعالجة النفايات وإعادة التدوير. يمكن للأشخاص الذين يحملون طفرات في ATP13A2 أن يعانوا أيضاً من حالة تتسم بترسبات حديدية في الدماغ. هذا الارتباط جعل من ATP13A2 نقطة دخول مثالية لدراسة كيف يختل توازن الحديد. باستخدام خط خلايا شبيه بالخلايا العصبية البشرية يفرط في إنتاج بروتين باركنسون ألفا‑سينوكلين، استخدم الفريق شظايا صغيرة من الحمض النووي الريبي لكتم التعبير عن ATP13A2 ثم تتبع كيف تغيّر الحديد وإنتاج الطاقة وصحة الخلية.
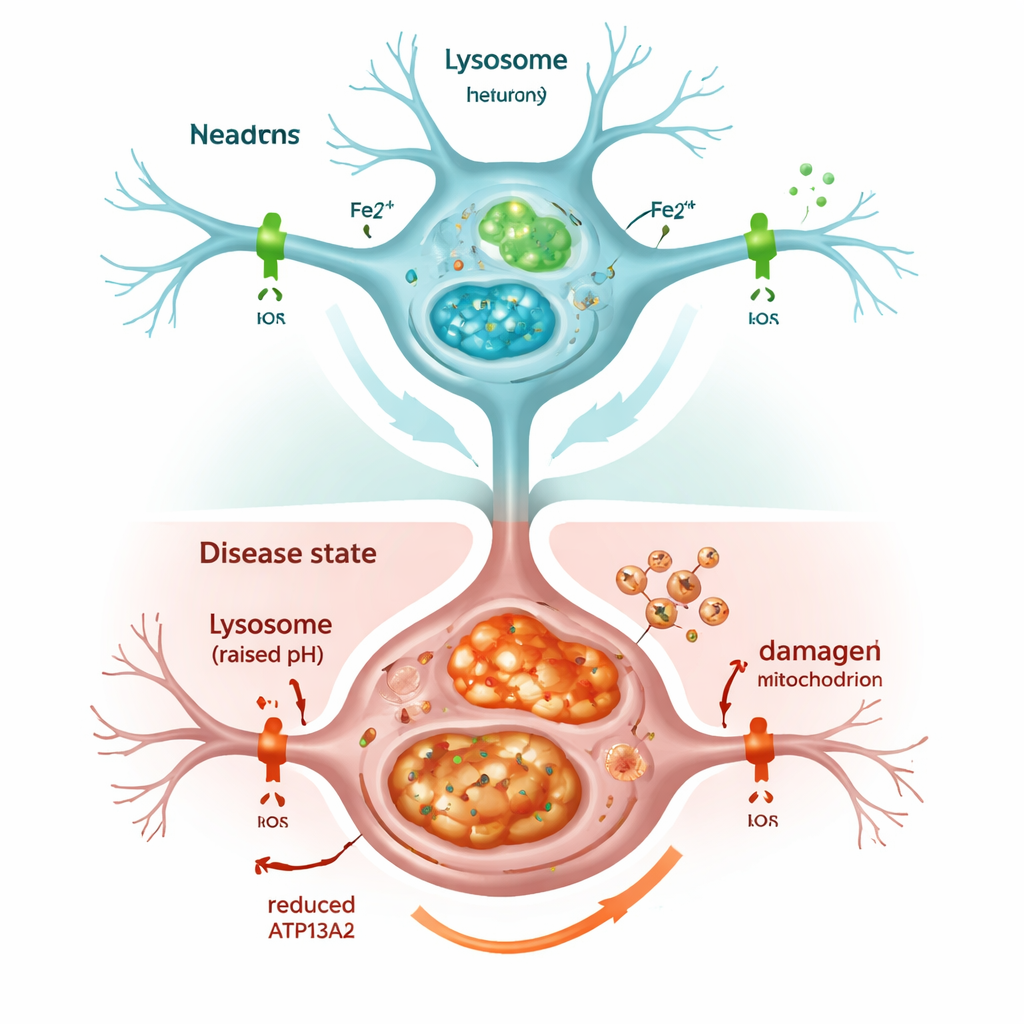
عندما يتعطل نظام إعادة التدوير الخلوي
أدى إيقاف ATP13A2 بسرعة إلى إضعاف الجسيمات الحالّة. انخفضت حموضتها الداخلية، وهي خاصية حاسمة لتحطيم المواد غير المرغوبة، وتراكمت مؤشرات عملية التنظيف الخلوية المعروفة بالالتهام الذاتي بدلاً من أن تُزال. نتيجة لذلك، تراكمت ألفا‑سينوكلين، في تكرار لما يُرى في أدمغة المصابين بباركنسون. كما أظهرت الخلايا زيادة عامة في الحديد، وخصوصاً في الشكل الكيميائي الفعّال المسمى Fe2+ داخل كل من الجسيمات الحالّة والميتوكوندريا. استجابت الخلية بصنع المزيد من الفيرّيتين، البروتين المخزن للحديد، لكن ذلك لم يكن كافياً لمنع المشكلات: أنتجت الميتوكوندريا المثقلة جزيئات تفاعلية للأكسجين بشكل زائد، وتراجع بقاء الخلايا. إن معالجة الخلايا بعقار رابط للحديد، مشابه لبعض الأدوية المستخدمة سريرياً، خفّض هذا الإجهاد التأكسدي وأنقذ صلاحية الخلايا جزئياً، مما يؤكد أن فائض الحديد نفسه كان دافعاً رئيسياً للضرر.
حساسات الحديد تتوقف عن الاستجابة للمعدن
طبيعياً، تمتلك الخلايا نظام تغذية راجعة يلاحظ ارتفاع مستويات الحديد ويستجيب بخفض استيراد الحديد. يُحسّ بروتين يُدعى IRP2 الحديد جزئياً عبر إشارة تعتمد على الهيم قادمة من الميتوكوندريا، ثم يضبط إنتاج بروتينات حمل الحديد على سطح الخلية. في الخلايا التي تفتقر إلى ATP13A2، فشل هذا الحاجز الوقائي. ظلّت الناقلات التي تجلب الحديد إلى الخلية عند مستويات مرتفعة رغم أن الحديد كان مرتفعاً بالفعل. لم تتغير مستويات بروتين IRP2 تقريباً، ولم يؤدِ إضافة حديد خارجي إلى تحفيز تكسّره الطبيعي. عاقب الفريق هذا الفشل إلى الميتوكوندريا: كانت الميتوكوندريا التالفة تتنفس بكفاءة أقل، وأبدت دلائل خلل في مراقبة الجودة (الالتهام الذاتي للميتوكوندريا)، والأهم أنها فقدت القدرة على تصنيع الهيم، الجزيء الحاوي على الحديد الذي يساعد IRP2 على استشعار الحديد. من دون ما يكفي من الهيم، لم يتلقّ IRP2 رسالة «الكثير من الحديد» وسمح باستمرار تدفّق الحديد إلى الداخل.
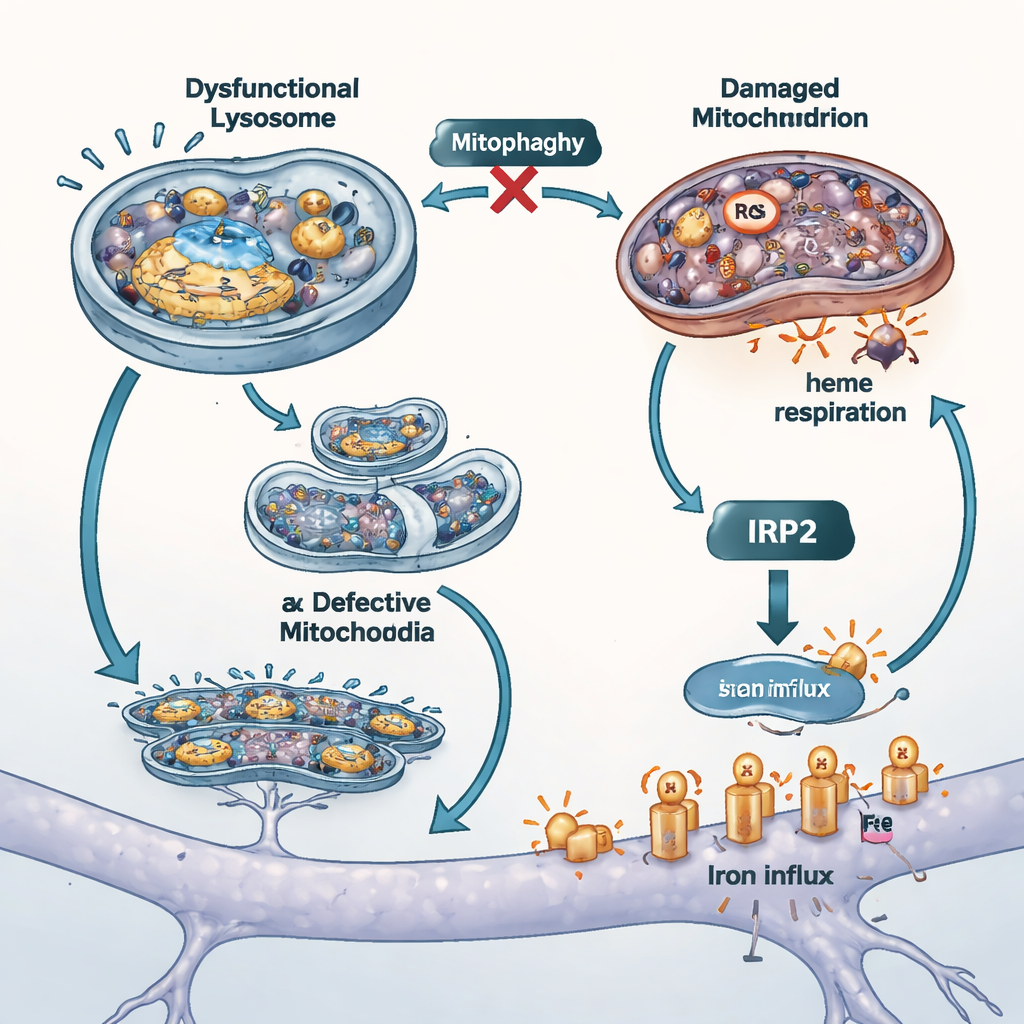
إغلاق صنبور الحديد وتجربة نماذج أخرى
لفحص مدى مساهمة دخول الحديد الخارجي غير المنضبط في إصابة الخلايا، قام العلماء بسد مسارين رئيسيين لامتصاص الحديد. استخدموا نسخة خالية من الحديد من بروتين الدم ترانسفيرين للمنافسة على أحد الناقلات، وعقاراً صغيراً لكبح نشاط ناقل آخر يُدعى DMT1. خفّضت كلتا المناورتين إجمالي الحديد والحديد الحر داخل الخلايا، وقللتا الإجهاد التأكسدي في الميتوكوندريا، وحسّنتا البقاء، ما يوحي بأن قنوات الحديد السطحية تُعد مضخمات هامة للضرر عند فقدان ATP13A2. كرر الباحثون أيضاً تجارب رئيسية في خلايا تفتقد جينًا آخر مرتبطًا بباركنسون، PINK1، المعروف بتسببه في ضعف الالتهام الذاتي للميتوكوندريا. أظهرت تلك الخلايا نفس مزيج تراكم الحديد وضعف إنتاج الهيم، مما يدعم الفكرة بأن مراقبة جودة الميتوكوندريا وتوازن الحديد مترابطان بإحكام في أشكال مختلفة من المرض.
ماذا يعني هذا لباركنسون والعلاجات المستقبلية
ببساطة، توضح الدراسة حلقة مفرغة خطيرة. عندما يُكبت ATP13A2، تفشل الجسيمات الحالّة في إزالة المكونات التالفة، بما في ذلك الميتوكوندريا الخاطئة. تنتج هذه الميتوكوندريا الضعيفة طاقة وهيم أقل، مما يعطل نظام استشعار الحديد في الخلية. يستمر تدفّق الحديد عبر الناقلات السطحية، ويتجمع في مقصورات عرضة للخطر، ويشعل تفاعلات سامة تزيح المزيد من الميتوكوندريا عن العمل. مع مرور الوقت، قد يساعد هذا المسار في تفسير سبب موت خلايا عصبية معينة في باركنسون واضطرابات الدماغ المصحوبة بتحميل الحديد. وتشير النتائج إلى أن العلاجات المستقبلية قد لا تقتصر على إزالة الحديد الفائض فحسب، بل قد تسعى أيضاً إلى استعادة وظيفة الجسيمات الحالّة، ومراقبة جودة الميتوكوندريا، وإنتاج الهيم—مهاجمة المشكلة من مصدرها بدلاً من مجرد تنظيف المعدن بعد وقوع الضرر.
الاستشهاد: Murakami, T., Ohuchi, K., Kiuchi, M. et al. Disruption of intracellular iron homeostasis through mitochondrial dysfunction associated with suppression of ATP 13A2 expression. Sci Rep 16, 5007 (2026). https://doi.org/10.1038/s41598-026-35368-x
الكلمات المفتاحية: مرض باركنسون, حديد الدماغ, الميتوكوندريا, الجسيمات الحالّة, تخليق الهيم