Clear Sky Science · ar
التحقيق في بقايا النقاط الساخنة الوظيفية لإنزيم عبر المراقبة اللحظية للتفاعل الإنزيمي باستخدام الرنين المغناطيسي والحسابات
لماذا هذا مهم لمضادات الفيروسات المستقبلية
فيفابيراڤير هو قرص يُستخدم بالفعل ضد الإنفلونزا وتم اختباره لفيروس كوفيد-19، لكنه لا يهاجم الفيروسات بالشكل الذي نبتلعه مباشرة. يجب على خلايانا أولاً تحويله إلى جزيء نشط يعيق الفيروس. تفكك هذه الدراسة، تقريبًا ذرّة بذرة، كيف يقوم إنزيم بشري واحد بخطوة تنشيط حاسمة، وأي الأجزاء الصغيرة في الإنزيم تعمل كنقاط «ساخنة» تتحكم في سرعة ودرجة تفعيل الدواء. فهم هذه التفاصيل قد يوجّه تصميم جيل جديد من مضادات الفيروسات تكون أقوى وأكثر قابلية للتنبؤ بنتائجها في المرضى.
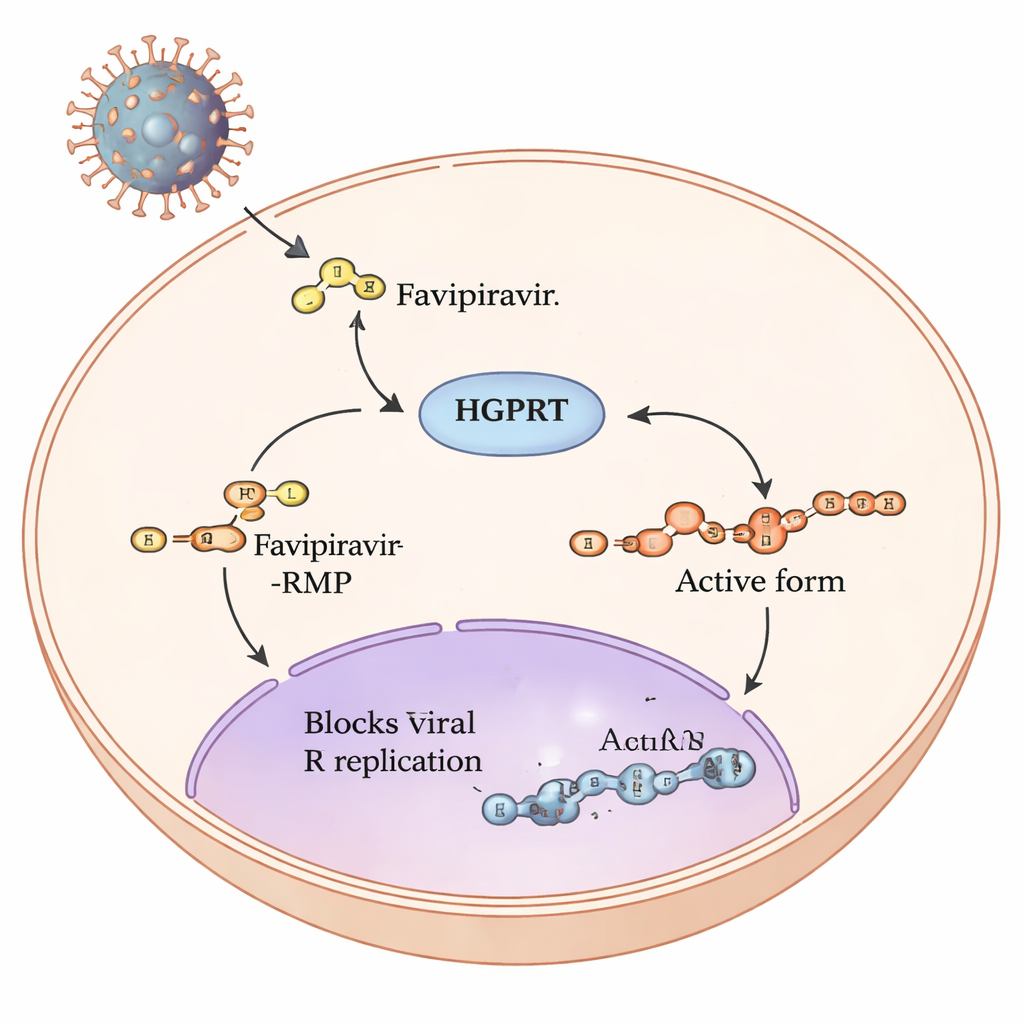
رحلة البروفَـرِق داخل خلايانا
فيفابيراڤير هو ما يُسمى بروفارِق: بعد دخوله إلى الخلايا البشرية، سلسلة من الخطوات الكيميائية تعيد تشكيله إلى شكل يمكنه تعطيل آلية نسخ الفيروسات ذات الحمض النووي الريبي مثل الإنفلونزا وSARS‑CoV‑2. الخطوة الأولى والأبطأ في هذا المسار يقوم بها إنزيم بشري يُدعى هيبوكساثين‑جوانين فوسفوريبوزيل ترانسفيراز (HGPRT). يضيف HGPRT مجموعة سكر‑فوسفات صغيرة إلى فيفابيراڤير، منتِجًا فيفابيراڤير‑RMP. فقط بعد هذه الخطوة يمكن لإنزيمات أخرى بناء الشكل الثلاثي الفوسفات النشط بالكامل الذي يتداخل مباشرة مع بوليميراز الحمض النووي الريبي الفيروسي. وبما أن هذه الخطوة الأولى التي يقودها HGPRT تعمل كاختناق على كمية الدواء النشط المتكوّن، فقد سعى المؤلفون لتحديد أي أجزاء من HGPRT هي الأكثر أهمية في معالجة فيفابيراڤير.
مراقبة الكيمياء في الزمن الحقيقي بالرنين المغناطيسي
يمتاز فيفابيراڤير باحتوائه على ذرة فلور تعمل كناقل راديوي صغير في مجال مغناطيسي. استغل الفريق ذلك باستخدام مطيافية الرنين المغناطيسي للفلور‑19 لمتابعة، في الزمن الحقيقي، كمية فيفابيراڤير وكمية فيفابيراڤير‑RMP الموجودة في أنبوب اختبار مع تقدم التفاعل. وبما أن الدواء وحده يحمل الفلور، فإن إشارات الرنين المغناطيسي واضحة وسهلة التتبع. من خلال تسجيل الأطياف بشكل متكرر خلال 12 ساعة، تمكن الباحثون من متابعة اختفاء المركب الابتدائي وظهور المنتج المعدّل، ثم استخراج مقاييس حركية قياسية مثل سرعة تقدم التفاعل ومدى إحكام ارتباط الإنزيم بالدواء.
ضبط مواقع رئيسية في الإنزيم
أشارت لقطات سابقة بالأشعة السينية لـ HGPRT المرتبط بـ فيفابيراڤير‑RMP إلى حفنة من الأحماض الأمينية التي تحتضن الدواء في جيب. تختبر الدراسة الجديدة ثلاثة من هذه المواقع عبر إجراء تغييرات دقيقة بحرف واحد في البروتين ومقارنة كل إنزيم طافِرة مع الطبيعي. أحد التغييرات، الذي سُمّي T138A، جعل الإنزيم مفاجئًا أسرع بنحو أربعة إلى ستة أضعاف في تحويل فيفابيراڤير، رغم أنه أزال مجموعة كيميائية كان يُعتقد أنها تساعد في تثبيت الدواء. التغيير الثاني، K140M، أبطأ التفاعل بشكل طفيف وضعف الارتباط الظاهري قليلًا. أما التغيير الثالث، D193N، فأفقد الإنزيم تمامًا قدرته على إنتاج فيفابيراڤير‑RMP، رغم أن البروتين المعدّل كان لا يزال يُنتج ويستطيع ربط المنتج. معًا، تُظهر هذه النتائج أن ليست كل نقاط الاتصال متساوية: فبعضها يعمل كمنظم دقيق للسرعة، بينما البعض الآخر يشكل مفاتيح جوهرية.
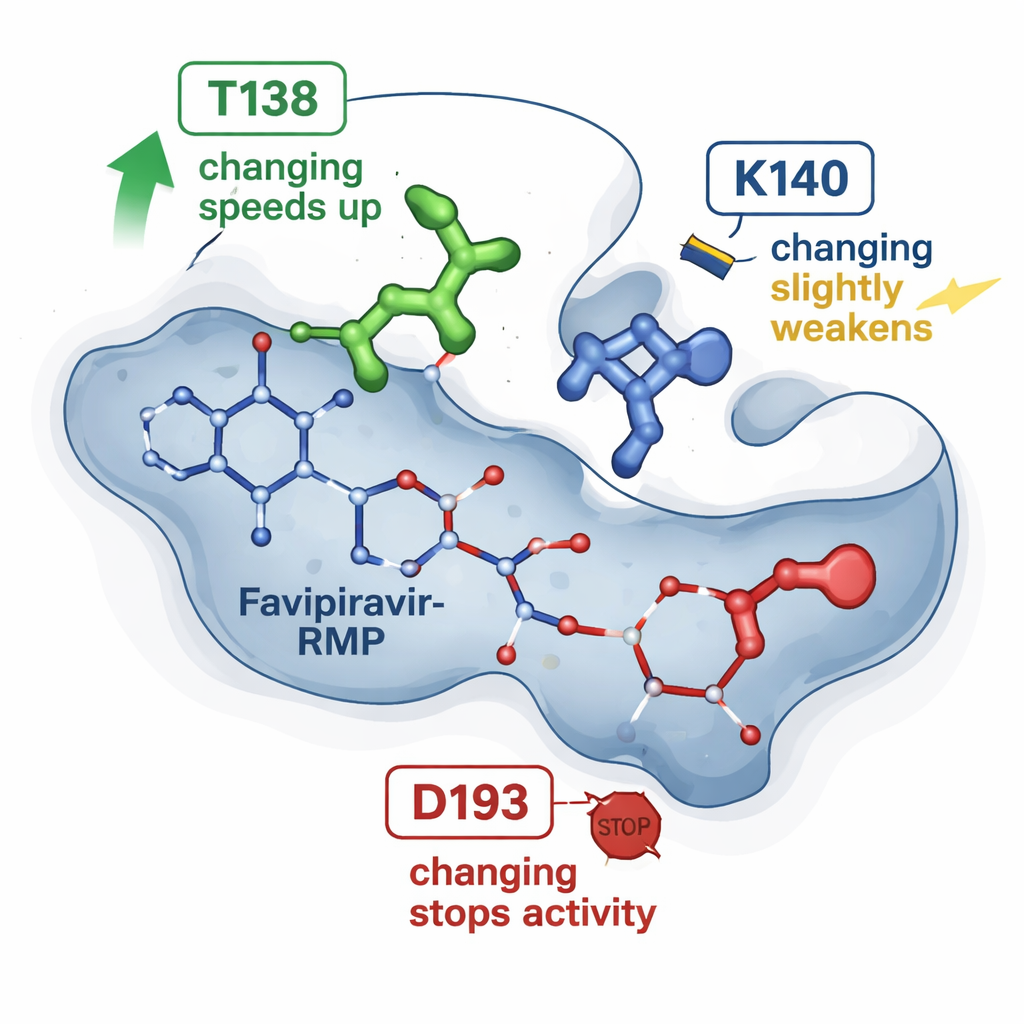
محاكاة الأجزاء المتحركة على الحاسوب
للنظر إلى ما وراء البُنى الساكنة، لجأ الباحثون إلى المحاكاة الجزيئية. انطلقوا من البنية ثلاثية الأبعاد المعروفة لـ HGPRT مع فيفابيراڤير‑RMP، واستخدموا أدوات حسابية راسخة لتقدير مدى قوة ارتباط الدواء في كل طافر ولإجراء العديد من محاكاة الديناميكا الجزيئية القصيرة. تتبع هذه المحاكاة كيف تهتز الذرات وتتفاعل خلال عشرات النانوثوانٍ. اتفقت الحسابات مع التوجهات المستمدة من الرنين المغناطيسي: فقد بدا أن متغير T138A يميل إلى احتفاظ أفضل بـ فيفابيراڤير‑RMP، لكنه أظهر أيضًا حلقات زمنية ينتقل فيها الدواء نحو مسار «هروب»، موجهًا بواسطة بقايا أخرى (K140) تثبت مجموعة الفوسفات مؤقتًا قبل التحرر. بالمقابل، ظل متغير D193N يمسك بالمنتج، لكنه فشل على الأرجح في خطوة تحفيزية مبكرة تتطلب أيون المغنيسيوم، مما يفسر خسارته للنشاط رغم الارتباط المستقر.
خريطة طريق لتصميم مضادات فيروسية أكثر ذكاءً
من خلال الجمع بين قياسات الرنين المغناطيسي اللحظية ونماذج حاسوبية مفصّلة، تخريطة هذه الدراسة النقاط الساخنة الوظيفية في HGPRT التي تتحكم في كفاءة تفعيل فيفابيراڤير. وبصيغة مبسطة لغير المتخصصين، الخلاصة أن إنزيماتنا الذاتية يمكن أن تؤثر بشكل كبير على مقدار الدواء المضاد للفيروسات النشط المتجمع داخل الخلايا، وأن تعديل شكل الدواء أو جيب الإنزيم يمكن أن يغيّر هذه النتيجة بشكل كبير. تقدم الاستراتيجية الهجينة للمؤلفين مخططًا عامًا لفحص كيفية تفاعل أدوية أخرى مع بروتيناتها المستهدفة، مما قد يسرّع تطوير مركبات مضادة للفيروسات جديدة متوائمة بشكل أفضل مع آليات تنشيط الجسم.
الاستشهاد: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
الكلمات المفتاحية: فيفابيراڤير, تنشيط مضاد للفيروسات, إنزيم HGPRT, مطيافية الرنين المغناطيسي, تصميم الأدوية