Clear Sky Science · ar
أنماط مدركة مكانياً للبيانات المناعية الفلورية متعددة العلامات
لماذا يهم جيران خلايا الورم
يعد سرطان البنكرياس من أكثر السرطانات فتكًا، ويرجع ذلك جزئياً إلى أن أورامه تعيش داخل «حي» معقد من الخلايا المناعية والخلايا الداعمة التي يمكن أن تقاتل السرطان أو تساعده على الاختباء. تقدم هذه الدراسة طريقة جديدة لقراءة التخطيط المكاني لتلك الخلايا في صور المجهر، كاشفةً كيف يتصرف الجهاز المناعي بشكل مختلف في ساركوما غدية قناة البنكرياس العدوانية (PDAC) مقارنةً بـالورم الغدي المخاطي الحليمي داخل القناة ما قبل السرطاني (IPMN). قد تشير معرفة هذه الأنماط الخفية إلى تشخيصات أفضل وعلاجات أكثر ذكاءً واستهدافًا.
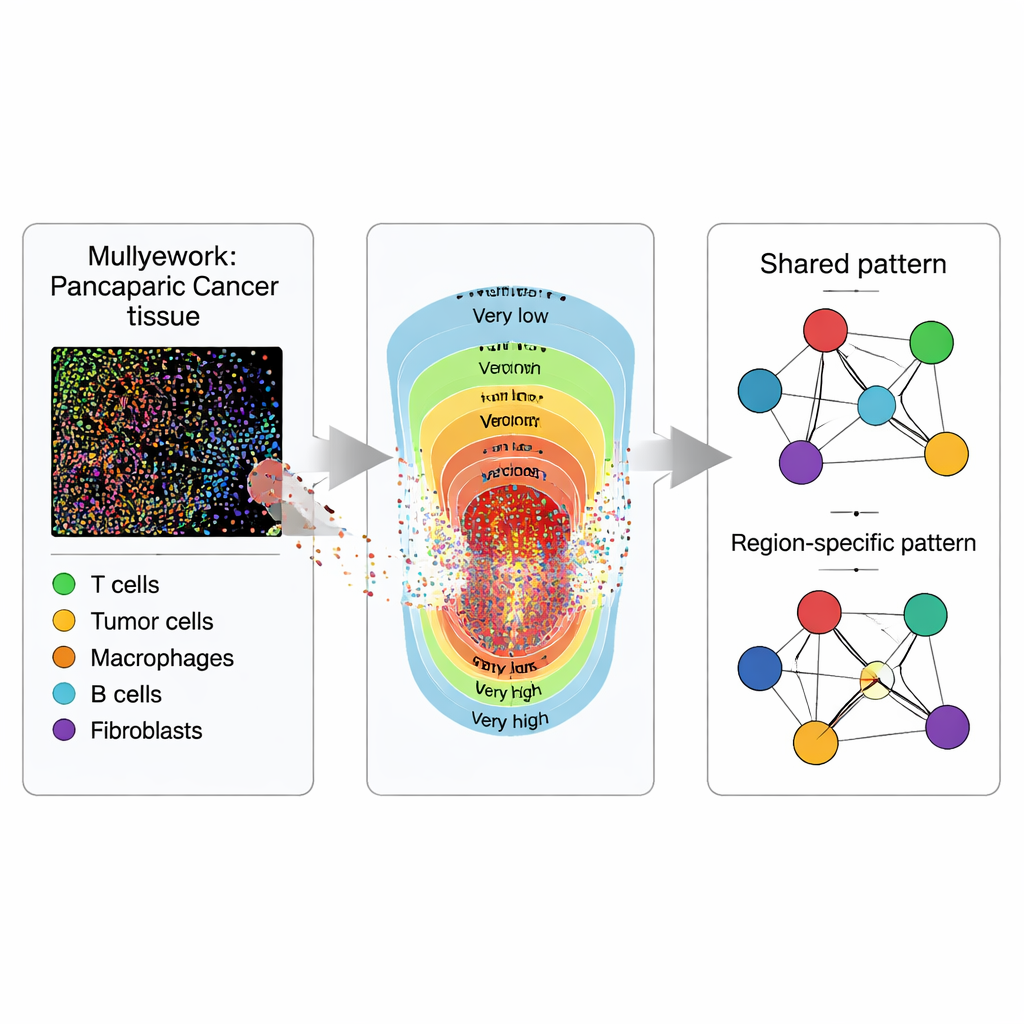
رؤية الأنسجة كخرائط لا مجرد صور
بدلاً من التعامل مع شريحة الورم كصورة مسطحة، يعاملها الباحثون كخريطة ممتلئة بنقاط. باستخدام التصوير المناعي الفلوري متعدد العلامات، يصبغون عينات الأنسجة من 119 مريضًا مصابًا بـPDAC و53 مريضًا مصابًا بـIPMN بحيث تتوهج أنواع الخلايا المختلفة بألوان مميزة. يحول برنامج متخصص كل خلية مرئية إلى نقطة ذات إحداثيات وتسيمة: خلايا الورم (باطنية)، عدة أنواع من خلايا T التي يمكن أن تهاجم أو تنظم الاستجابات المناعية، وخلايا عرض المستضد التي تعرض أجزاءً من الورم لخلايا T. السؤال الرئيسي ليس فقط كم عدد كل نوع من الخلايا، بل أين تقع بالنسبة إلى بعضها البعض عبر النسيج.
تقسيم الورم إلى مناطق
لالتقاط كيفية تغير الأورام من المركز إلى الخارج، تُقسَّم كل عينة نسيجية إلى خمس مناطق بناءً على مدى كثافة خلايا الورم، من «منخفضة جدًا» إلى «مرتفعة جدًا» في شدة الورم. تمثل هذه المناطق تدرجًا في عبء الورم وتكدس الخلايا الذي يراه أخصائيو الأمراض تحت المجهر لكن قلما يقومون بقياسه. ضمن كل منطقة، يقدر الفريق "خرائط شدة" مُملَّسة لكل نوع خلية، محولين النقاط المتناثرة إلى خرائط حرارية مستمرة لمواقع تجمع كل نوع من الخلايا. تسمح لهم هذه التقسيمات بمقارنة ليس فقط كيفية تفاعل الخلايا بشكل عام، بل كيف تتغير تلك التفاعلات من مناطق الورم المتناثرة إلى الكثيفة.
تحويل جيران الخلايا إلى شبكات
بعد ذلك، يترجم الباحثون الأنماط المكانية إلى شبكات، حيث يمثل كل نوع خلية عقدة وتمثل الروابط مدى ميل نوعين من الخلايا للظهور معًا بعد احتساب تأثير جميع الأنواع الأخرى. باستخدام إطار إحصائي بيزي يسمونه ISPat (أنماط مدركة مكانياً ومطلعة)، يفصلون الميزات المشتركة عبر جميع المناطق عن تلك الخاصة بكل منطقة. يمكن لـISPat أيضًا إدخال معرفة بيولوجية سابقة عند توفرها، مما يساعد على استقرار التقديرات في بيانات معقدة. تظهر تجارب المحاكاة أن ISPat قادر على استرجاع الأنماط المعروفة بشكل موثوق ويفعل ذلك أسرع بكثير من الأساليب التقليدية، مما يجعله عمليًا للدراسات التصويرية الكبيرة.
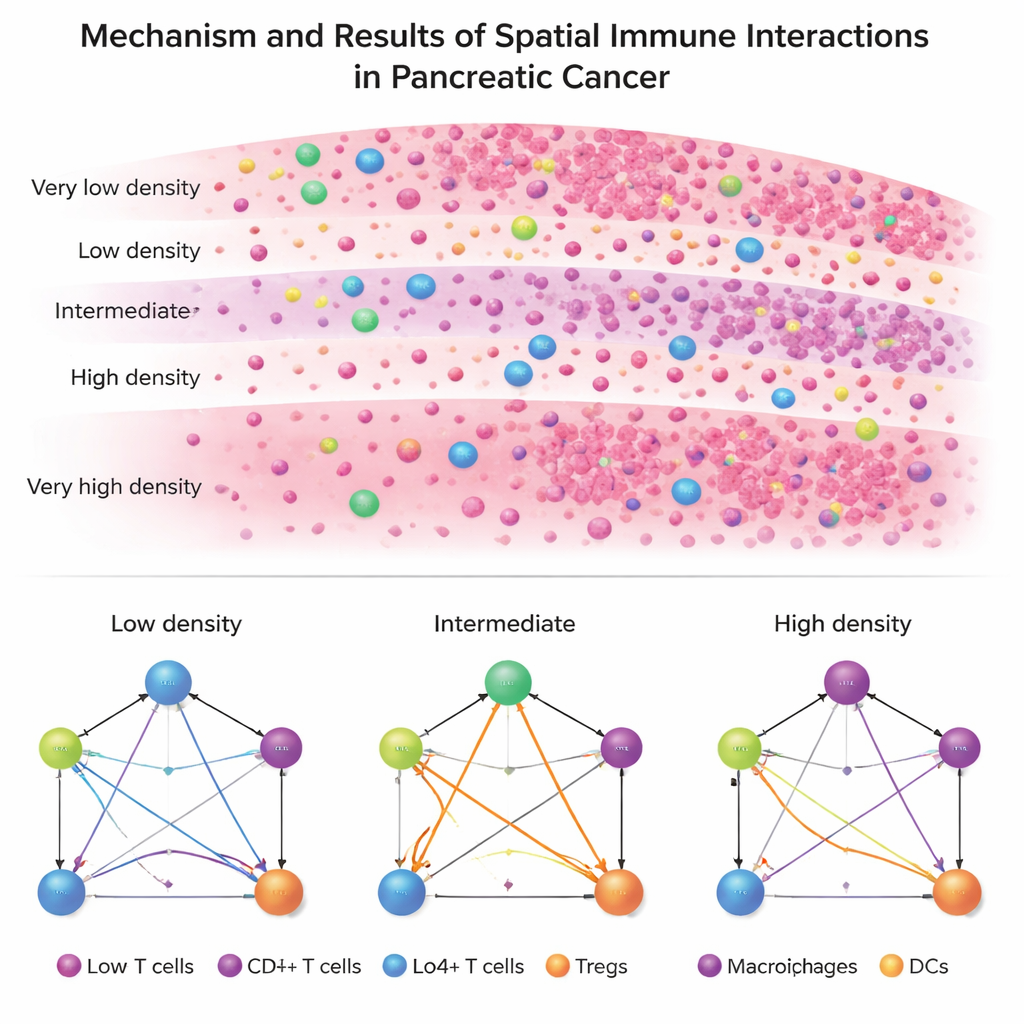
مرضان، بنيتان مناعيتان مختلفتان
عند تطبيق ISPat على بيانات المرضى الحقيقية، يظهر تباين لافت بين PDAC وIPMN. يعرض PDAC بنية مناعية جامدة وموحدة: عبر معظم المناطق تقريبًا، تحافظ خلايا الورم وخلايا T المساعدة وخلايا T القاتلة (السامة) وخلايا T التنظيمية وخلايا عرض المستضد على نمط علاقات متشابه تقريبًا. يشير هذا إلى بيئة مثبطة مناعيًا مستقرة ومتجذرة يصعب تفكيكها. بالمقابل، يظهر IPMN تباينًا أكبر بكثير من منطقة إلى أخرى، خاصة في كيفية تواصل الخلايا T التنظيمية مع الخلايا المناعية الأخرى. في IPMN، تظهر المناطق ذات الكثافة المتوسطة — ليست مكتظة تمامًا بخلايا الورم ولا خالية تقريبًا منه — أكبر إعادة تشكيل دراماتيكية للتفاعلات المناعية.
نقاط ساخنة للتهرب المناعي والعلاج
بالتعمق أكثر، تحدد الدراسة أزواجًا محددة من أنواع الخلايا التي تختلف تفاعلاتها باستمرار بين PDAC وIPMN، لا سيما في تلك المناطق ذات الكثافة المتوسطة. العديد منها ينطوي على الخلايا T التنظيمية التي يمكن أن تخفض الهجمات المناعية، وخلايا عرض المستضد وخلايا T القاتلة التي تشن وتنفذ الاستجابات المضادة للورم. من الجدير بالذكر أن التفاعلات التي تدفع عرض المستضد والقتل المباشر للورم، وكذلك تلك التي تعزز القمع المناعي، تختلف بأوضح شكل في هذه المناطق المتوسطة التدرج، لا في أقصى مناطق الورم. يشير هذا النمط إلى أن ساحة المعركة الحاسمة للتحكم المناعي تقع في المناطق الانتقالية حيث لا يزال الورم والجهاز المناعي يتفاوضان بنشاط.
ماذا يعني هذا للمرضى
لغير المتخصص، الخلاصة هي أن موضع الخلايا داخل الورم يهم بقدر أهمية نوع الخلايا نفسها. يبدو أن PDAC يغلق ترتيبًا مناعيًا قمعيًا ومستقرًا، بينما تظل الخريطة المناعية لـIPMN أكثر مرونة وتعتمد على المنطقة. قد تصبح هذه البصمات المكانية مؤشرات حيوية لتمييز الأورام الخطيرة عن الآفات قبل السرطانية وللتنبؤ أي المرضى قد يستفيدون من علاجات مناعية معينة. يوفر إطار ISPat أداة عامة لقراءة هذه الرموز المكانية في أمراض عديدة، داعمًا لمستقبل يُوجَّه فيه علاج السرطان ليس فقط بواسطة الجينات وأنواع الخلايا، بل بواسطة جغرافيا الخلايا الدقيقة داخل ورم كل مريض.
الاستشهاد: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
الكلمات المفتاحية: سرطان البنكرياس, البيئة الدقيقة للورم, التصوير المكاني, التفاعلات المناعية, الأورام الدقيقة الموجهة