Clear Sky Science · ar
نظام وسم REC الخالٍ من اللايسين لتطبيقات الوسم القريب بالبيوتين
لماذا تهم الوسوم الصغيرة على البروتينات
داخل كل خلية، نادراً ما تعمل البروتينات بمفردها—فهي تتعاون في شراكات متغيرة تدفع العمليات الصحية والمرَضية. لدراسة هذه الشراكات، غالباً ما يلصق العلماء "بطاقات تعريف" صغيرة بالبروتينات حتى يمكن تتبعها أو سحبها من خليط أو رؤيتها تحت الميكروسكوب. تُعد طريقة شائعة تُسمى الوسم القريب بالبيوتين وسيلة لرسم خريطة من يقف بالقرب من من داخل الخلية، لكنها تحمل مشكلة مخفية: العديد من هذه البطاقات تتعرض لتعديلات كيميائية وتختفي فعلياً عندما تكون هناك حاجة إليها أكثر. تقدم هذه الدراسة نوعاً جديداً من الوسوم، أُطلق عليه وسم REC، مصمَّم ليظل مرئياً تحت هذه الظروف القاسية.
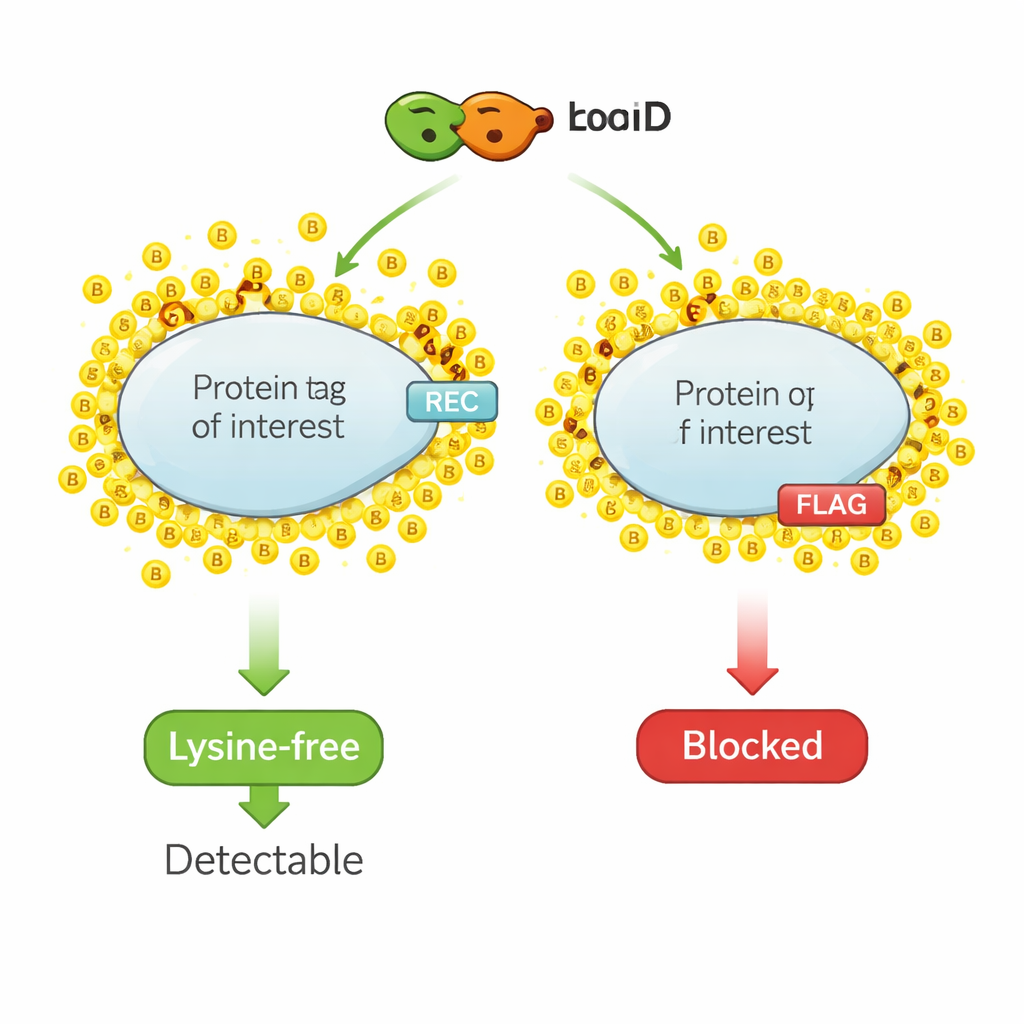
مرمِّز كيميائي لجيران البروتين
يعمل الوسم القريب بالبيوتين مثل قلم تمييز جزيئي. يُدمَج إنزيم معدل، مثل TurboID، مع بروتين محل الاهتمام. عند إضافة البيوتين—فيتامين صغير—يلصق TurboID بسرعة جزيئات البيوتين بالبروتينات القريبة. بعد ذلك يصطاد الباحثون جميع البروتينات الموسومة بالبيوتين ويحدّدونها، مما يعطي لمحة عن الحي البروتيني المحلي. غير أن نفس الكيمياء التي تساهم في وسم البروتينات القريبة تستهدف أيضاً وسوم الإبيتوبي الصغيرة المستخدمة عادة للاكتشاف، لأن هذه الوسوم تحتوي غالباً على اللايسين، وهو حمض أميني يُعد الموقع الرئيسي لارتباط البيوتين. عندما تُغطّى اللايسينات في الوسم بالبيوتين، لا تعود الأجسام المضادة قادرة على التعرف على الوسم، فيتضاءل الإشارة في طرق الكشف التقليدية أو تختفي.
تصميم وسم يرفض التعديل
لحل هذه المشكلة، شرع المؤلفون في إنشاء وسم جديد خالٍ تماماً من اللايسين. بدأوا من مقطع من بروتين طفيلي للملاريا يُدعى PfRipr5، والذي يتمتع بقليل من التشابه مع بروتينات الإنسان، مما يقلل من خطر التفاعلات العرضية. باستخدام طريقة فرز معتمدة على شريحة ميكروية في الأرانب، أنشأوا 22 جسمًا مضادًا أحادي النسيلة ضد PfRipr5 وحددوا واحدًا، سُمِّي النسخة رقم 6، ذا ارتباط قوي ومحدد بشكل خاص. من خلال تقليم وتحوير مقطع PfRipr5 بشكل منهجي، ضيقوا هدف الجسم المضاد إلى تتابع مكوَّن من 11 حمضًا أمينيًا. احتوى هذا التتابع المصغر على لايسين واحد فقط، استبدلوه بحمض أميني مشابه، الأرجينين. وبشكل ملحوظ، ظلّ الجسم المضاد مرتبطًا بكفاءة مماثلة. أُطلق على هذا التتابع المحسّن الخالي من اللايسين اسم وسم REC، وعلى الجسم المضاد المطابق اسم مضاد REC.
اختبار وسم REC في الميدان
اختبر الفريق بعد ذلك ما إذا كان وسم REC قادرًا على أن يحل محل الوسوم المستخدمة على نطاق واسع مثل FLAG في تقنيات المختبر الشائعة. عندما وُصِل بالبوتينات المضيئة أو بروتينات الإشارة وأُنتج في أنظمة خالية من الخلايا وخلايا ثدييات، كانت البروتينات الموسومة بـ REC تُكتشف بسهولة بواسطة التصحيح المناعي (immunoblotting)، واختبار صفائحي حساس ضوئياً يُدعى AlphaScreen، والتلوين المناعي داخل الخلايا. كانت قوة الكشف مشابهة لقوة وسم FLAG ولنظام وسم آخر خالٍ من اللايسين (AGIA)، وأظهر مضاد REC ضوضاء خلفية قليلة جدًا عبر مجموعة متنوعة من خطوط خلايا البشر والقرود. والأهم أن الوسم عمل سواء وُضِع في بداية البروتين أو نهايته، وعلى بروتينات موجودة في مناطق خلوية متنوعة، بما في ذلك النواة والميتوكندريا والشبكة الإندوبلازمية وغشاء الخلية.
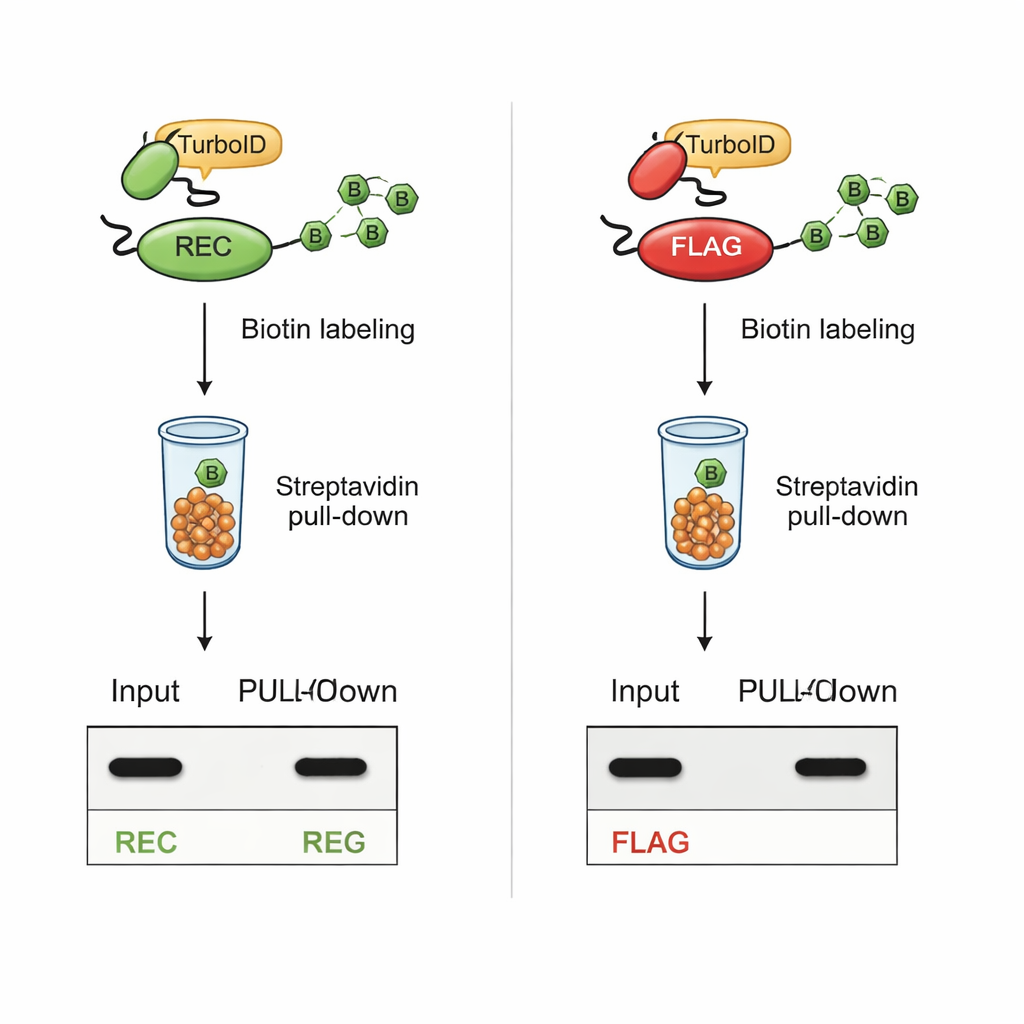
البقاء مرئياً أثناء الوسم المكثف
الاختبار الحاسم كان ما إذا كان REC سيبقى قابلاً للاكتشاف بعد وسم بيوتينيل سريع بواسطة TurboID. في خلايا حيث وُصِل TurboID بشركاء تفاعل معروفين، ظلت البروتينات الحاملة لوسم REC مرئية بوضوح في كل من مستخلصات الخلايا الكلية والجزء المنقّى والموسوم بالبيوتين. بالمقابل، فقدت البروتينات الحاملة لوسم FLAG إشارة FLAG بمجرد تنشيط TurboID، رغم أن البروتينات نفسها كانت لا تزال موجودة. أظهرت تجارب إضافية باستخدام ببتيدات تركيبية أن TurboID يبيوتين مباشرة اللايسينات في تسلسل FLAG، مما يمنع فعليًا وصول الأجسام المضادة. وسم REC، لخلوه تمامًا من اللايسين، بقي غير متأثر بواسطة TurboID وظل سهل الاكتشاف.
ماذا يعني هذا للتجارب المستقبلية
للباحثين الذين يستكشفون شبكات البروتين داخل الخلايا الحية، يقدم وسم REC أداة عملية جديدة: يتصرف مثل الوسوم المألوفة في الاختبارات اليومية ولكنه يستمر في العمل حتى عند نشاط إنزيمات الوسم القريبة القوية. هذا يعني أن العلماء يمكنهم التأكد بمزيد من الموثوقية من وجود بروتيناتهم الموسومة وإمساكها بشكل صحيح، ويمكنهم دراسة تعديلات أخرى معتمدة على اللايسين—مثل التأبيُت (ubiquitination) والأسيتلة—دون تداخل الوسم نفسه. باختصار، REC هو تغيير تصميمي صغير ذو تأثير كبير، يساعد على جعل تجارب رسم خرائط البروتينات المعقدة أكثر وضوحًا ومصداقية.
الاستشهاد: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
الكلمات المفتاحية: وسم البروتين, الوسم القريب بالبيوتين, TurboID, تفاعلات البروتين, وسوم إبِتُوب