Clear Sky Science · ar
تفاعل مثيلة DNA لجين ELMO1 مع Med31 يعزز التحول البطاني الظهاري والنتوء المعوي الناجم عن H. pylori عبر استقطاب M2
لماذا تهم بكتيريا المعدة في خطر الإصابة بالسرطان
يحمل معظمنا مليارات البكتيريا في جهازنا الهضمي، وإحداها — هيليكوباكتر بيلوري — يمكن أن تعيش بهدوء في المعدة لعقود. بالنسبة بعض الأشخاص تكون هذه العدوى غير ضارة، أما بالنسبة للآخرين فتصبح الخطوة الأولى نحو سرطان المعدة، أحد أخطر أنواع السرطان في العالم. تستقصي هذه الدراسة كيف أن تغييرًا كيميائيًا دقيقًا في الحمض النووي لخلايا المعدة يساعد على تحويل عدوى طويلة الأمد إلى تلف سابق للسرطان وفي النهاية إلى بيئة مواتية لنمو السرطان.
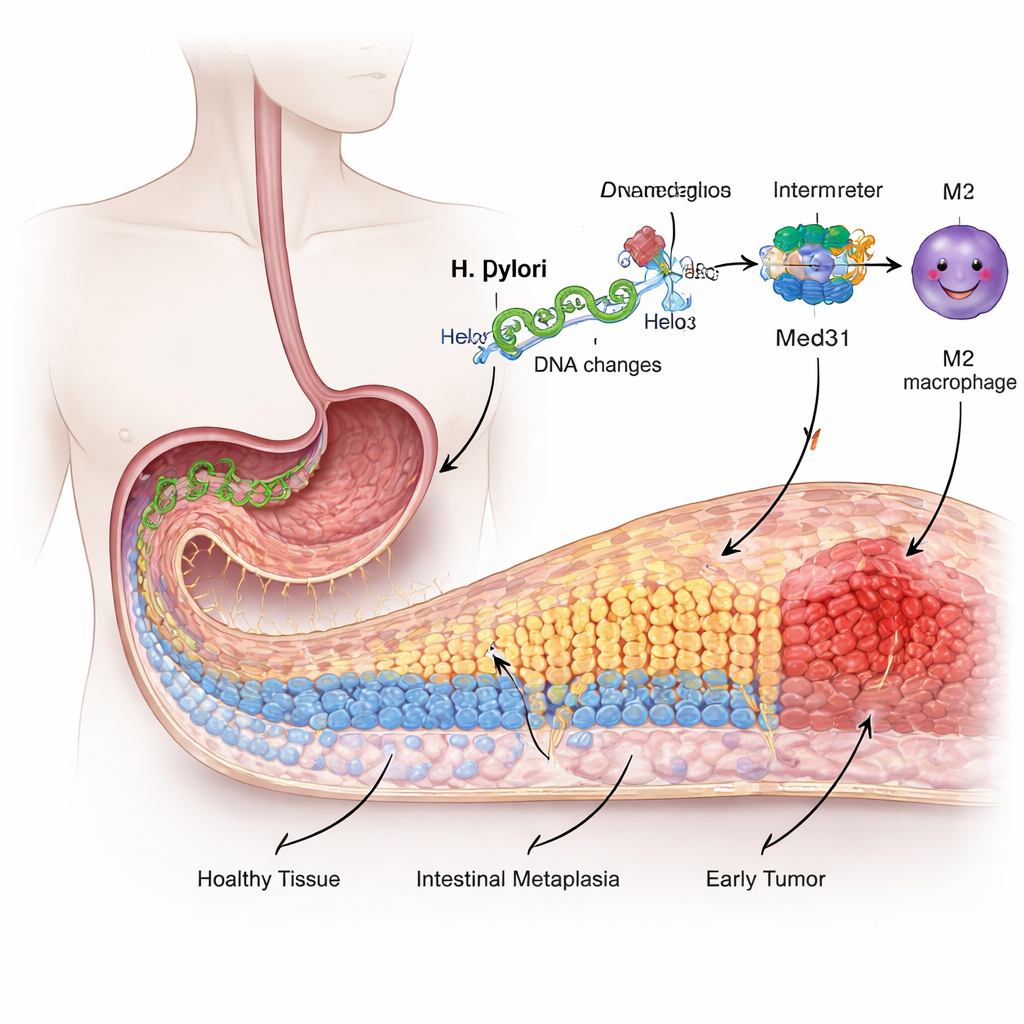
من بطانة ودية إلى تحول محفوف بالمخاطر
السطح الداخلي للمعدة مبطن بخلايا متخصصة مهيأة لتحمل الحمض القوي، وليس لهضم الطعام مثل الأمعاء. على مدى سنوات من التهيج والالتهاب الناتج عن H. pylori، تبدأ بعض هذه الخلايا المعدية في «إعادة تزيين» نفسها، متخذةً خصائص خلايا معوية في عملية تُسمى التحول المعوي. يُعتبر هذا التغير مرحلة سابقة للسرطان. استخدم الباحثون سلالة خلوية بشرية معدية لمحاكاة العدوى ووجدوا أن التعرض لـ H. pylori جعل هذه الخلايا تنمو أسرع، وتتحرك بسهولة أكبر، وتفعّل علامات من نوع الأمعاء — كلها علامات على أن البطانة تُغير هويتها الطبيعية.
وسوم كيميائية صغيرة بعواقب كبيرة
يمكن وسم حمضنا النووي بمجموعات كيميائية صغيرة تُسمى مجموعات الميثيل تعمل كمفاتيح تشغيل/إيقاف للجينات دون تغيير الشفرة الوراثية نفسها. ركز الفريق على جين يُدعى ELMO1، المعروف بالفعل بدوره في حركة الخلايا وانتشار السرطان. أظهروا أن عدوى H. pylori زادت من مثيلة جين ELMO1 وبشكل مفاجئ إلى حد ما عزّزت نشاطه ومستويات بروتينه في الخلايا المعدية. عندما استخدموا دواءً يزيح هذه الوسوم الميثيلية، فقدت الخلايا العديد من التغيرات الناجمة عن العدوى: انخفضت معدلات انقسامها، وتراجعت حركتها، وظهرت إشارات أقل للتحول المعوي. تشير هذه النتائج إلى أن مثيلة ELMO1 تشكّل مفتاحًا حاسمًا تقلبه البكتيريا.
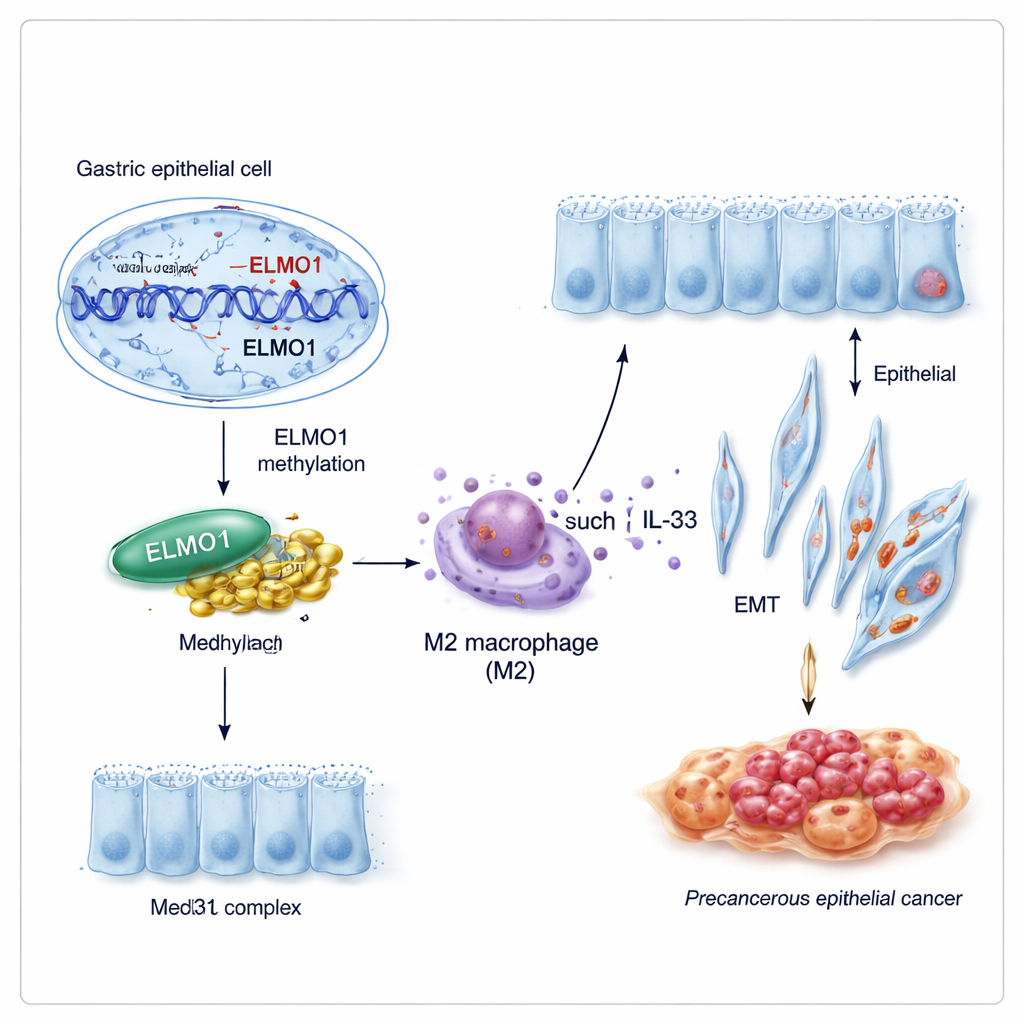
شراكة جديدة تعيد برمجة سلوك الخلايا
نادراً ما تعمل الجينات بمفردها. اكتشف الباحثون أن ELMO1 الميثّل يفضّل الدخول في شراكة مع بروتين آخر، Med31، وهو جزء من «لوحة تحكم» كبيرة تساعد في تقرير أي الجينات تُشغّل الخلية. في ظروف تفضّل مثيلة الحمض النووي، ارتفعت مستويات ELMO1 وزاد Med31، وربطا بعضهما فعليًا، بينما تم إقصاء شريك أقدم معروف لـ ELMO1 وهو DOCK10. يبدو أن فريق ELMO1–Med31 الجديد يغير برنامج التعبير الجيني في خلايا المعدة بطرق تشجعها على اكتساب ملامح معوية والتصرّف بقدر أكبر من العدوانية.
كيف تُدفع الخلايا المناعية إلى مساعدة الورم
لا يتطور السرطان بمعزل؛ بل ينمو داخل حي معقد من الخلايا المناعية والخلايا المساندة. تُظهر الدراسة أن الخلايا المعدية المصابة ذات ELMO1 الميثّل تطلق مستويات أعلى من IL‑33، وهو إشارة تدفع الخلايا المناعية المجاورة المسماة البلاعم (الماكروفاجات) إلى حالة «M2» المناسبة للورم. باستخدام نظام تعايش خلوي، وجد المؤلفون أن البلاعم المعرضة لهذه الإشارات انحازت بشكل قوي نحو النوع M2 وبدورها أفرزت عوامل دفعت خلايا معدية جديدة لتصبح أكثر حركة وغزوًا وأكثر شبهاً بالخلايا المعوية. ارتفعت مؤشرات الانتقال البطاني الظهاري إلى اللحمي — عندما تتحول الخلايا الطلائية الثابتة إلى خلايا متجولة قادرة على الغزو — بشكل حاد تحت تأثير هذه البلاعم من النوع M2.
ماذا يعني هذا لمنع سرطان المعدة
تجمع النتائج مجتمعة سلسلة أحداث: تغير عدوى H. pylori مثيلة الحمض النووي لجين ELMO1، يتعاون ELMO1 المعدّل مع Med31، ترسل الخلايا المصابة إشارات تحوّل الخلايا المناعية المجاورة إلى مساعدين من النمط M2، وهؤلاء المساعدون يدفعون بدورهم كلًا من التحول المعوي والحالة الخلوية الأكثر غزوًا. للفهم العام، الفكرة الأساسية أن بكتيريا معدية شائعة يمكنها إعادة تشكيل كل من بطانة المعدة والاستجابة المناعية المحلية عبر وسوم كيميائية قابلة للعكس على الحمض النووي. قد يفتح فهم هذا المسار أبوابًا لاختبارات دموية جديدة تكشف أنماط مثيلة معرّضة للخطر مبكرًا، وكذلك لأدوية تقطع محور ELMO1–Med31–M2 قبل أن تتطور العدوى المزمنة إلى سرطان المعدة.
الاستشهاد: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
الكلمات المفتاحية: سرطان المعدة, هيليكوباكتر بيلوري, مثيلة الحمض النووي, التحول المعوي, البيئة الدقيقة للورم