Clear Sky Science · ar
تقييم الأساس الكيميائي الحيوي الكامن وراء المقاومة ضد الأميلويدوز الجهازي
عندما تمنع تغييرات صغيرة في البروتين تراكمًا قاتلاً
يمكن للعديد من الأمراض الالتهابية المزمنة، من التهاب المفاصل الروماتويدي إلى السل، أن تحفّز مضاعفة نادرة لكنها غالبًا ما تكون مميتة تُسمى الأميلويدوز الجهازي من نوع AA. في هذه الحالة، يتراكم بروتين دموي طبيعي على شكل ألياف صلبة تسد الأعضاء. تطرح هذه الدراسة سؤالًا مفاجئًا ومتفائلًا: هل يمكن أن تجعل تغييرات طبيعية صغيرة في ذلك البروتين بعض الحيوانات مقاومة إلى حد كبير للمرض—وإذا كان الأمر كذلك، كيف يحدث ذلك؟
التهديد الخفي لتراكمات البروتين
تبدأ الأميلويدوز من نوع AA بإشارة إنذار التهابية في الدم تُسمى أميلويد المصل A (SAA). أثناء الالتهاب الشديد أو المطوّل، يمكن أن ترتفع مستويات SAA بمقدار آلاف المرات فوق المعدل الطبيعي. في بعض البشر والحيوانات، يطوى جزء من هذا البروتين بشكل خاطئ ويتكدس في ألياف طويلة، تُعرف بالألياف الأميلويدية، التي تنتشر خلال أعضاء مثل الطحال والكليتين. مع مرور الوقت تضعف هذه الألياف وظائف الأعضاء. ومع ذلك، ليس كل فرد لديه مستويات عالية من SAA يصاب بالأميلويدوز، وبعض سلالات الفئران تظل مقاومة بشكل مدهش حتى عند دفعها نحو المرض في المختبر. قد يشير فهم السبب إلى استراتيجيات جديدة لمنع تراكم الأميلويد في البشر.
فئران مقاومة ونسخها البروتينية الخاصة
في الفئران، تنشأ معظم ألياف الأميلويد AA من نسخة واحدة من SAA تُسمى SAA1.1، المرتبطة ارتباطًا قويًا بالمرض. مع ذلك، بعض سلالات الفأر تنتج أساسًا نسخًا متغيرة قليلًا، أُسميت SAA1.5 وSAA2.2، وهذه السلالات نادرًا ما تطور الأميلويدوز الجهازي من نوع AA. تختلف البروتينات ببضع وحدات بناء فقط (أحماض أمينية)، ومع ذلك تتجمع هذه الاختلافات في منطقة مضغوطة تشكل القلب الداخلي للألياف المسببة للمرض. اقترح الباحثون أن هذه الاختلافات الصغيرة لا تمنع البروتينات من التكتل تمامًا، بل تمنعها من اعتماد الشكل الليفي المحدد جدًا الذي يكون ضارًا.
اختبار البروتينات في المختبر
لمعالجة هذه الفكرة، صنع الفريق جميع المتغيرات الثلاثة من SAA للفأر في بكتيريا وراقب كيف تصرفت في تجارب أنابيب الاختبار. رصدوا تشكيل الألياف باستخدام صبغة فلورية تضيء عند تكوّن الأميلويد، وتحققوا من البنى بواسطة مجاهر إلكترونية. شكلت نسخة SAA1.1 المرتبطة بالمرض أليافًا طويلة ومستقيمة بسهولة. كما أن SAA2.2 كان قادرًا أيضًا على تشكيل ألياف، لكنها كانت أكثر سمكًا وأكثر التواءً ومتنوعة من الناحية التركيبية، ولم تولّد نفس إشارة الصبغة القوية. بالمقابل، فشلت SAA1.5 في تشكيل ألياف تحت الظروف المختبرة. عندما أضاف العلماء عينات صغيرة من ألياف مرضية حقيقية مأخوذة من طحال فئران مريضة بوصفها «بذور»، نمت SAA1.1 بسرعة أليافًا جديدة نسخت بنية الأصل عن كثب، تمامًا مثل بريون. اللافت أن SAA1.5 وSAA2.2 لم يلتصقا بتلك البذور على الإطلاق؛ فلم تستطع الألياف المأخوذة من خارج الجسم استقطابهما إلى الشكل الممرض.
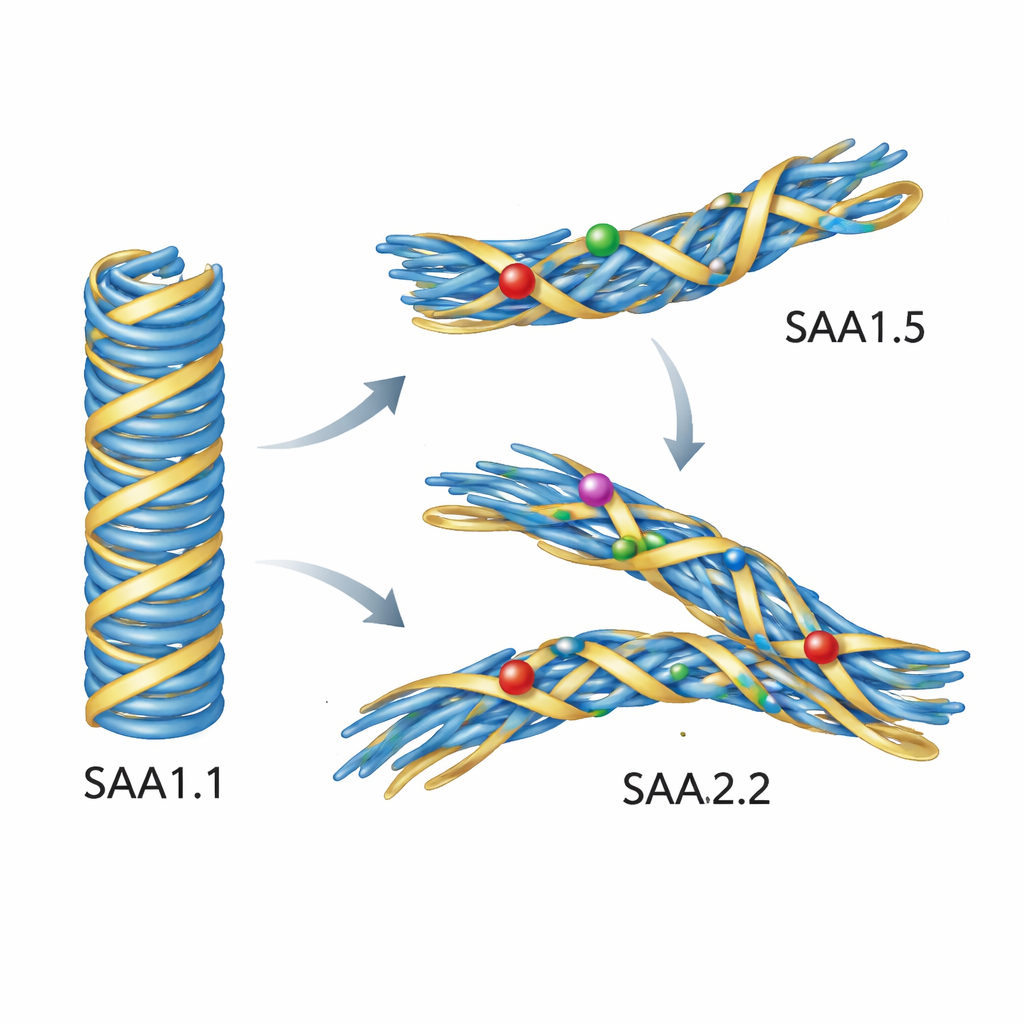
المحاكاة تبيّن لماذا ترفض البروتينات الطفرة الشكل الضار
لم تستطع التجارب وحدها إظهار بالضبط ما الذي يخطئ على المستوى الذري، لذا لجأ المؤلفون إلى محاكاة حاسوبية مفصّلة. بدأوا من بنية عالية الدقة لألياف AA الممرضة في الفأر المبنية من SAA1.1، ثم استبدلوا حسابيًا سلاسل SAA1.5 وSAA2.2. عندما حاكوا هذه الألياف في الماء عند حرارة الجسم، بقي نموذج SAA1.1 مستقرًا بشكل ملحوظ. بالمقابل، تحركت وتشوّهت الألياف المبنية من SAA1.5 أو SAA2.2. انتقلت حلقة رئيسية في القلب إلى الخارج وارتخى تماسها مع الجزء البادئ من البروتين، وانقلبت عدة سلاسل جانبية إلى أوضاع جديدة. هذه الترتيبات الطفيفة عطّلت التعبئة الضيقة التي تحدد الطيّ المرتبط بالمرض. بعبارة أخرى، لم تكن التسلسلات المتغيرة مشكلة في تكوين الألياف عمومًا—بل لم تكن قادرة على ملاءمة المخطط البنيوي للنموذج الأميلويدي الممرض بشكل مريح.
كيف تلهم هندسة الطبيعة علاجات مستقبلية
تُظهر النتائج مجتمعة أن السلالات الفأرية «المقاومة للأميلويد» ليست محمية لأن بروتين SAA الخاص بها لا يستطيع التجمّع إطلاقًا. بل إن نسخ SAA لديها غير متوافقة بنيويًا مع شكل الألياف الواحد المحدد الذي يسبب الأميلويدوز الجهازي من نوع AA. لا تزال هذه البروتينات قادرة على التكتل، لكنها تفعل ذلك بأشكال بديلة تبدو حميدة. تُعرف طفرات حماية مماثلة في أمراض أخرى ناجمة عن طي البروتين الخاطئ، بما في ذلك بعض حالات البروين والزهايمر. وهذا يشير إلى مبدأ أوسع: تعديل بروتين عرضة للمرض بحيث لا يستطيع تبني معماره السام—مع إبقائه يعمل بشكل طبيعي—قد يكون كافيًا لمنع المرض. على المدى الطويل، قد تساعد علاجات مستوحاة من هذه النسخ «المقاومة» الطبيعية، أو من شظايا قصيرة مشتقة منها، في توجيه البروتينات بعيدًا عن الطيات الضارة ونحو طيات غير ضارة.
الاستشهاد: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
الكلمات المفتاحية: الدمام الأميلويدية نوع AA, أميلويد المصل A, طي البروتين الخاطئ, مقاومة الأميلويد, نماذج الفأر