Clear Sky Science · ar
نمذجة والتحقق التجريبي لرواسب جسيمات نانوية من بوليكابرولاكتون
لماذا تهم الكرات البلاستيكية الصغيرة في الطب
تخيل تعبئة دواء قوي داخل جسيم بحجم ذرة يستطيع التسلل عبر الأوعية الدموية وإطلاق حمولته بالضبط حيث تُحتاج. تُعد هذه الجسيمات، المسماة بالجسيمات النانوية البوليمرية، محور العديد من العلاجات وأدوات التصوير الناشئة. لكن تحضيرها بالحجم الصحيح وبشكل قابل للتكرار أصعب مما يتوقع المرء. تُظهر هذه الدراسة كيف يمكن لنموذج حاسوبي بسيط قائم على الفيزياء أن يتنبأ بحجم جزيء قابل للتحكم لجسيم نانوي قابل للتحلل على نحو واسع الاستخدام، ما قد يقلص سنوات من التجريب والخطأ في تطوير أدوية نانوية جديدة.
من خلط المطبخ إلى دقة المختبر
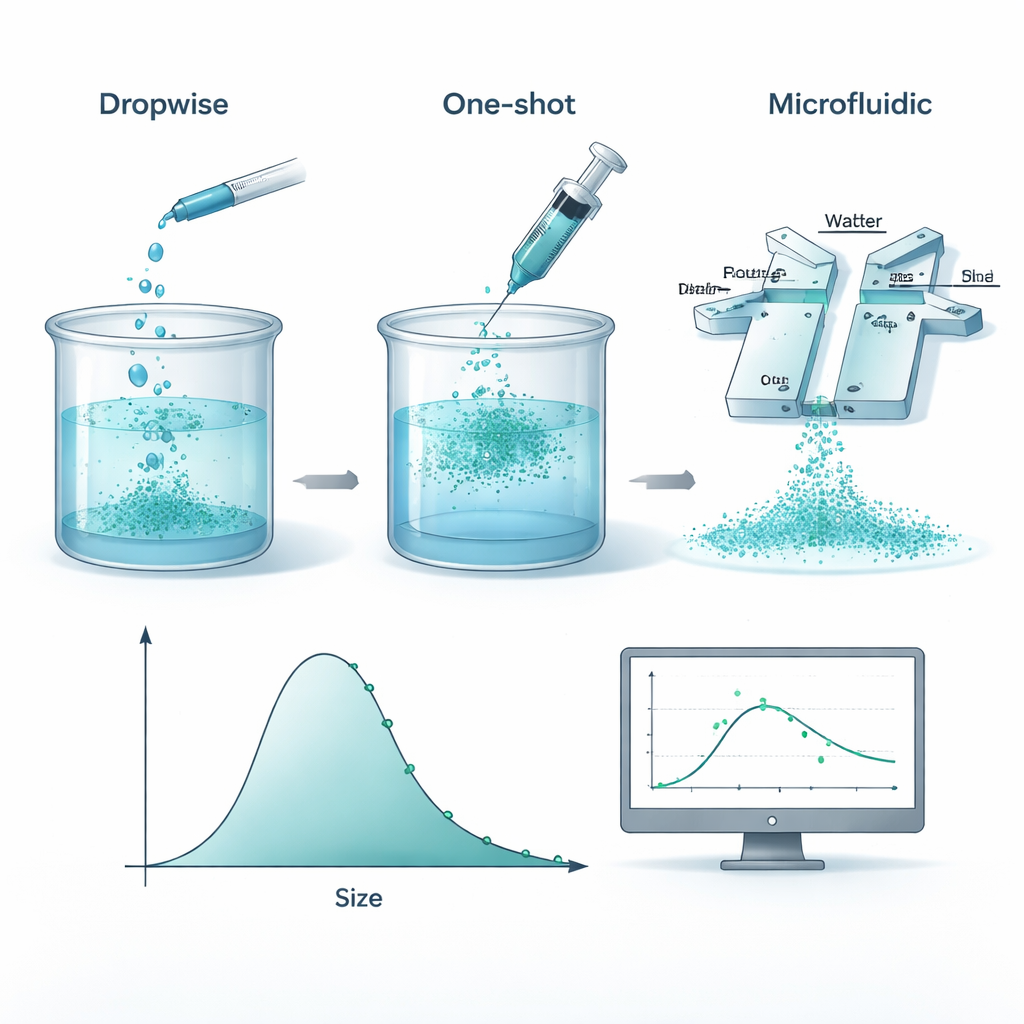
لإنتاج هذه الجسيمات، يذوب الباحثون بلاستيك قابل للتحلل يُسمى بوليكابرولاكتون (PCL) في مذيبات عضوية ثم يمزجونه مع الماء بحيث «ينهار» البوليمر من المحلول ويتكوّن على شكل كرات صغيرة. قارن الفريق ثلاث طرق عملية للقيام بذلك: إضافة محلول البوليمر قطرةً قطرة ببطء، صبّه دفعة واحدة، ودفع السائلين عبر شريحة ميكروفلويديك صغيرة حيث يلتقيان في قنوات ضيقة. تحت ظروف محكمة التحكم، أنتجت الطرق الثلاث أحجام جسيمات ومتفاوتاتها المعيارية المتماثلة إلى حد كبير. هذا يعني أنه، على الأقل ضمن النطاقات المدروسة، ما يهم أكثر من أداة الخلط بالذات هو ما تضعه في الخليط—كمية البوليمر والمثبت—أكثر من طريقة التحريك.
كيف يشكل اللزوجة والجزيئات المساعدة الجسيمات
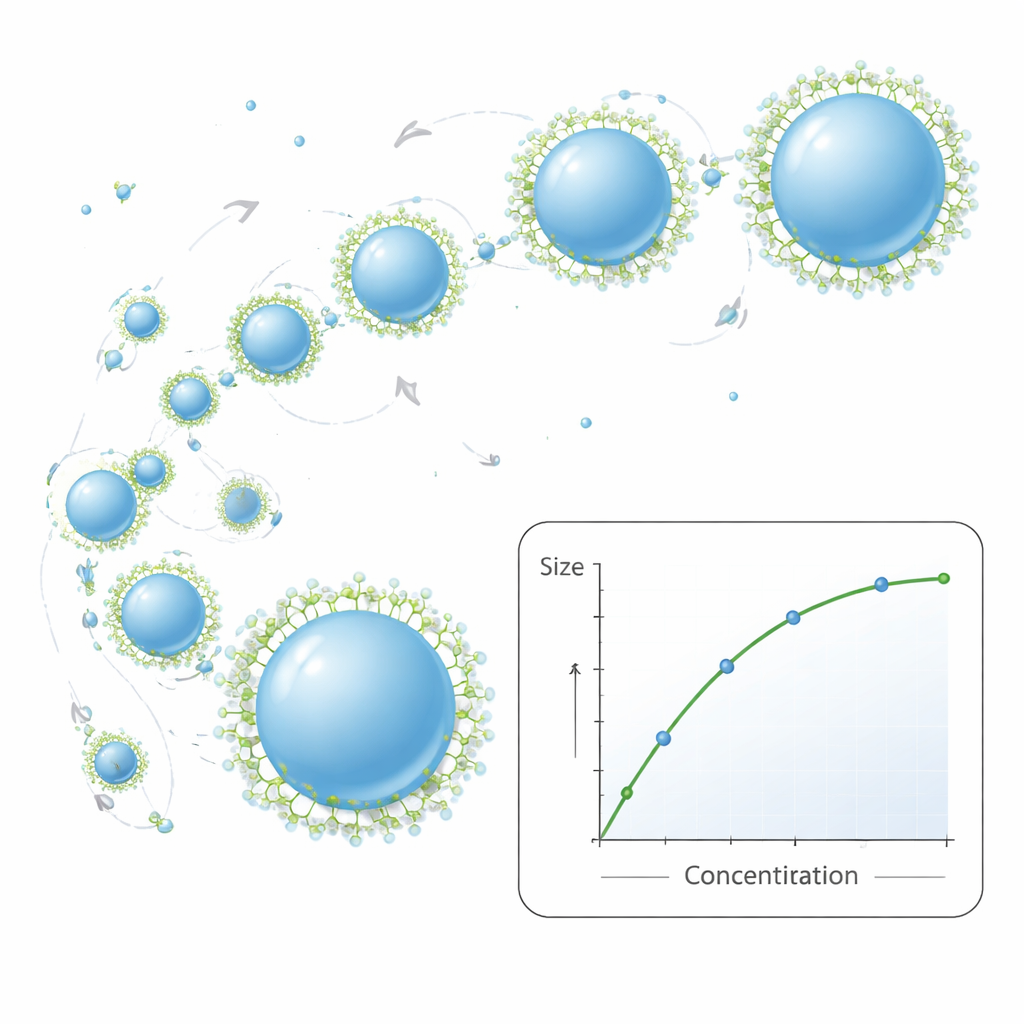
استكشف الباحثون بعد ذلك كيف تتحكم مكونات الوصفة في حجم الجسيم النهائي. زيادة كمية PCL في الطور العضوي تجعل ذلك السائل أكثر سماكة أو لزوجة. تخيل محاولة مزج شراب سميك في الماء بدل العصير: الشراب الأثقل يتفتت إلى قطرات أكبر. هنا، أدت محاليل البوليمر الأثخن إلى جسيمات نانوية أكبر وتوزيعات حجم أوسع قليلاً. إضافة مذيب ثانٍ، الإيثانول، ساعد على الحفاظ على استقرار العملية حتى عند مستويات بوليمر عالية جداً، لكن على حساب جعل الجسيمات أكبر عند نطاق التركيزات العليا. مكوّن ثانٍ، عامل فعال سطحي يُدعى Pluronic F‑127، يعمل كعامل مضاد للتكتل على المستوى الجزيئي. عند مستويات منخفضة من السطحية، تميل الجسيمات إلى التصادم والالتصاق ببعضها، مما يجعلها أكبر وأقل تجانساً. مع زيادة تركيز العامل السطحي، يغطي أسطح الجسيمات ويمنع اندماجها، ويؤدي إلى جسيمات أصغر وأكثر استقراراً—حتى نقطة تتناقص عندها المكاسب ويصبح توزيع الأحجام أكثر خليطاً.
قاعدة نمو بسيطة تتطابق مع الواقع
في صميم العمل يوجد نموذج رياضي مضغوط يصف كيف تكبر الجسيمات النانوية بعد ظهورها الأولي. يعامل حركتها كاهتزاز عشوائي في السائل، حيث تؤدي التصادمات أحياناً إلى اندماج جسيمين لتشكيل جسيم أكبر. افترضت النماذج السابقة أنه كلما التقت الجسيمات فإنها تندمج فوراً وتصبح كرات مثالية. يضيف النموذج الجديد لمستين واقعيّتين: أولاً، يسمح بزمن نهائي لتستريح الجسيمات المتلامسة من شكل مستطيل إلى كرة واحدة؛ ثانيًا، يتيح لجزيئات العامل السطحي أن «تغطي» السطح تدريجياً، مما يبطئ أو يوقف المزيد من الاندماج. مع عدد قليل فقط من المدخلات القابلة للقياس—مثل درجة الحرارة، لزوجة السائل، وتركيز البوليمر الابتدائي—يتنبأ النموذج بكيفية تغير متوسط حجم الجسيم مع ظروف الوصفة. عبر العديد من التجارب، طابقت الأحجام المتنبأة عن قرب الأحجام المقاسة بواسطة تشتت الضوء، بينما التقط أيضاً الاتجاهات العامة في اتساع توزيع الأحجام.
استخدام النموذج كأداة تصميم
لاختبار ما إذا كان هذا النهج مفيداً فعلاً، قلب الفريق المسألة: بدلاً من مطالبة النموذج بشرح بيانات ماضية، طلبوا منه اقتراح وصفات ينبغي أن تنتج ثلاثة أحجام جسيمات محددة ودرجات من التجانس. ثم حضروا هذه التركيبات «المصممة» في المختبر. اختلفت أقطار الجسيمات المقاسة عن المستهدفة بنسبة 1–7 في المئة فقط—ضمن التباين التجريبي المعتاد—مما يُظهر أن النموذج يمكنه توجيه اختيارات التركيبة بشكل موثوق. كانت التنبؤات بخصوص مدى ضيق أو اتساع توزيع الأحجام أقل دقة، لكنها كانت لا تزال جيدة بما يكفي للتمييز بين مجموعات أكثر تجانساً وأخرى أكثر انتشاراً. بالمقارنة مع طرق المحاكاة الثقيلة التي تتتبّع كل جزيء أو كل دوامة في التدفق، يعمل هذا النموذج المبسّط بسرعة على حواسب متواضعة ويسهل تكييفه لأنواع بوليمرات وترتيبات معالجة أخرى.
ما يعنيه هذا لمستقبل الأدوية النانوية
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن صنع جسيمات نانوية مفيدة لم يعد مضطراً لأن يعتمد فقط على التجربة والخطأ المرهقة في المختبر. من خلال التقاط الفيزياء الأساسية لكيفية تحرك القطرات البلاستيكية الصغيرة وتتصادم وتُحَمى بواسطة العوامل السطحية، تقدم هذه الدراسة «خريطة» عملية تربط خيارات التركيبة—كمية البوليمر، مزيج المذيبات، كمية المثبت—بحجم الجسيم النهائي. ونظراً لأن PCL مادة قابلة للتحلل ومستخدمة شائعاً في توصيل الأدوية، والغرسات، وعوامل التصوير، فقد يساعد هذا النموذج الباحثين على تصميم أدوية نانوية أكثر أماناً وفاعلية بسرعة أكبر وبمخلفات أقل. يمكن توسيع نفس المبادئ لتشمل بوليمرات أخرى، مما يجلب مزيداً من التنبؤ والكفاءة إلى عالم العلاجات بحجم النانو.
الاستشهاد: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
الكلمات المفتاحية: جسيمات نانوية بوليمرية, ترسيب نانوي, توصيل الأدوية, النمذجة العددية, بوليكابرولاكتون