Clear Sky Science · ar
تُعرّف الجينات المتعلقة بإزالة اليوبيكويتين الأنماط المناعية في سرطان القولون والمستقيم وترتبط بالتنبؤ والبصمات المرتبطة بالعلاج المناعي
لماذا تكون هذه الدراسة مهمة للناس
يُعد سرطان القولون والمستقيم من بين أكثر السرطانات شيوعًا وفتكًا على مستوى العالم، ومع ذلك قد يختلف توفُّر النتائج واستجابة المرضى للعلاجات الحديثة مثل العلاج المناعي كثيرًا حتى بين أورام تبدو متشابهة تحت المجهر. تطرح هذه الدراسة سؤالًا جديدًا: هل يمكننا تصنيف سرطانات القولون والمستقيم إلى مجموعات أوضح من خلال النظر في كيفية تعامل خلايا الورم مع "إعادة تدوير" البروتينات وكيف يرتبط ذلك بدفاعات الجهاز المناعي؟ قد يساعد الجواب الأطباء على توقع مسار المرض بشكل أفضل وتصميم تراكيبات علاجية أذكى في المستقبل.
تنظيف البروتين وسلوك السرطان
داخل كل خلية تُوسَم البروتينات البالية أو المتضررة وتُعاد تدويرها حتى لا تتراكم وتسبب مشاكل. أحد مسارات هذا النظام، المسمى إزالة اليوبيكويتين، يزيل تلك الوسوم ويساهم في ضبط دقيق لأي البروتينات تُدمر وأيها تُحفظ. جمع المؤلفون مجموعات بيانات عامة واسعة لأورام الأمعاء والأنسجة السليمة وفحصوا آلاف الجينات للعثور على تلك المرتبطة بهذا النظام لتنظيف البروتين وببقاء المرضى. قلّصوا القائمة إلى 17 جينًا رئيسيًا ارتبطت بشدة بالتحكم في انقسام الخلايا، وإصلاح تلف الحمض النووي، وببنية المادة المحيطة بالخلايا. أصبحت هذه الجينات العمود الفقري لطريقة جديدة في تجميع سرطانات القولون والمستقيم.
ينبثق نوعان رئيسيان من الأورام
باستخدام أنماط النشاط في الجينات الـ17، قسم الباحثون الأورام إلى نوعين فرعيين رئيسيين. كان الأشخاص في مجموعة واحدة يميلون إلى العيش لفترة أطول وكان المرض لديهم في مرحلة مبكرة أكثر. أما المجموعة الأخرى فكان توقعها أسوأ. عند فحص الفريق بصورة أوسع للجينات التي كانت مفعّلة أو مطفأة في كل نوع فرعي، ظهر أن مجموعة النتائج السيئة أظهرت إشارات قوية لانقسام الخلايا السريع، واستجابات إجهاد لضرر الحمض النووي، وإعادة تشكيل كثيفة للهيكل النسيجي المحيط بالورم. بالمقابل، أظهر نوع النتائج الأفضل قدرًا أقل من هذا التشكيل العدواني ونمطًا أكثر توازنًا لانقسام الخلايا وإصلاحها.
جوار الورم والاستجابة المناعية
لا ينمو السرطان في عزلة؛ بل يعيش ضمن جوار من الخلايا المناعية والخلايا الداعمة والنسيج الشبيه بالندبة. استخدمت الدراسة أدوات حاسوبية لتقدير أي الخلايا المناعية كانت حاضرة في كل ورم. أظهرت الفئتان الفرعيتان مناظر مناعية مختلفة بوضوح. كان النوع ذو النتائج السيئة غنيًا بالكولاجين والكُتَل الليفية، مكوِّنًا حاجزًا ماديًا وكيميائيًا يمكن أن يمنع خلايا تي المقاتلة من الوصول. كما حمل إشارات للكبت المناعي ودرجات أعلى في مقاييس تتنبأ بالمقاومة للعلاج المناعي. أما النوع ذو النتائج الأفضل فكان لديه تراكم مصفوفة أقل، وتشكيلات مناعية أكثر ملاءمة مثل خلايا تي القاتلة وخلايا تي المساعدة، ودرجات توحي بحساسية أكبر للعلاجات المناعية.
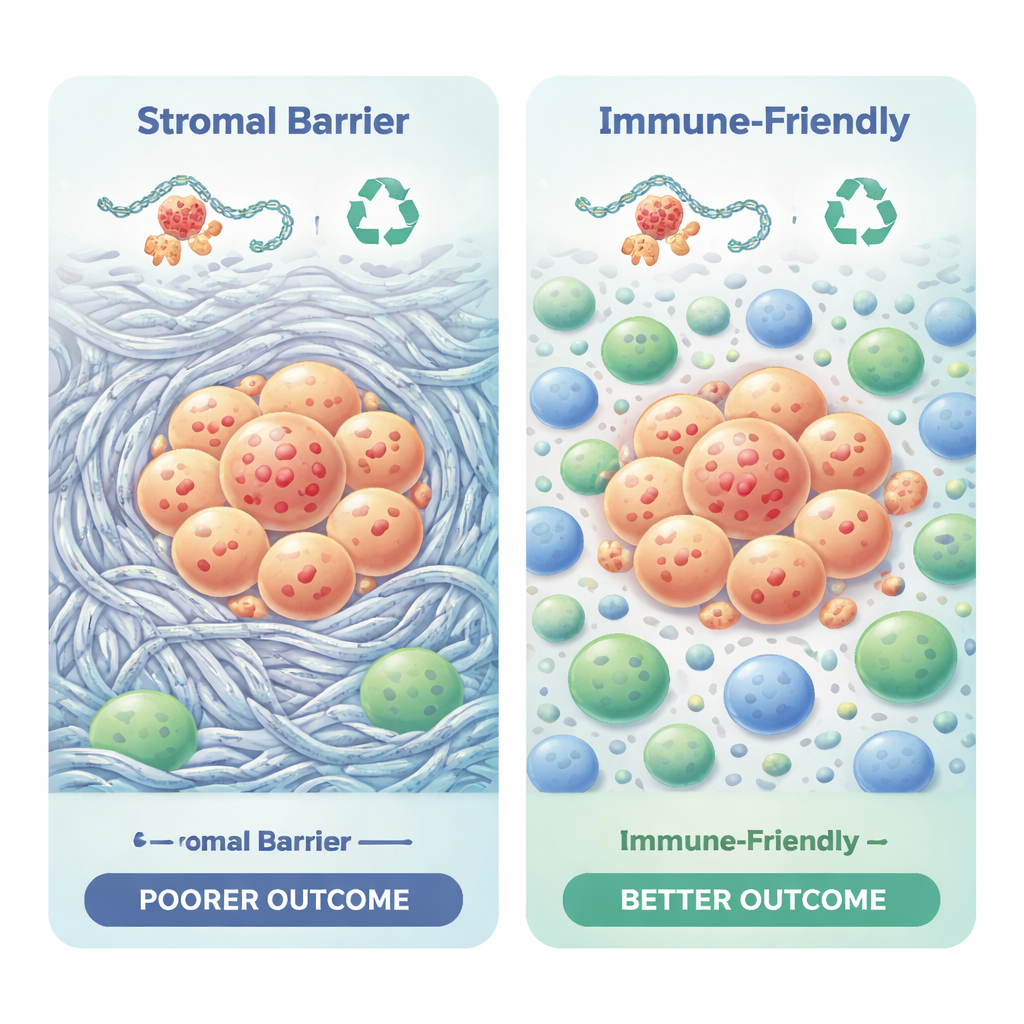
جينات بنيوية رئيسية كمنارات تحذيرية
للقفز من الأنماط العامة إلى علامات عملية، بنى المؤلفون شبكات للبروتينات المتفاعلة وبحثوا عن جينات "محورية" مركزية. حدّدوا تسعة جينات تشارك بشكل كبير في بناء وإعادة تشكيل السقالة النسيجية المحيطة بالورم، بما في ذلك عدة كولاجينات وجزيئات مثل الفايبرونيكتين والبيريوستين. كان النشاط العالي لبعض هذه الجينات، وخصوصًا BGN وFN1 وPOSTN، علامة متكررة على بقاء أسوأ في مجموعتين مستقلتين من المرضى. تقع هذه الجينات المحورية عند تقاطع الصلابة الميكانيكية والإشارات الكيميائية وتجنيد الخلايا المناعية، مما يجعلها مرشحة جذابة لاختبارات مستقبلية قد تساعد في توقع المخاطر أو توجيه خيارات العلاج.
ما الذي يعنيه ذلك للمستقبل
هذا العمل لم يغير بعد طريقة علاج المرضى، لأنه يعتمد على تحليل حاسوبي لبيانات موجودة بدلًا من تجارب سريرية جديدة. ومع ذلك، يقدم خلاصة واضحة وغير متخصصة: يبدو أن طريقة تعامل الورم القولوني المستقيمي مع إعادة تدوير البروتين وإعادة تشكيل بيئته المحلية تساهم في تحديد ما إذا كان الجهاز المناعي قادرًا على الوصول إليه ومهاجمته. تميل الأورام ذات اضطراب شديد في التحكم بالبروتين وقشرة ليفية سميكة إلى صد الخلايا المناعية وترتبط بنتائج أسوأ، بينما تؤدي الأورام ذات ندبات أقل ووصول أكثر انفتاحًا للخلايا المناعية إلى نتائج أفضل. في المستقبل، قد تكون تراكيب من أدوية تستهدف إصلاح الحمض النووي أو المصفوفة الليفية مع العلاج المناعي مفيدة بشكل خاص للمجموعة عالية المخاطر المعرفة في هذه الدراسة.
الاستشهاد: Xu, Y., Mo, Z., Jiang, Q. et al. Deubiquitination-related genes define immune subtypes of colorectal cancer and are associated with prognosis and immunotherapy-related signatures. Sci Rep 16, 4862 (2026). https://doi.org/10.1038/s41598-026-35271-5
الكلمات المفتاحية: سرطان القولون والمستقيم, البيئة الميكروية للورم, الأنماط المناعية الفرعية, تحلل البروتينات, العلاج المناعي