Clear Sky Science · ar
إعادة برمجة التمثيل الغذائي تعزز مقاومة الإجهاد التأكسدي في الخلايا القلبية المتمايزة
لماذا تهم معركة خلايا القلب مع الأكسجين
يعتمد كل نبضة من قلبك على خلايا عضلية متخصصة تُسمى الخلايا القلبية. مع نمونا تواجه هذه الخلايا تحوّلاً كبيراً في حياتها: تنتقل من بيئة منخفضة الأكسجين ومعتمدة على السكريات داخل الرحم إلى عالم غني بالأكسجين بعد الولادة. الأكسجين ضروري، لكنه أيضاً يولد نواتج ثانوية ضارة يمكن أن تَتلف الحمض النووي وتقتل الخلايا. تستكشف هذه الدراسة كيف تُعيد خلايا القلب الناضجة برمجة تمثيلها الغذائي بحيث تتمكن من التعامل مع مزيد من الأكسجين، وتوليد طاقة أكبر، وفي الوقت نفسه تحمي نفسها من الضرر التأكسدي — وهو ما قد يوفر رؤى لعلاجات مستقبلية لأمراض القلب وتجديد الأنسجة.
من بناة بسيطين إلى رياضيين للطاقة
الخلايا القلبية غير الناضجة، المعروفة باسم الخلايا القلبية البدئية، هي خلايا صغيرة منقسمة تعتمد أساساً على تحطيم الجلوكوز للحصول على الطاقة. ومع تمايزها إلى خلايا قلبية ناضجة، تتوقف عن الانقسام وتكبر، وغالباً ما تندمج لتشكّل خلايا متعددة النوى وممدودة أكثر ملاءمة للانقباض القوي. باستخدام المجهر عالي الدقة، راقب الباحثون هذا التحول على مدى عشرة أيام في نموذج خلوي مخبري. انخفضت مؤشرات تكاثر الخلايا بينما امتدت الخلايا وأعادت تنظيم نفسها إلى هياكل ليفية تشبه القلب، ما أكد دخولها حالة أكثر شبهاً بالخلايا البالغة وقابلة للانقباض. 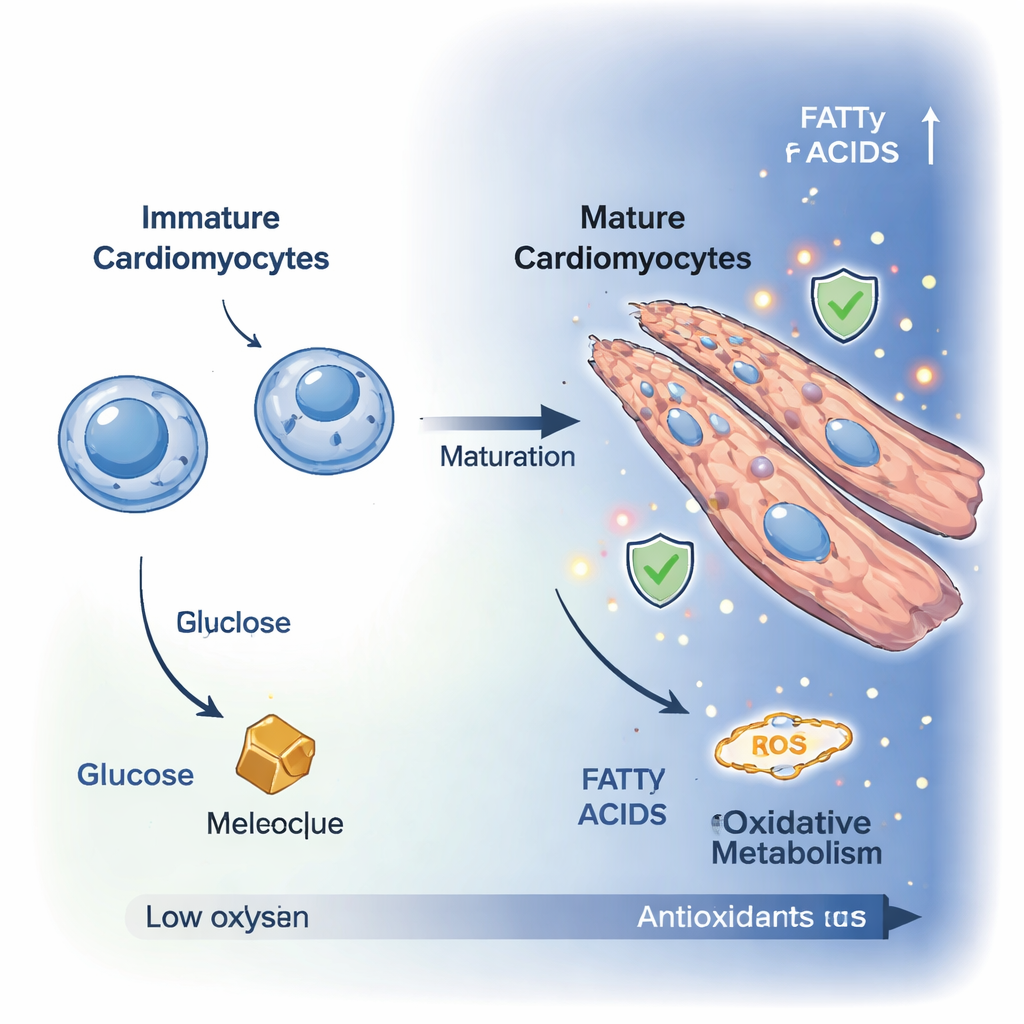
تغيير مصادر الوقود وتوصيل طرق طاقة جديدة
لفهم ما يحدث داخلياً، قاس الفريق مئات الجزيئات الصغيرة داخل الخلايا واستخدم تصويراً متقدماً لتوهج الخلايا الطبيعي لتعقّب استخدام الطاقة في الوقت الحقيقي. أظهرت هذه التقنيات معاً تحوّلاً واضحاً من حالة تحلل سكري (التحلل اللبني)، حيث تعتمد الخلايا أساساً على حرق الجلوكوز، إلى حالة أكسدة تهيمن عليها تنفس الميتوكندريا. انخفضت مستويات الجلوكوز والفركتوز، بينما ازداد تركيز وسائط دورة حمض ثلاثي الكربوكسيل (دورة TCA) — مثل حمض الستريك، الماليك، والأوكسوغلوتارات. كشفت تحليلات المسارات عن نشاط أقوى في الطرق التي تغذي الميتوكندريا بالوقود، بما في ذلك ناقل الماليك–الأسبارتات وتفكك الأحماض الأمينية، مما يشير إلى أن الخلايا القلبية الناضجة توسع خيارات الوقود لديها وتوجه الطاقة بكفاءة أكبر إلى محطات الطاقة الخاصة بها.
العيش مع مزيد من الأكسجين — ومزيد من الإجهاد
حرق الوقود بكفاءة أكبر في الميتوكندريا له ثمن: إنتاج أعلى لأنواع الأكسجين التفاعلية (ROS)، وهي جزيئات كيميائية عدوانية يمكن أن تُتلف الدهون، والبروتينات، والحمض النووي. وجد الباحثون أنه مع نضوج الخلايا القلبية، أصبحت ميتوكندرياتها أكبر وأكثر استطالة، وزادت مؤشرات الإجهاد التأكسدي. كشف التصوير القائم على الفلورة عن المزيد من الحبيبات الشبيهة بالليبوفوسين، وهو علامة مميزة للدهون المؤكسدة، وأظهر مسبار نووي مستويات ROS أعلى في الخلايا المتمايزة. أشارت بيانات الميتابولوميات إلى تغيرات في أيض الجلوتاثيون، وهو نظام مضاد للأكسدة مركزي يستخدم جزيء الجلوتاثيون — المبني من أحماض أمينية مثل الغلوتامات والجليسين — لتحييد ROS. تقترح هذه النتائج أنه مع تصاعد الأيض التأكسدي في خلايا القلب، تضبط أيضاً مساراتها المضادة للأكسدة للحفاظ على الضرر تحت السيطرة. 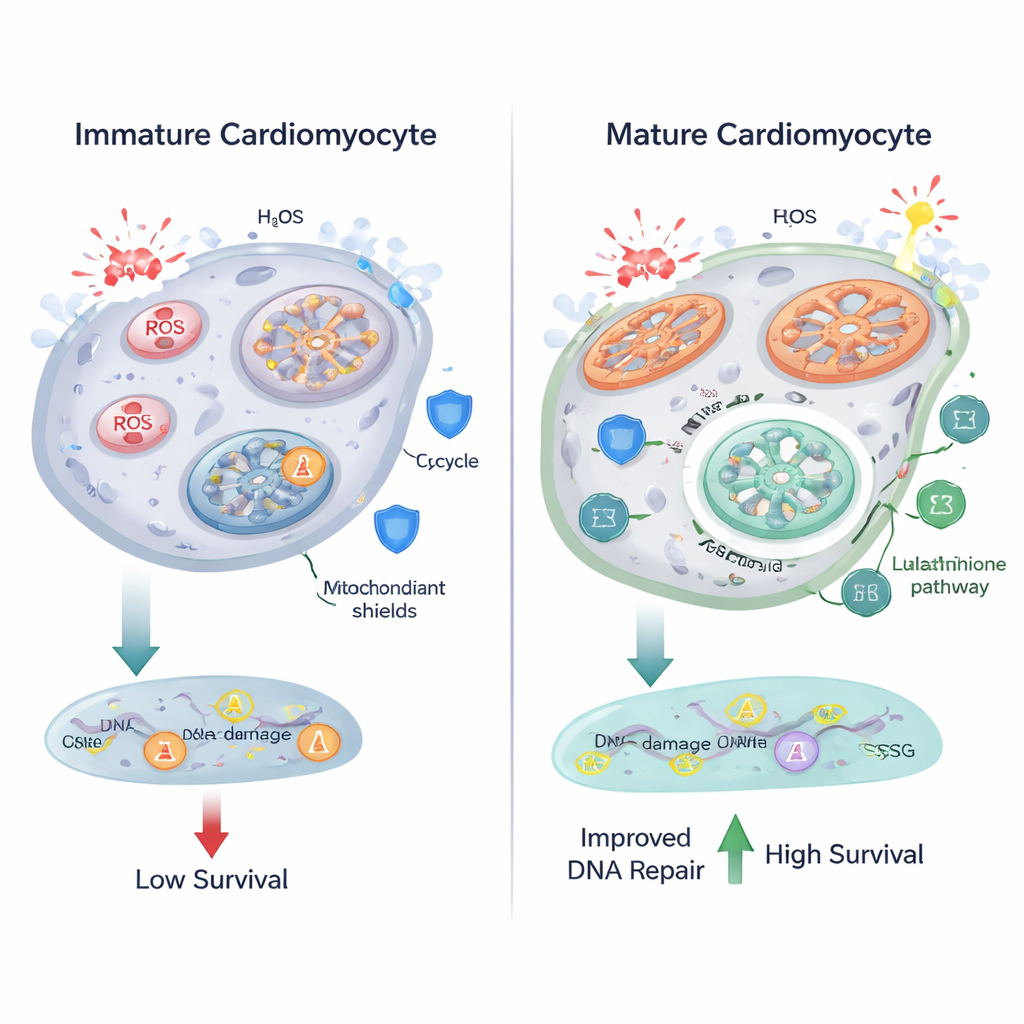
الضرر محصور، والدفاعات معززة
ومن المدهش أنه، على الرغم من ارتفاع ROS، لم تُظهر الخلايا القلبية المتمايزة فواصل حمض نووي أكثر من نظيراتها غير الناضجة عند القياس بواسطة بؤر γ-H2AX، وهو علامة حساسة لتلف الحمض النووي. عندما تحدّى الفريق الخلايا بيروكسيد الهيدروجين، وهو عامل مؤكسد قوي، تراكمت ROS وانكسرت الحموض النووية في كل من الخلايا النامية والناضجة — لكن الخلايا الناضجة أدارت الوضع بشكل أفضل. أظهرت نسبة أقل من الآفات النسبية لمستويات ROS الأعلى لديها، وكانت أقل ميلاً لتنشيط إشارات مرتبطة بموت الخلايا مثل PUMA، وأظهرت معدلات بقاء أعلى بشكل ملحوظ. تشير هذه النتائج إلى أن الخلايا القلبية النامية لا تعدل تمثيلها الغذائي فحسب، بل ترقي أيضاً آليات إصلاح الحمض النووي والبقاء عليها، مما يمكّنها من تحمل ظروف تأكسدية أكثر قسوة.
ما الذي يعنيه هذا لحماية القلب
بعبارات بسيطة، تُظهر هذه الدراسة أنه مع نضوج خلايا القلب، تتعلم العمل بطاقة أعلى دون الاحتراق. فهي تتحول من نمط حياة غني بالسكريات وقليل الأكسجين إلى نمط معتمد على الأكسجة ومحركات ميتوكوندريا، وفي الوقت نفسه تبني دروعاً وفرق إصلاح أفضل للتعامل مع الإجهاد التأكسدي. قد يساعد فهم هذا التوازن الدقيق بين إنتاج الطاقة والحماية الذاتية العلماء على تصميم استراتيجيات لجعل أنسجة القلب البالغة التالفة أكثر قدرة على الصمود، أو لتوجيه الخلايا الجذعية نحو خلايا قلبية أكثر أماناً ومتانة للعلاجات التجديدية.
الاستشهاد: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
الكلمات المفتاحية: تمايز الخلايا القلبية, الإجهاد التأكسدي, الميتوكندريا, تمثيل الخلايا الغذائي, أمراض القلب