Clear Sky Science · ar
فقدان Snhg5 يعطل تنظيم دورة الخلية دون تغيير تكوّن الأكياس في نموذج فأري لمرض الكلى الكيسي
لماذا يهم جين كلوي ذو اسم غريب
مرض الكلى متعدد الأكياس (PKD) هو اضطراب وراثي شائع تتكاثر فيه عدد لا يحصى من الأكياس المملوءة بالسوائل ببطء داخل الكليتين، مما يؤدي غالباً إلى فشل كلوي. يعرف العلماء أن عيوبًا في جينين، PKD1 وPKD2، تقود المرض، لكن هناك العديد من العوامل الجينية الأخرى التي قد تؤثر على سرعة تقدمه. تركز هذه الدراسة على نوع غير اعتيادي من الجينات يُسمى الحمض النووي الريبي الطويل غير المشفر، واسمه Snhg5، وتطرح سؤالًا بسيطًا لكن مهمًا: هل يشكل هذا الجزيء تأثيرًا ذا دلالة في مسار PKD، أم أنه مجرد متفرج إلى حد كبير؟
نظرة أقرب إلى رسول جيني غامض
على عكس الجينات التقليدية التي توفر مخططات للبروتينات، تعمل الأحماض النووية الريبية الطويلة غير المشفرة أكثر كمنظمات جزيئية أو مفاتيح داخل الخلايا. أظهرت أعمال سابقة أن Snhg5 يرتفع بشكل قوي في نماذج الفئران لـ PKD وتم ربطه بعدة أنواع من السرطان وإصابات الكلى، مما يوحي بأنه قد يحفز نموًا ضارًا. ابتدا الباحثون بتخطيط مكان وزمان نشاط Snhg5 في الفئران الطبيعية. وجدوا أنه يُشغّل في العديد من الأعضاء، مع مستويات مرتفعة بشكل خاص في الأمعاء، وأن نشاطه في الكلى ينخفض حدة بعد الولادة، مع تحوّل العضو من نمو سريع إلى حالة أكثر استقرارًا ونضجًا. داخل خلايا الكلى، توجد شبه كل جزيئات Snhg5 في النواة، مركز القيادة الذي يحتوي على الحمض النووي، ما يوحي بأن Snhg5 يساعد في التحكم بنشاط الجينات بدلاً من بناء البروتينات مباشرة.
أنماط في الكلى المريضة لا تروي القصة كاملة
قارن الفريق بعد ذلك مستويات Snhg5 في مجموعة من نماذج الفئران لـ PKD. في النماذج سريعة التطور، حيث تتشكل الأكياس بسرعة، ارتفع Snhg5 بمقدار ضعفين إلى ثلاثة أضعاف في الكلى المريضة، وأظهرت الصور على مستوى الخلية الواحدة إشارات نووية قوية في الخلايا المبطنة للأكياس والنسيج المحيط. بشكل مفاجئ، عندما نظروا إلى نموذج فأري أبطأ وأخف يحاكي المسار الطويل للبشر، لم يزد Snhg5. والأكثر بروزًا، في نسيج كلوي بشري من أشخاص مصابين بـ PKD السائد جينيًا في مرحلة متقدمة، كان النظير البشري للجين، المسمى SNHG5، منخفضًا بأكثر من 90 في المئة. مجتمعة، تشير هذه النتائج إلى أن التغيرات في هذا الحمض النووي الريبي ترافق تكوّن الأكياس، لكن اتجاه وتوقيت التغير يختلفان بين الأنواع ومراحل المرض، مما يثير الشكوك في أن Snhg5 وحده هو محرك مباشر لنمو الأكياس.
ماذا يحدث عند إزالة الجين
للتقدم من الارتباط إلى السببية، استخدم الباحثون تحرير الجينات CRISPR لحذف جين Snhg5 بالكامل في الفئران، فأنشأوا سلالة «مطسوقة» شاملة. خلافًا للمخاوف من أن إزالة مثل هذا الجزيء المتغير بشدة قد تكون ضارة، وُلدت الفئران التي تفتقر إلى Snhg5 بنسب طبيعية، وعاشت أعمارًا طبيعية، وكانت كليتاها تبدو وتعمل مثل تلك لدى أقرانها الأصحاء. أظهر الفحص المجهري بنية كلية طبيعية دون ندوب أو التهاب، وأظهرت اختبارات الدم عدم وجود علامات على ضعف التصفية الكلوية. على المستوى الجزيئي، برزت تغييرات أدق: أظهرت كل من كلى الفئران وخلايا أنابيب الكلى المزروعة دون Snhg5 تحولات متسقة في نشاط الجينات المرتبطة بانقسام الخلايا ونسخ الحمض النووي. في زراعة الخلايا، توقف عدد أكبر من الخلايا في مراحل متأخرة من دورة الخلية وفي حالة تالفة تُعرف بـ sub-G1. كان بروتين واحد على وجه الخصوص، ARPC5، وهو جزء من مركب يساعد الخلايا على الانقسام عن طريق إعادة ترتيب الدعامة الداخلية، منخفضًا عند غياب Snhg5، مما يلمّح إلى سلسلة محتملة من السبب والتأثير.
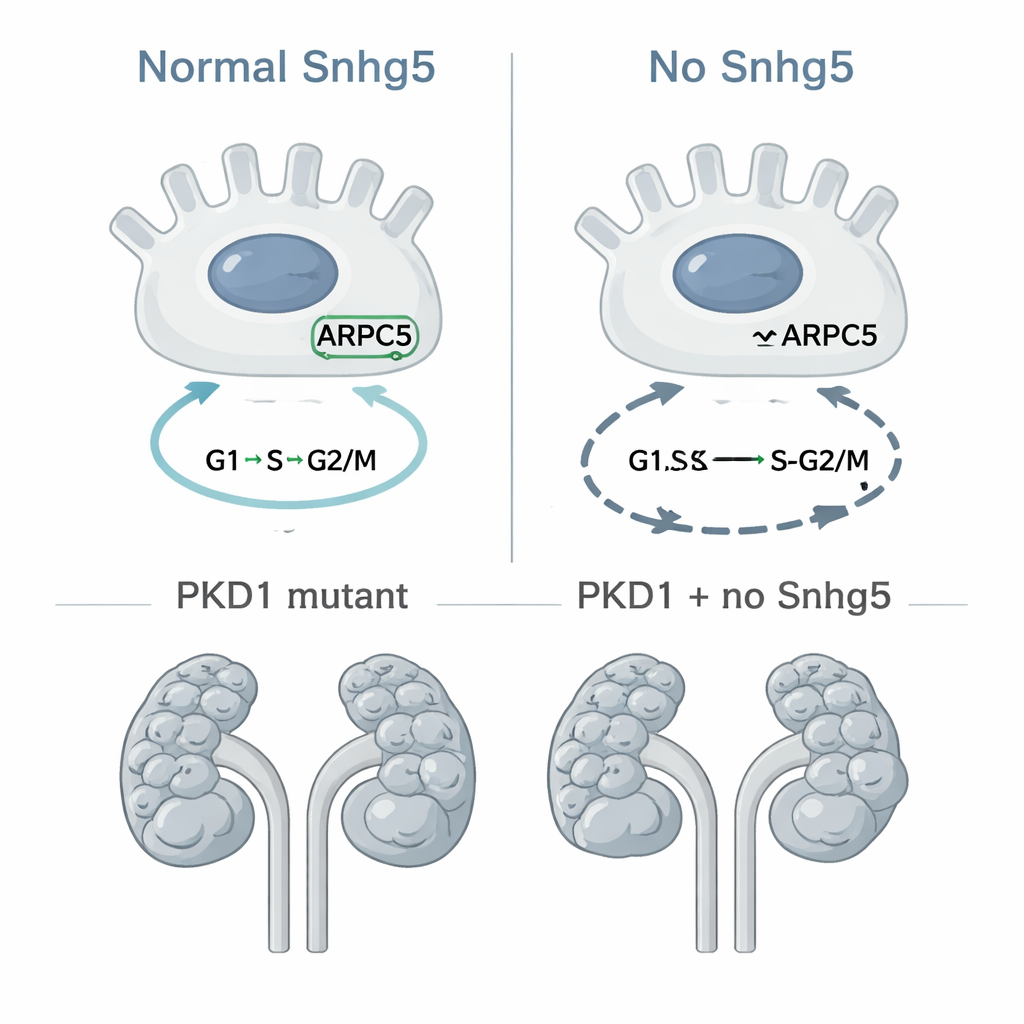
اختبار دوره في نمو الأكياس مباشرة
نظرًا لأن الانقسام الخلوي غير المضبوط هو سمة أساسية في PKD، سأل الفريق بعد ذلك ما إذا كانت إزالة Snhg5 ستبطئ تكوّن الأكياس في نموذج فأري راسخ تُعطل فيه جين PKD1 خصيصًا في خلايا قناة التجميع، مصدر العديد من الأكياس. قاموا بتربية فئران بحيث كان لبعضها طفرة PKD1 فقط، بينما افتقر البعض الآخر إلى كل من PKD1 وSnhg5. عندما فحصوا الحيوانات في اليوم العاشر من العمر، ظهر أن المجموعتين لديهما كليتان شديدتا التكيّس، وأظهرت القياسات الدقيقة لحجم الكلية ومساحة الأكياس وعددها عدم وجود حماية معنوية من حذف Snhg5. إن وُجد اختلاف، فقد مال فأروا الطفرة المزدوجة إلى حمل كيسي أكبر قليلًا، على الرغم من أن الفرق كان صغيرًا وغير مقنع إحصائيًا. بعبارة أخرى، على الرغم من أن Snhg5 يؤثر في جينات دورة الخلية في خلايا الكلى، فإن غيابه لا يغير بصورة ملحوظة سرعة ظهور أو توسع الأكياس في هذا النموذج المحدد من PKD.
ما الذي يعنيه هذا للعلاجات المستقبلية
بالنسبة للمرضى ومطوري الأدوية، الخلاصة الرئيسية هي أن Snhg5، رغم كونه أحد الإشارات الجينية المتغيرة بشدة في نموذج فأري لـ PKD، ليس حجر الزاوية في تكوّن الأكياس — على الأقل ليس في المرحلة المبكرة سريعة النمو لمرض مشتق من قنوات التجميع. يبدو أن الجين يضبط بدقة كيفية تقدم خلايا الكلى خلال دورة الانقسام، على الأرجح عبر تأثيره على عوامل مثل ARPC5، لكن هذا التأثير دقيق بما يكفي لدرجة أن فقدانه الكامل يترك تطور الكلى وتقدم PKD المبكر دون تغيير كبير. تؤكد هذه النتائج درسًا أوسع: ليست كل تغيرات جزيئية بارزة في الأنسجة المريضة هدفًا علاجيًا واعدًا. سيفرض فصل السبب عن النتيجة اختبار الأحماض النووية الريبية الطويلة مثل Snhg5 عبر نماذج مرضية ونقاط زمنية متعددة قبل أن يمكن متابعتها بثقة كمرشحات دوائية.
الاستشهاد: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
الكلمات المفتاحية: مرض الكلى متعدد الأكياس, الحمض النووي الريبي الطويل غير المشفر, Snhg5, دورة الخلية, أكياس الكلى