Clear Sky Science · ar
نانوكبسولات الكيتوزان-ديكستران سلفات لتعزيز فعالية التيجيسيكلين ضد السالمونيلا الانتيرية غير التيفية
لماذا هذا الأمر مهم لسلامة الغذاء
يعرف معظم الناس السالمونيلا كمسبب مزعج للتسمم الغذائي، غالباً المرتبط بالدواجن غير المطهية جيداً. لكن القليلين يدركون أن بعض السلالات أصبحت مقاومة للمضادات الحيوية لدرجة أن أدوية قوية تُستخدم كملاذ أخير قد تفشل. تستعرض هذه الدراسة نهجاً قائماً على النانوتكنولوجيا لإنقاذ أحد هذه الأدوية، التيجيسيكلين، عن طريق تعبئته داخل كبسولات صغيرة قائمة على السكريات تساعده على التسلل إلى الخلايا المصابة وإيقاف آليات المقاومة الرئيسية في السالمونيلا.
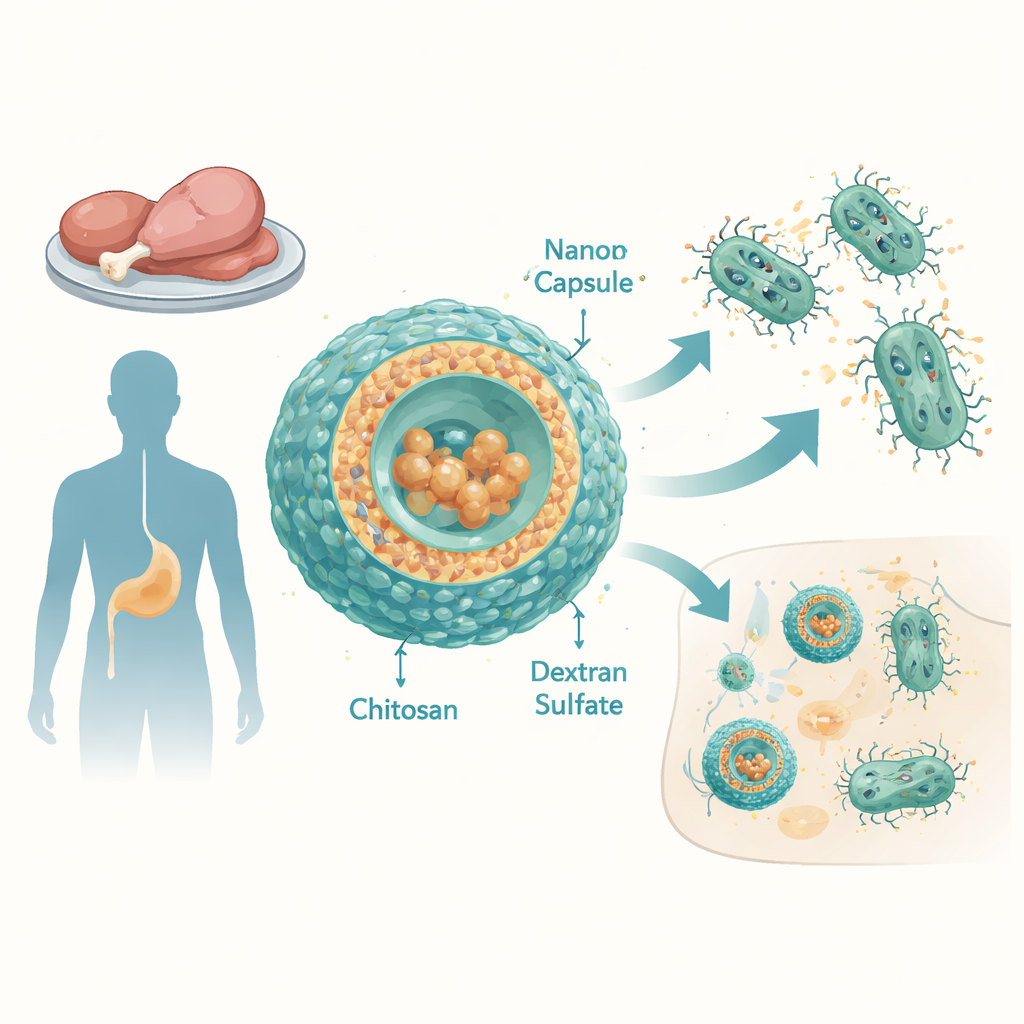
التهديد المتزايد من سلالات السالمونيلا الشرسة
السلالات غير التيفية من السالمونيلا (NTS) تعتبر سبباً رئيسياً للإسهال وعدوى مجرى الدم في جميع أنحاء العالم، وخصوصاً في البلدان منخفضة ومتوسطة الدخل. درس الباحثون 12 سلالة من Salmonella enterica مأخوذة من لحوم الدجاج والبط في مصر. كانت هذه السلالات مقاومة للعديد من المضادات الحيوية الشائعة الاستخدام، بما في ذلك البنسيلينات والسيفالوسبورينات والتيتراسايكلينات وغيرها، وأظهرت درجات عالية من المقاومة المتعددة للمضادات. حتى التيجيسيكلين، وهو دواء واسع الطيف محجوز للحالات الصعبة، أظهر فعالية ضعيفة: إذ كانت البكتيريا تتحمل تركيزات عالية جداً منه. وكان سبب رئيسي لذلك هو فرط نشاط "مضخات الطرد"—آلات جزيئية موجودة في غشاء البكتيريا وتعمل على ضخ المضادات الحيوية خارج الخلية باستمرار.
بناء كبسولة دوائية أذكى
لمواجهة ذلك، صمم الفريق كبسولات على مقياس النانو مصنوعة من بوليمرين طبيعيين: الكيتوزان المستخرج من الكيتين (المادة الموجودة في قشور اللافقاريات)، وديكستران سلفات، وهو جزيء سكري متفرع. من خلال ضبط نسب هذه المكونات بعناية، أنتجوا جسيمات مستقرة بحجم نحو 100–150 نانومتر، ذات شحنة سطحية موجبة تساعدها على التفاعل مع أغشية البكتيريا وخلايا العائل. تم تحميل التيجيسيكلين داخل هذه الجسيمات بكفاءة عالية ملحوظة—إذ انتهى الأمر بمعظم الدواء بداخل الكبسولات. في اختبارات مخبرية تحاكي ظروف الدم، أطلقت الكبسولات معظم التيجيسيكلين خلال بضع ساعات، ما يشير إلى أنها قد توصل دفعة قوية من المضاد الحيوي إلى مواقع العدوى.
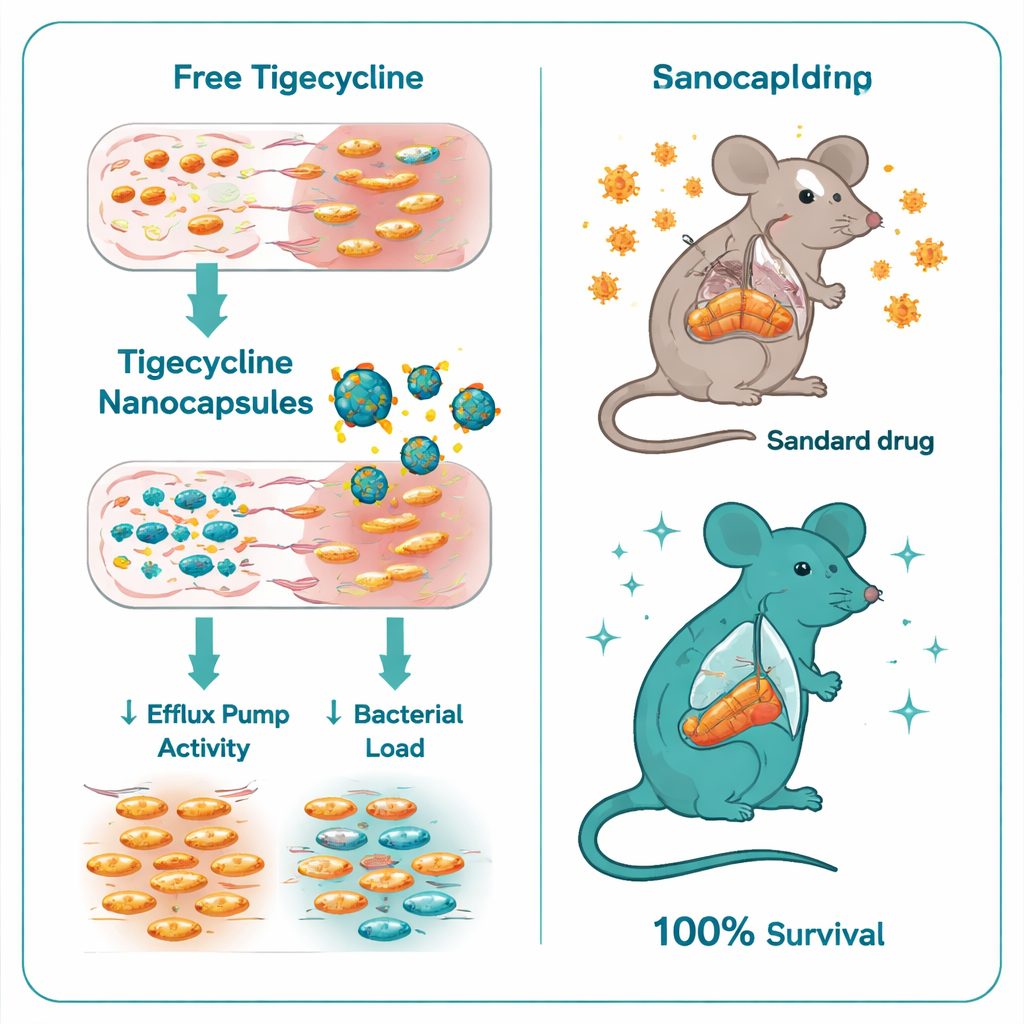
تخفيف دفاعات البكتيريا
عند مقارنة التيجيسيكلين العادي مع التيجيسيكلين المحمّل في نانوكبسولات الكيتوزان–ديكستران سلفات، كان الفرق ملحوظاً. انخفض الحد الأدنى لتركيز الدواء اللازم لإيقاف نمو البكتيريا من 32–128 ميكروغرام لكل مليلتر للتيجيسيكلين الحر إلى 0.5–1 ميكروغرام لكل مليلتر مع النانوكبسولات—تحسن بمقدار ست إلى سبع مرات. أظهرت تجارب وقت-القتل أن الشكل المغلف قتل السالمونيلا بسرعة وبشكل أعمق. وعلى المستوى الجيني، خفّضت النانوكبسولات أيضاً من تنظيم جينات المقاومة الرئيسية: تراجعت معبرات جينات ramA وacrB، التي تساعد في التحكم وتشكيل مضخات الطرد الكبرى، بعدة أضعاف في البكتيريا المعالجة. بعبارة أخرى، لم تقتصر فائدة الكبسولات على توصيل المزيد من الدواء فحسب؛ بل ساعدت أيضاً على إيقاف أحد المسارات الرئيسة لهروب البكتيريا.
حماية الفئران المصابة من مرض قاتل
بعد ذلك اختبر الفريق التركيبة الجديدة في نموذج فأري لعدوى Salmonella Typhimurium الشديدة. ماتت جميع الفئران المصابة غير المعالجة خلال ثمانية أيام. تحسنت حالة الفئران التي تلقت التيجيسيكلين القياسي لكن معدل الوفيات ظل مرتفعاً، مع نجاة 40% فقط. على النقيض التام، نجت كل فأر عولج بالنانوكبسولات المحمّلة بالتيجيسيكلين. كانت هذه الحيوانات تحتوي على عدد أقل بكثير من البكتيريا في كبدها وأمعائها، وكانت فحوصات الدم أقرب إلى وظائف كبد وكلى طبيعية، وظهرت تلفيات نسيجية أخف عند الفحص المجهري. حتى الكبسولات الفارغة من الكيتوزان–ديكستران سلفات، دون مضاد حيوي، قدمت بعض الحماية، ربما لأن للكيتوزان تأثيرات مضادة للميكروبات ومضادة للالتهاب بدرجة معتدلة، لكن الجمع مع التيجيسيكلين كان واضح التفوق.
ماذا قد يعني هذا للعلاجات المستقبلية
بالنسبة لغير المتخصصين، الرسالة الأساسية أن تعبئة مضاد حيوي موجود داخل نانوكبسولة ذكية ومتوافقة حيوياً يمكن أن يعيد له فعاليته ضد سلالات السالمونيلا شديدة المقاومة. من خلال مساعدة الدواء على الوصول إلى البكتيريا المختبئة داخل الخلايا وعن طريق خفض نشاط المضخات التي تطرد الدواء عادة، حوّل نظام الكيتوزان–ديكستران سلفات دواءً احتياطياً يعاني إلى علاج فعال للغاية في الفئران، مع بقاء 100% منها على قيد الحياة. وبينما يلزم مزيد من العمل قبل أن يُستخدم هذا الأسلوب في البشر أو في الحيوانات المزرعية، فهو يقدّم مساراً واعداً لتمديد العمر المفيد للمضادات الحيوية المهمة وتحسين سلامة إمدادات الغذاء لدينا دون الحاجة لاختراع أدوية جديدة تماماً من الصفر.
الاستشهاد: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
الكلمات المفتاحية: السالمونيلا, مقاومة المضادات الحيوية, جسيمات نانوية, توصيل الدواء, تيجيسيكلين