Clear Sky Science · ar
البروتيوماتيك المتكاملة والميتَبولوميك تكشف أن اللاكتونات الفيتوسيسكويتربينية تثبط نشاط خلايا سرطان الثدي ثلاثي السلبي عبر استنزاف تصنيع ATP وإعادة برمجة الأيض الأساسي
مركبات نباتية تجوع سرطان الثدي العدواني
يُعد سرطان الثدي ثلاثي السلبي واحدًا من أصعب أشكال سرطان الثدي علاجًا لأنه يفتقر إلى «مقابض» هرمونية معتادة تستهدفها العديد من الأدوية. تستعرض هذه الدراسة جزيئين مستخرجين من نبات طبي يبدو أنهما يوقفان محطات الطاقة الداخلية في هذه الخلايا السرطانية، مما يقطع عنها إمدادها بالطاقة مع الحفاظ على خلايا الثدي السليمة. فهم آلية عملهما قد يفتح الباب لعلاجات أكثر لطفًا واستهدافًا للمرضى الذين تتوفر لديهم خيارات محدودة حاليًا.
لماذا يهم استهداف مصدر طاقة السرطان
تعتمد كل خلية على هياكل صغيرة تسمى الميتوكوندريا لصنع ATP، وقود الخلية الأساسي. غالبًا ما تعتمد الخلايا السرطانية، وخاصة العدوانية منها، على الميتوكوندريا لدعم النمو السريع والانتشار والبقاء تحت الضغط. ركز الباحثون على خلايا سرطان الثدي ثلاثي السلبي، التي تمثل حوالي 15–20% من حالات سرطان الثدي وتميل للانتكاس والانتقال أكثر من الأنواع الأخرى. درسوا مركبًا طبيعيًا يُدعى ديأوكسي إيليفيانتوبين (DET) وابنه المُصنَّع DETD‑35، وهما لاكتونات سيسكويتربين من نبات Elephantopus الطبي. أظهرت أعمال سابقة أن هذه المركبات تحفز الإجهاد التأكسدي وأشكالًا غير نمطية للموت الخلوي في الخلايا السرطانية، لكن كيفية تعطيلها لمفاعلات الطاقة داخل الخلايا لم تكن مفهومة جيدًا.
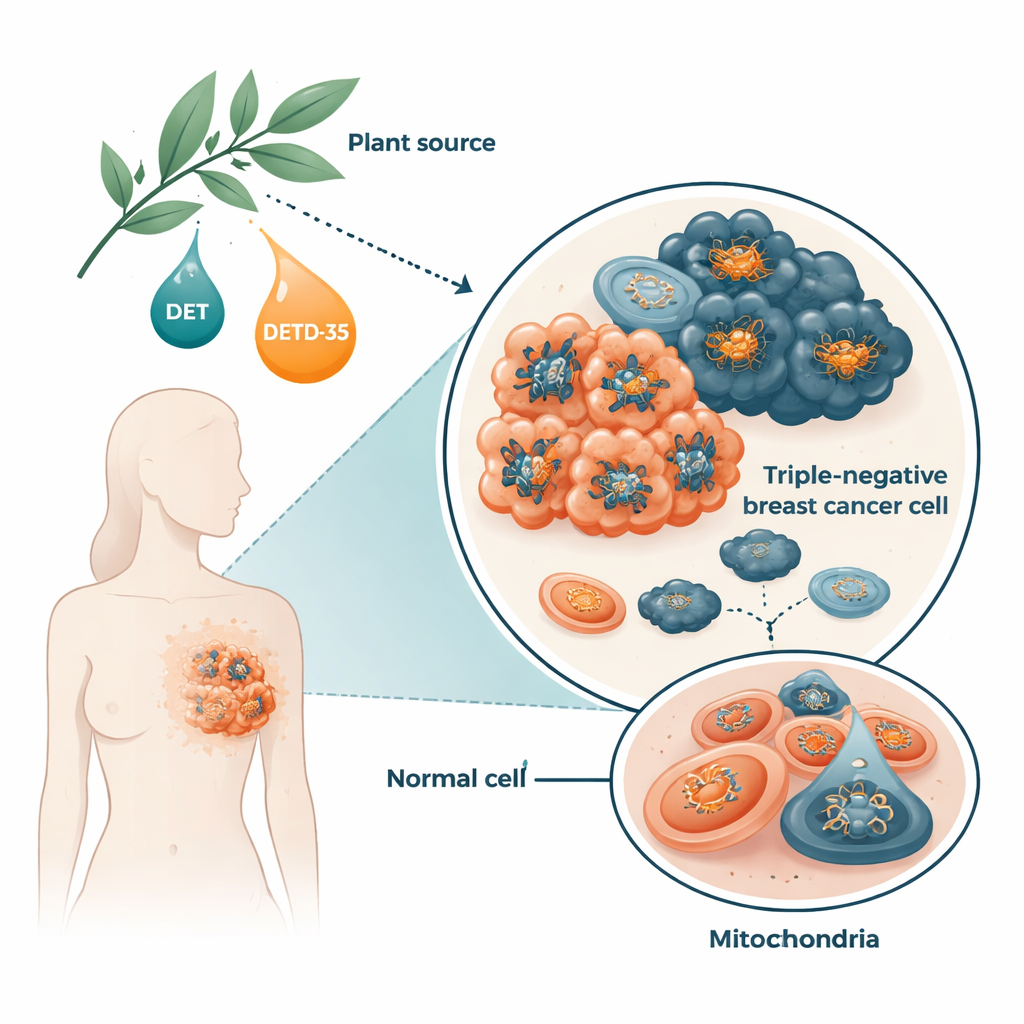
كيف تعطل المركبات النباتية ميتوكوندريا خلايا السرطان
باستخدام خلايا بشرية من سرطان الثدي ثلاثي السلبي مزروعة في المختبر، وجد الفريق أن DET وDETD‑35 زادا بسرعة إنتاج أنواع الأكسجين التفاعلية، وهي نوع من «عوادم» التفاعلات الكيميائية الناجمة عن إنتاج الطاقة. استجابت الخلايا بزيادة بعض الإنزيمات الوقائية، لكن ذلك لم يكن كافيًا لاستعادة التوازن. كما أجبرت المركبات قناة في غشاء الميتوكوندريا تُعرف بممر النفاذية العابر (permeability transition pore) على الفتح، وهو تغيير مرتبط بالانتفاخ وفقدان الشحنة الغشائية والمراحل المبكرة للموت الخلوي. خلال ساعات قليلة فقط، انخفضت مستويات ATP داخل الخلايا السرطانية بشكل حاد. عندما أضاف الباحثون مضاد أكسدة مسبقًا، انقلبت هذه التأثيرات الضارة إلى حد كبير، مما أظهر أن الإجهاد التأكسدي شكّل جزءًا رئيسيًا من العملية.
رسم خريطة الأضرار للبروتينات والأيض
لفهم الصورة الكبيرة، جمع العلماء بين نهجين «أوميكس» قويين. قاموا بفهرسة آلاف بروتينات الميتوكوندريا وقياس العديد من المستقلبات الصغيرة في الخلايا المعالجة مقابل غير المعالجة. كشفت هذه الرؤية المتكاملة أن DET وDETD‑35 يعطلان بروتينات مشاركة في الفسفرة التأكسدية، المسار الرئيسي الذي تستخدمه الميتوكوندريا لصنع ATP، ونشّطا إشارات مرتبطة بالموت. في الوقت نفسه، أُعيد توصيل مسارات أيضية أساسية تتعامل مع الأحماض الأمينية والدهون وكتل البناء للحمض النووي. تغيّرت بعض الدهون التي تساعد في تشكيل الغشاء الداخلي للميتوكوندريا، وكذلك جزيئات مرتبطة بالدفاعات المضادة للأكسدة وتحلل السكر، بطرق تتماشى مع خلايا مرهقة ومُستنزفة طاقيًا. والأهم أن هذه التغيرات الشاملة لم تُشاهد في خلايا الثدي الطبيعية المعرضة لنفس الجرعات، ما يشير إلى درجة من الانتقائية للخلايا الورمية.
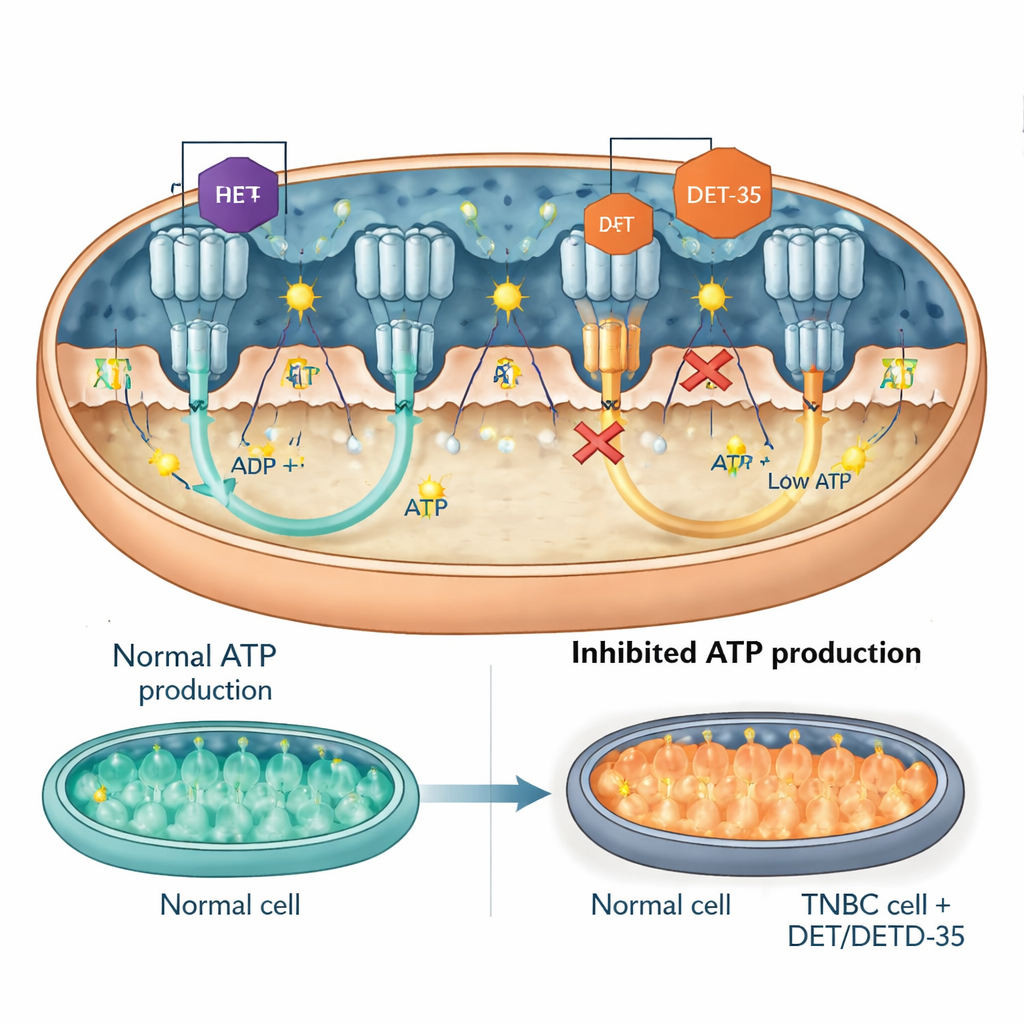
بروتين إشاري رئيسي وتوربين ATP نفسه
ثم ركز الفريق على عناصر محددة داخل هذه الشبكات المضطربة. كان أحدها PRKCA، بروتين إشاري يمكنه الانتقال إلى الميتوكوندريا والتأثير في كل من إنتاج الطاقة واستجابات الإجهاد. زاد DET وDETD‑35 من مستويات PRKCA في الخلايا السرطانية. عندما استخدم الباحثون أدوات جينية لتقليل PRKCA، أصبحت الأدوية أقل سمية: أصبحت الخلايا السرطانية أكثر احتمالًا للبقاء، وأنتجت ATP أكثر، وأظهرت علامات أقل على خلل الميتوكوندريا والابوبتوز. وكان التركيز الآخر على إنزيم تصنيع ATP، «التوربين» الجزيئي الذي يدور لصنع ATP. أظهرت القياسات أن DET وDETD‑35 قللا مباشرة من نشاط إنزيم تصنيع ATP في ميتوكوندريا الخلايا السرطانية. أشارت نماذج الالتحام الحاسوبي إلى أن كلا المركبين يستقران عند واجهات حرجة من الإنزيم، نفس المناطق العامة التي ترتبط بها أدوية معروفة حاصرة لإنزيم تصنيع ATP، مع إعاقة حركته فعليًا وخفض إنتاج ATP. في فئران تحمل أورامًا بشرية لسرطان الثدي ثلاثي السلبي، خفّض العلاج بأي من المركبين مستويات مكونات إنزيم تصنيع ATP في نسيج الورم، مما يدعم النتائج المأخوذة من مزارع الخلايا.
ماذا قد يعني هذا لعلاجات السرطان المستقبلية
بشكل عام، ترسم الدراسة صورة متماسكة: هذه المركبات المستمدة من نباتات تدفع خلايا سرطان الثدي ثلاثي السلبي إلى أزمة طاقة عن طريق تحميلها المفرط بالإجهاد التأكسدي، وفتح مسام الميتوكوندريا، وعرقلة آلية صنع ATP مباشرة. مع تبخُّر ATP وتشويش الأيض، تفقد الخلايا السرطانية قدرتها على النمو والبقاء، بينما تظل خلايا الثدي السليمة إلى حد كبير غير متأثرة تحت نفس الظروف. الخلاصة للقارئ العام هي أن العلماء قد يتمكنون من استغلال اعتماد السرطان الكبير على محطات طاقته الداخلية، باستخدام جزيئات مصممة بعناية — مستوحاة أحيانًا من نباتات — لتفريغ بطاريات الخلايا الورمية دون قطع الكهرباء عن الأنسجة الصحية. يلزم المزيد من العمل قبل أن تصل مثل هذه العوامل إلى العيادة، لكن هذه الرؤية المتكاملة للبروتينات والمستقلبات وتدفق الطاقة تقدم خارطة طريق واعدة.
الاستشهاد: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبي, الميتوكوندريا, إنزيم تصنيع ATP, مستخلصات طبيعية, استقلاب السرطان