Clear Sky Science · ar
البكتيريا في الأطعمة والميكروبيوتا المعوية تُنتج الميثيلغلايوكسال وهذا المستقلب يؤدي إلى تكوّن القلويدات النشطة حيوياً 1‑أسيتيل‑β‑كاربولين
لماذا يهم مختبر الكيمياء في أمعائك
داخل أمعائنا وفي العديد من الأطعمة المخمّرة، تحوّل تريليونات البكتيريا باستمرار السكريات التي نأكلها إلى مجموعة من النواتج الكيميائية. تستعرض هذه الدراسة أحد هذه المسارات بالتفصيل: كيف تحول بعض البكتيريا الشائعة السكريات إلى مركب عالي التفاعل يُدعى الميثيلغلايوكسال، ثم إلى عائلة من الجزيئات النشطة حيوياً المعروفة باسم 1‑أسيتيل‑β‑كاربولينات. ونظراً لأن هذه المواد مرتبطة بعمليات مرضية وفي الوقت نفسه بآفاق علاجية محتملة، فقد يغيّر فهمنا لزمان وكيفية إنتاج البكتيريا لها الطريقة التي نفكّر بها في الطعام، والميكروبيوم، والصحة.
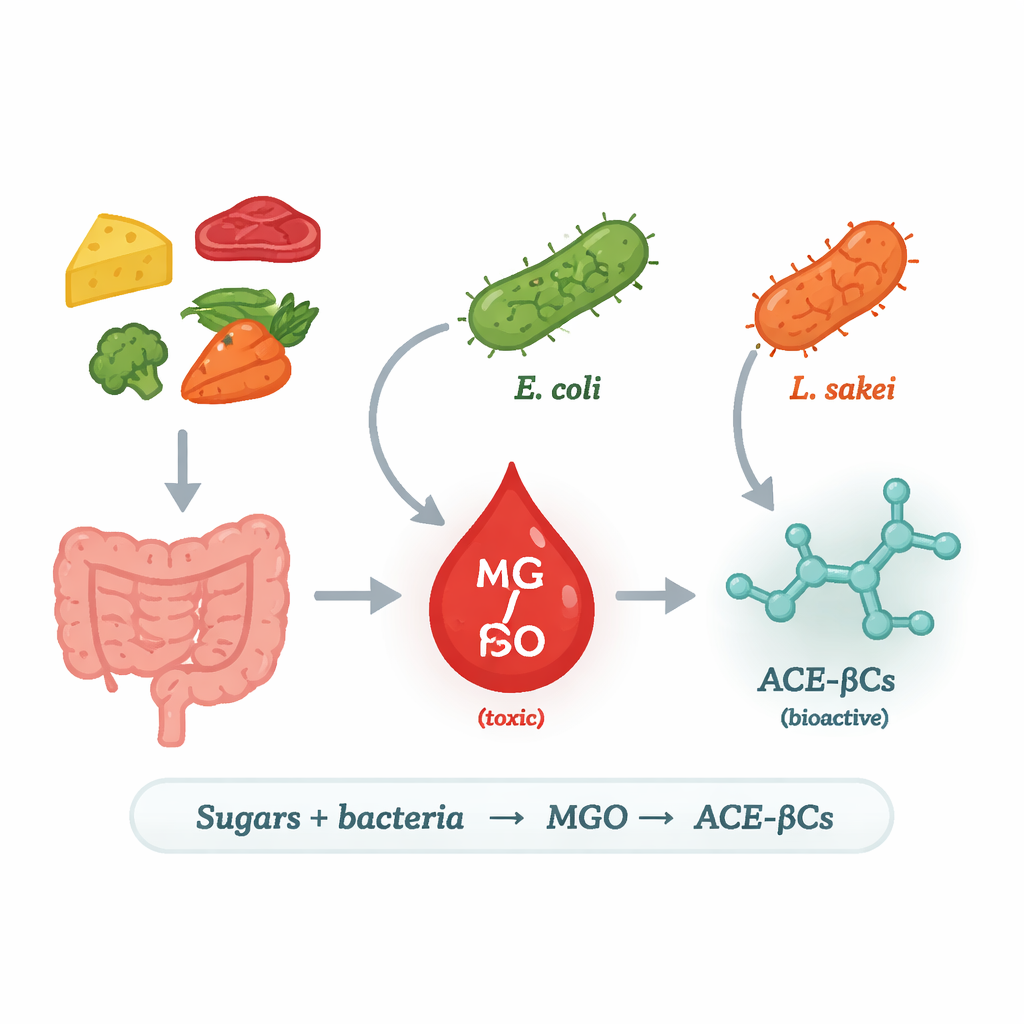
من السكريات اليومية إلى جزيء محفوف بالمخاطر
ركّز الباحثون على الميثيلغلايوكسال (MGO)، وهو ناتج تحلل السكريات شديد التفاعل وسام. في البشر، يرتبط فائض MGO بمرض السكري وأمراض القلب والتنكس العصبي لأنه يمكن أن يتلف البروتينات والحمض النووي. تحافظ خلايانا عادة على MGO تحت السيطرة عبر أنظمة إزالة السموم، لكنها ليست المصدر الوحيد: إذ يمكن للبكتيريا أيضاً إنتاج MGO. في بعض الميكروبات، يحوّل إنزيم يسمى ميثيلغلايوكسال سينثيز (MgsA) وسيط معالجة السكر مباشرة إلى MGO، ما يخلق «اختصاراً» في أيض الطاقة. تساءل الفريق أيّ بكتيريا غذائية ومعوية تستخدم هذا المسار، وتحت أي ظروف، وماذا يحدث لـMGO الذي تطلقه.
من هم المنتجون البكتيريون؟
للإجابة عمّا سبق، نما العلماء عدة سلالات من بكتيريا اللاكتية الموجودة غالباً في الأطعمة، إلى جانب سلالة مخبرية من Escherichia coli، في وسط مسيطر عليه يحتوي إما على الجلوكوز أو الغالاكتوز. ثم تتبّعوا MGO وقلويدين مرتبطين في السائل المزروعي مع مرور الوقت باستخدام كروماتوغرافيا دقيقة للغاية وطيف الكتلة. لم تُنتج سوى E. coli والنوع المرتبط باللحوم Lactilactobacillus sakei كميات ملحوظة من MGO والقلويدات؛ أما بقية بكتيريا اللاكتية المختبرة فلم تُنتجها. كشف بحث جيني عن الفرق المحوري: تحمل E. coli وL. sakei جين mgsA، في حين أن معظم أقاربها من اللاكتية لا يحملونه. عندما أدخل الباحثون جين mgsA من L. sakei إلى سلالة غير منتجة، بدأت تلك البكتيريا المهندَسة بإنتاج كل من MGO والقلويدات، رابطين بذلك بشكل قاطع بين MgsA وهذا المسار.
كيف يتحول MGO السام إلى قلويدات نشطة حيوياً
السؤال التالي كان ماذا يحدث لـMGO بعد تكوينه. ركّز الفريق على قلويدات 1‑أسيتيل‑β‑كاربولين (ACE‑βCs)، وهي جزيئات صغيرة أُبلغ عن أن لها نشاطات مضادة للميكروبات ومضادة للالتهاب ومضادة للسرطان. أظهروا أنه عندما نمت البكتيريا المولّدة لـMGO في وجود الحمض الأميني إل‑تريبتوفان، ارتفعت مستويات اثنين من ACE‑βCs—1‑أسيتيل‑β‑كاربولين وصيغته الحمضية الكربوكسيلية في الموضع 3—بشكل حاد. كما أن إضافة MGO إضافي إلى الوسط عزز تكوّنها. يشير ذلك إلى أن MGO يتسرب من الخلايا ويتفاعل تلقائياً مع إل‑تريبتوفان في السائل المحيط، بدون حاجة لإنزيمات إضافية، لتوليد هذه المركبات النشطة حيوياً. بعبارة أخرى، الكيمياء نفسها التي تجعل MGO خطيراً تحوّله أيضاً إلى جزيئات أكثر تعقيداً قد يكون لها آثار مفيدة.
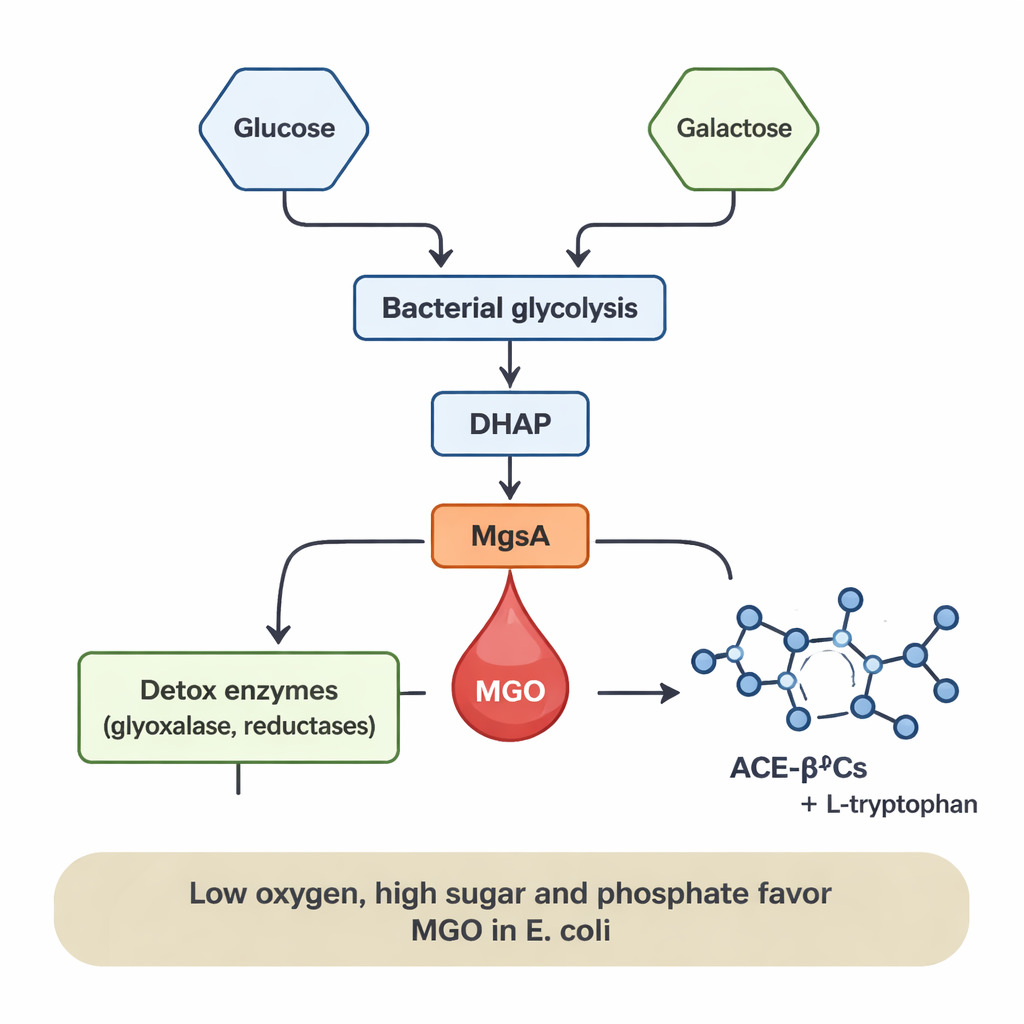
ما الذي يضبط مستوى الإنتاج
لم يكن إنتاج MGO ثابتاً؛ بل اعتمد بشكل قوي على غذاء البكتيريا وبيئتها. في E. coli، ظهر MGO فقط عندما كان الجلوكوز موجوداً، وارتفعت مستوياته مع زيادة تركيز الجلوكوز. كما أن إضافة الفوسفات، وهو مغذٍ معدني شائع، عزّز تكوّن MGO بعدة أضعاف، على الأرجح لأنه يشجّع تراكم وسائط السكر المفسفرة التي تتغذى على اختصار MgsA. كما أن الظروف منخفضة الأكسجين (لاهوائياً)—المماثلة لتلك في الأمعاء البشرية—فضّلت إطلاق MGO، في حين خفّضت الظروف عالية الأكسجين والمهوّاة مستواه بشكل حاد على الرغم من أن البكتيريا ظلت تنمو جيداً. بالمقابل، أنتجت L. sakei MGO أساساً عند النمو على الغالاكتوز، وزاد الإنتاج مع ارتفاع مستويات الغالاكتوز. تشير هذه الأنماط إلى أنه كلما كان تدفّق السكريات عبر أيض البكتيريا عالياً والأكسجين محدوداً، يمكن أن يعمل MGO كـ«صمام ضغط» يخفّف توتّر تراكم وسائط السكر.
ما الذي يعنيه هذا للأغذية والصحة
تشير النتائج إلى أن ليس كل البكتيريا المعوية أو الغذائية متساوية في قدرتها على تكوين MGO وACE‑βCs. الأنواع التي تحمل إنزيم MgsA، مثل سلالات معينة من L. sakei وE. coli، قد تكون مساهمات مهمة، خصوصاً في بيئات غنية بالسكريات ومنخفضة الأكسجين مثل الأمعاء أو بعض عمليات التخمر. قد يضيف MGO الذي تفرزه هذه البكتيريا إلى العبء الكيميائي الكلّي على أنسجة العائل، لكن تحويله إلى قلويدات ACE‑βC قد يساهم أيضاً جزئياً في «التقاط» هذا المركب التفاعلي مع توليد جزيئات لها آثارها البيولوجية الخاصة. وعلى الرغم من أن هذه الدراسة أُجريت في مزروعات مخبرية، فهي تبرز مساراً معقولاً يمكن من خلاله أن تشكّل التغذية وتركيب الميكروبيوتا وأيض البكتيريا معاً التوازن بين المواد الضارة وربما المفيدة في أجسامنا، وتشير إلى ACE‑βCs كعلامات محتملة لإنتاج MGO البكتيري في الأطعمة والأمعاء.
الاستشهاد: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
الكلمات المفتاحية: ميكروبيوتا الأمعاء, ميثيلغلايوكسال, الأيض البكتيري, تخمّر الأغذية, قلويدات بيتا‑كاربولين