Clear Sky Science · ar
اللاكتات ينظم محور YTHDF2‑FTH1 لتعزيز الفيروبتوزيس في خلايا عضلة القلب وتفاقم إصابة نقص التروية وإعادة التروية القلبية
لماذا ينبغي لمرضى القلب أن يهتموا بهذه الكيمياء
عندما يعيد الأطباء فتح شريان قلبي مسدود بعد نوبة قلبية، فإن تدفق الدم الطازج ينقذ النسيج لكنه قد يسبب أيضاً ضرراً إضافياً يعرف باسم إصابة نقص التروية–إعادة التروية. تكشف هذه الدراسة عن سبب غير متوقع داخل خلايا القلب: ناتج أيضي شائع هو اللاكتات. يظهر الباحثون أن اللاكتات يمكنه تعديل مفتاح جزيئي يدفع خلايا القلب نحو نوع محدد من الموت الخلوي المدفوع بالحديد، مما يزيد من شدة الضرر. قد تشير معرفة هذا المسار الخفي إلى عقاقير جديدة تحمي القلب بشكل أفضل أثناء العلاج الطارئ.
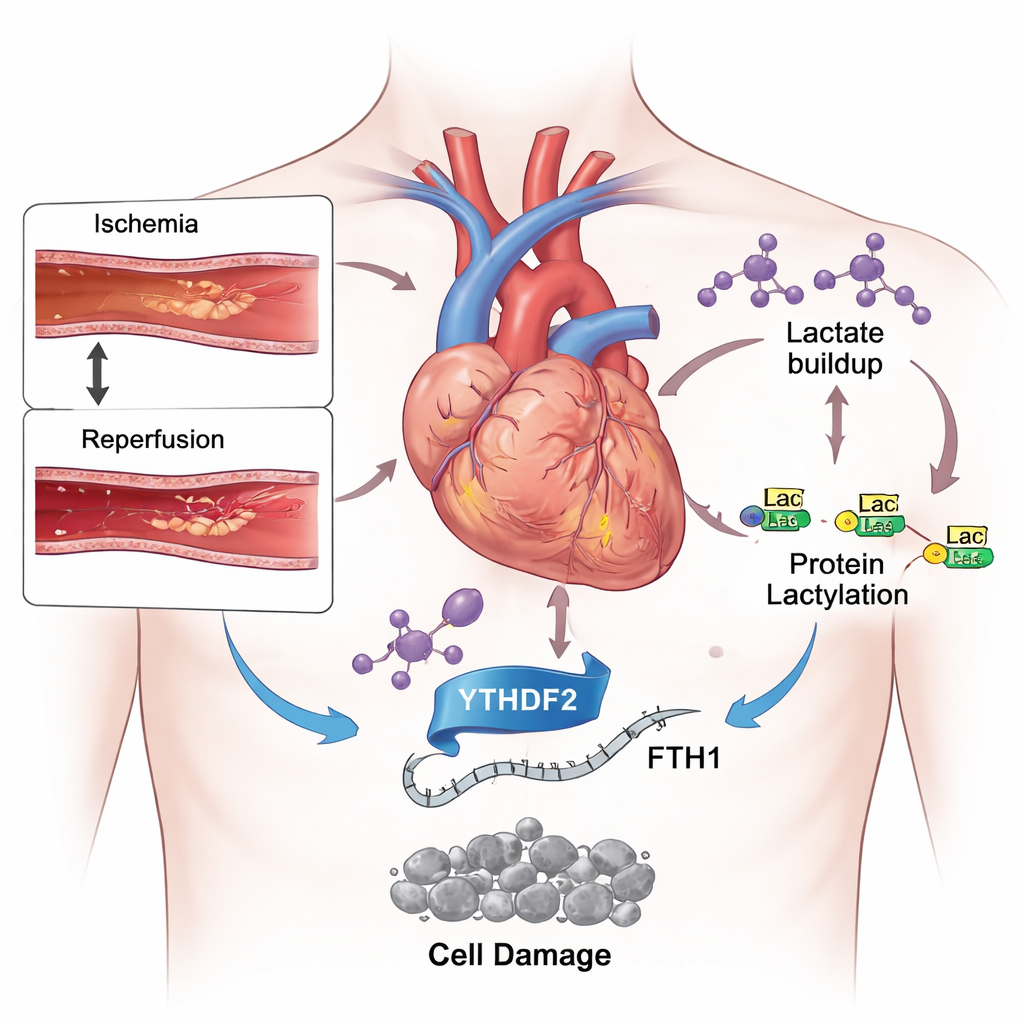
سيف ذو حدين في علاج النوبة القلبية
أصبحت الطب الحديث جيداً جداً في إعادة فتح الشرايين التاجية المسدودة بسرعة، مما يحد من الضرر الأولي الناتج عن النوبة القلبية. ومع ذلك قد يفقد المرضى مساحات كبيرة من نسيج القلب بعد استعادة تدفق الدم. أحد الأسباب هو أن عودة الأكسجين والمغذيات فجأة تخلق عاصفة من الضغوط الكيميائية داخل خلايا القلب. من بين عدة أنماط للموت الخلوي تحفز في هذا السياق، استحوذ نوع أحدث يسمى الفيروبتوزيس على الاهتمام. على خلاف أشكال أكثر ألفة مثل الموت المبرمج (الأبوبتوزيس)، يعتمد الفيروبتوزيس على الحديد والأكسدة المفرطة للدهون في أغشية الخلايا، مما قد يضعف القلب بشكل دائم.
كيف يصبح اللاكتات أكثر من مجرد «حرق العضلات»
خلال النوبة القلبية، تتحول عضلة القلب الجائعة إلى الاعتماد على التحلل السكري، وهو نظام احتياطي يكسر السكر بسرعة لكنه ينتج كميات كبيرة من اللاكتات. باستخدام فئران خضعت لانسداد قصير ثم إعادة فتح لشريان قلبي، وخلايا شبيهة بخلايا القلب مزروعة وتعرضت لنقص الأكسجين ثم استعادة الأكسجة، وجد الباحثون ارتفاعاً حاداً في مستويات اللاكتات. في الوقت نفسه، اكتشفوا مزيداً من الوسم الكيميائي المسمى لاكتيلاتيون على العديد من البروتينات وعلى الهستونات، وهي هياكل تنظم الحمض النووي. عندما أعطوا الحيوانات دواءً يبطئ التحلل السكري ويقلل إنتاج اللاكتات، تقلص الضرر القلبي، انخفضت مؤشرات الدم للضرر، وتحسنت الموازنة بين الحديد الضار ومضادات الأكسدة الواقية. تشير هذه النتائج إلى أن اللاكتات الزائد ليس مجرد ناتج عن الإجهاد بل عامل نشط يسبب الضرر.
مفتاح جزيئي يخفف قيود الحديد
بتعمق أكثر، ركز الفريق على YTHDF2، بروتين يقرأ الوسوم الكيميائية على الرنا ويقرر سرعة تدمير رسائل معينة. اكتشفوا أن نقص التروية–إعادة التروية واللاكتات المضافة كلاهما عززا مستويات YTHDF2 وزادا لاكتيلاتيون حول الجين الذي يشفره، معززين إنتاجه. تبين أن واحداً من الأهداف الرئيسية لـ YTHDF2 هو رنا سلسلة الفيريتين الثقيلة 1 (FTH1)، جزء أساسي من قفص تخزين الحديد داخل الخلية. عادةً يخزن FTH1 الحديد في شكل آمن، مما يمنعه من تغذية التفاعلات الضارة. في خلايا القلب المضغوطة، ارتبط YTHDF2 بقوة أكبر برنا FTH1 وسرع من تحلله، تاركاً الخلايا بعدد أقل من أقفاص الفيريتين، ومزيداً من الحديد الحر، وزيادة في الإجهاد التأكسدي، وعلامات كلاسيكية للفيروبتوزيس.
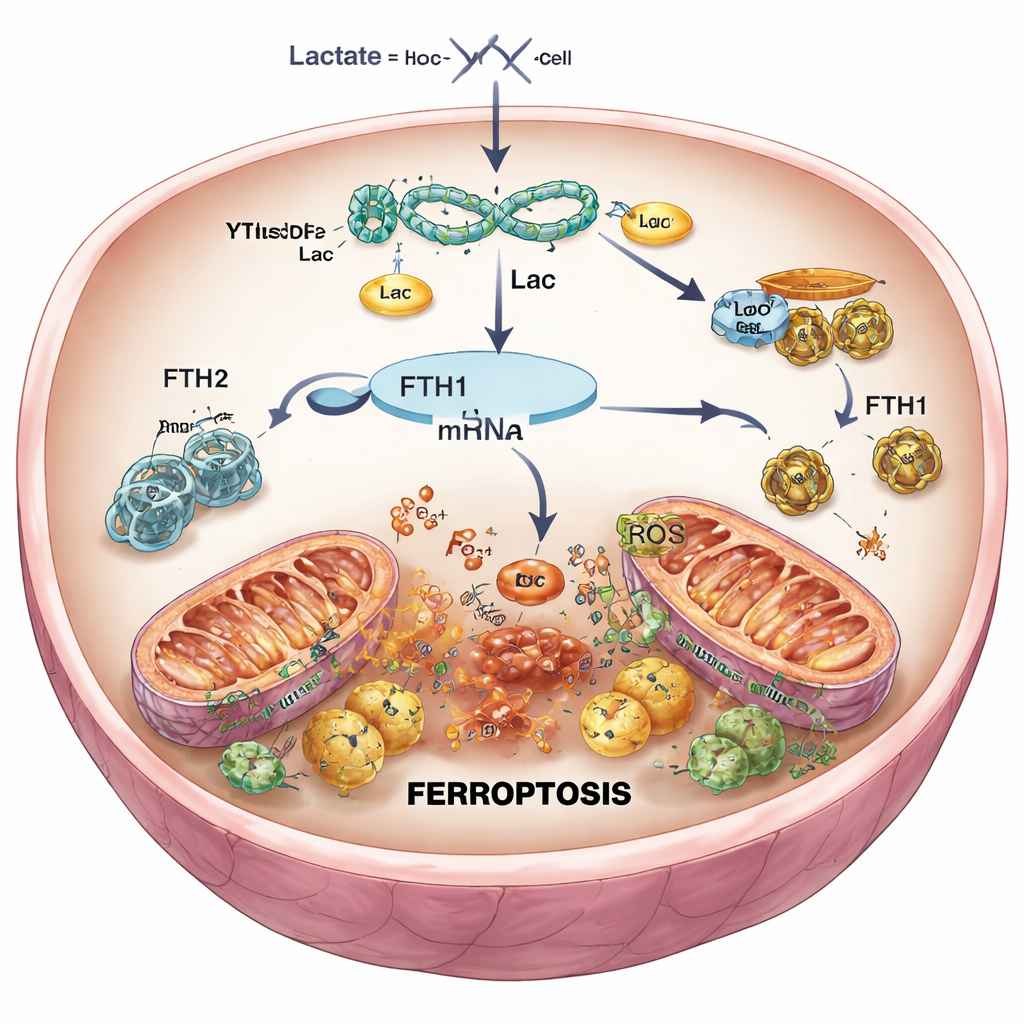
خفض إشارة الموت في خلايا القلب
لاختبار السببية، استخدم الباحثون أدوات جينية لتقليل YTHDF2 انتقائياً في خلايا القلب وفي الفئران. عندما تم قمع YTHDF2، عادت مستويات FTH1 للارتفاع، انخفض الحديد وجذور الأكسجين التفاعلية، وحافظت الميتوكوندريا على شكل أقرب للطبيعي، وتحسنت بقاء الخلايا بعد محاكاة إعادة التروية. في الفئران، أدى انخفاض YTHDF2 إلى تندبات أصغر ونسج تبدو أكثر صحة. ومع ذلك، عندما تم تقليل FTH1 في الوقت نفسه، اختفت هذه الفوائد إلى حد كبير: ارتفع الحديد مجدداً، عادت الأضرار التأكسدية، وتزايد حجم النخر القلبي. هذا أكد أن YTHDF2 يعزز الفيروبتوزيس بشكل رئيسي عن طريق قمع FTH1، مرفوعاً قيود التحكم في الحديد داخل خلايا القلب.
ماذا يعني هذا لعلاجات القلب المستقبلية
بجمع الأجزاء معاً، ترسم الدراسة سلسلة جديدة من الأحداث: انسداد ثم إعادة فتح الشريان يسبب تراكم اللاكتات؛ اللاكتات تزيد YTHDF2 عبر اللاكتيلاتيون؛ ثم يقوم YTHDF2 بتدمير توجيهات الرنا للبروتين الحارس للحديد FTH1؛ والحمولة الحديدية الناتجة تحفز الفيروبتوزيس، مما يعمق الضرر القلبي. للمرضى، الرسالة مفعمة بالأمل: يقدم هذا المسار عدة نقاط تدخل جديدة. قد تجعل أدوية تقلل إشارة اللاكتات الضارة، أو تحجب التعديل المحدد لـ YTHDF2، أو تحافظ على وظيفة FTH1 إعادة التروية الطارئة أكثر أماناً وتحمي المزيد من نسيج القلب. وبينما لا تزال هذه النتائج بحاجة إلى تأكيد في أنسجة بشرية، فإنها تفتح مساراً واعداً نحو علاجات ألطف وأكثر فعالية لباقي نازلي النوبة القلبية.
الاستشهاد: Xiang, Z., Xiang, B., Ouyang, T. et al. Lactate regulates the YTHDF2-FTH1 axis to promote cardiomyocyte ferroptosis and aggravate myocardial ischemia-reperfusion injury. Sci Rep 16, 4865 (2026). https://doi.org/10.1038/s41598-026-35130-3
الكلمات المفتاحية: النوبة القلبية, اللاكتات, الموت الخلوي المدفوع بالحديد, إصابة نقص التروية وإعادة التروية, حماية خلايا القلب