Clear Sky Science · ar
نماذج تعلّم عميق مدمجة لعلم الأمراض المجهري للقولون مع التركيز على تحديات الأداء والتعميم
لماذا يهم هذا البحث للمرضى والأطباء
يعد سرطان القولون أحد أكثر السرطانات فتكًا في العالم، ومع ذلك يظل تشخيصه معتمدًا على خبراء يفحصون صور المجهر للنسيج بدقة، وهي مهمة بطيئة وعرضة للاختلاف في الرأي. تستقصي هذه الدراسة ما إذا كانت نماذج ذكاء اصطناعي صغيرة جدًا وفعالة قادرة على تمييز نسيج القولون السرطاني بدقة كافية لتكون مفيدة في العيادات اليومية، بما في ذلك تلك ذات قدرات حاسوبية محدودة. كما تكشف عن نقطة ضعف مخفية: نماذج قد تبدو مثالية أثناء التطوير قد تتعثر بشدة عند مواجهة بياناتٍ جديدة من العالم الحقيقي.
تعليم الحواسيب لقراءة صور المجهر
عند أخذ خزعة من القولون، يفحص أخصائيو الأمراض شرائح رقيقة ملطخة من النسيج تحت المجهر. يظهر النسيج السرطاني غددًا مشوهة، وأشكال خلايا غير منتظمة، وغزوًا للهياكل المحيطة، بينما يتمتع النسيج السليم بأنماط منتظمة ومنظمة. استخدم الباحثون مجموعة عامة مكونة من 24,000 صورة رقمية لمثل هذه الشرائح، مقسمة بالتساوي بين السرطان (سرطان غدّي للقولون) والنسيج الحميد. أعادوا تحجيم جميع الصور إلى تنسيق صغير موحد وطبقوا تحسينات واقعية — تدويرات صغيرة، انعكاسات، تكبيرات، وتغييرات لونية لطيفة — لمحاكاة التباينات الطبيعية في كيفية قطع الشرائح واصطباغها ومسحها ضوئيًا. تساعد هذه المعالجة الدقيقة نماذج الذكاء الاصطناعي على التركيز على أنماط النسيج المهمة بدلاً من التفاصيل السطحية مثل الاتجاه أو السطوع الدقيق.
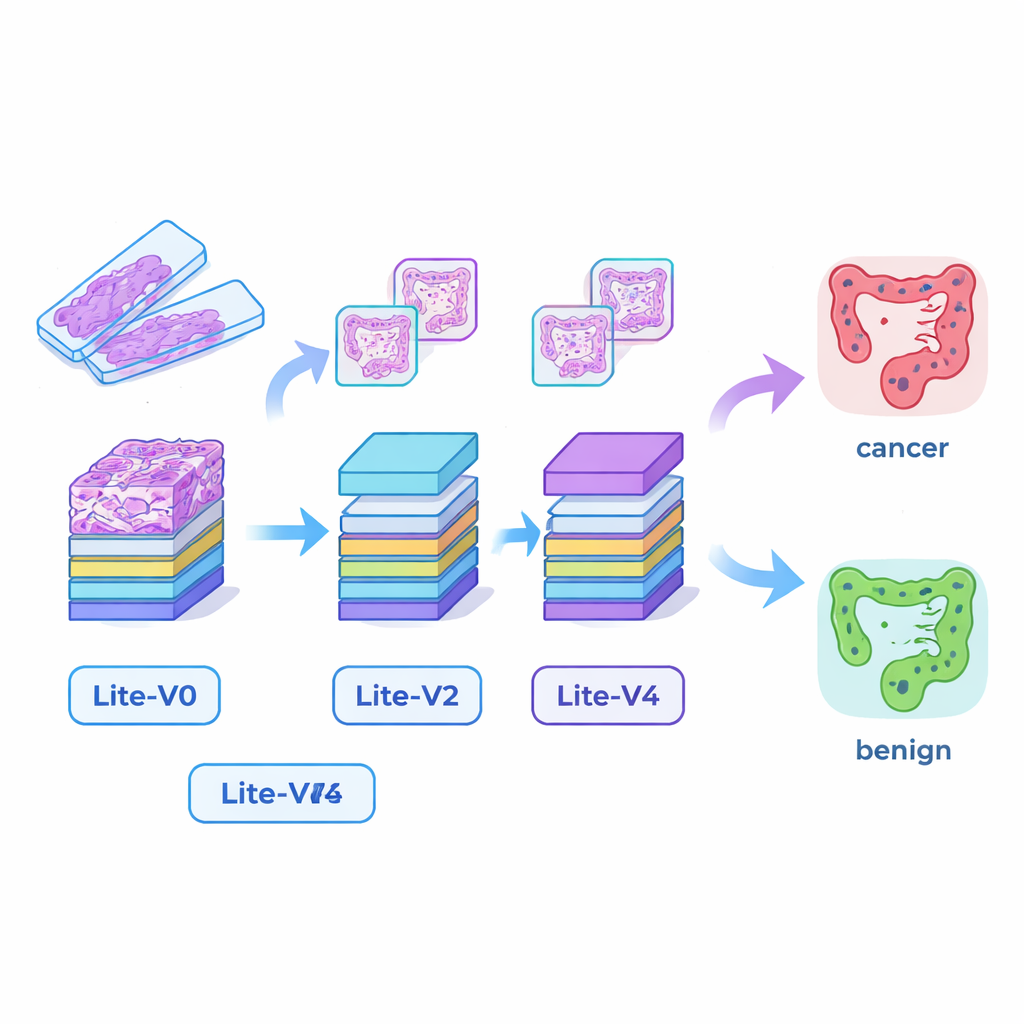
بناء «عيون» ذكاء اصطناعي صغيرة لكنها قادرة
تعتمد العديد من أنظمة الذكاء الاصطناعي الطبية الناجحة على نماذج تعلم عميق كبيرة جدًا تتطلب بطاقات رسومية قوية وذاكرة كبيرة، مما يجعل نشرها في مستشفيات أصغر أو بجانب السرير أمراً صعبًا. لسد هذه الفجوة، صمم الباحثون أربع شبكات عصبية التلافيفية مدمجة — Lite‑V0 وLite‑V1 وLite‑V2 وLite‑V4. ينظر كل منها إلى نفس رقع الصور المدخلة، لكنها تختلف في عدد الطبقات والفلاتر التي تستخدمها لاكتشاف ميزات بصرية مثل الحواف والقوام وأشكال الغدد. تشترك النماذج الأربعة في تصميم بسيط وشفاف: كتل مكررة من الالتفاف القياسي، والتطبيع والتجميع، تليها «رأس قرار» صغير يُنتج احتمال أن يكون النسيج سرطانيًا أو حميدًا. كان الهدف قياس مقدار الدقة الممكن استخلاصه من نماذج صغيرة تكفي للتركيب على أجهزة سريرية أساسية.
نتائج مبهرة داخل المختبر
درّب الفريق وقارن بين النماذج الأربعة على تقسيمة ثابتة من مجموعة البيانات، مستخدمين مقاييس مقبولة على نطاق واسع: الدقة، وF1 المتوازن الذي يعطّل الأخطاء في كلا الفئتين بالتساوي، ومصفوفات الالتباس، ومخططات تشخيصية مثل منحنيات ROC ومنحنيات الدقة‑الاستدعاء. برز نموذج متوسط الحجم، Lite‑V2، كنموذج متميز. على الرغم من أنه لا يتجاوز حوالي 1.5 ميغابايت وله ما يقرب من 128,000 معامل قابل للتدريب، فقد حقق أداءً يكاد يكون خالٍ من الأخطاء على مجموعة التحقق الداخلية، مع F1 متوسط يقارب 0.999 وحساسية ونوعية قريبتين من الكمال. بعبارة أخرى، داخل هذا البيئة المحضرة بعناية، كان Lite‑V2 يكاد يميز دائمًا النسيج القولوني السرطاني عن الحميد، مع بقاءه سريعًا وخفيفًا بما يكفي للاستخدام على حواسيب متواضعة.
عندما تكسر التباينات في العالم الحقيقي السحر
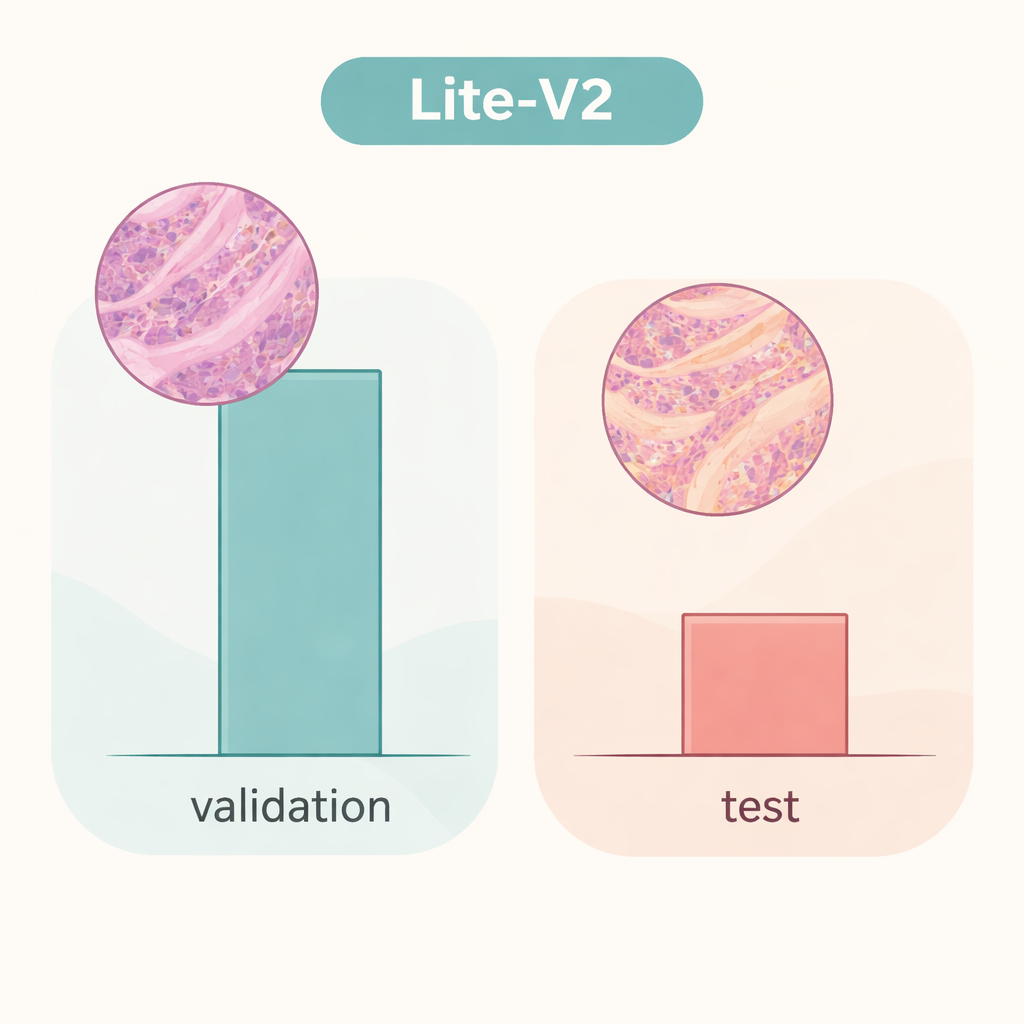
مع ذلك، تتغير القصة بشكل جذري عندما يُختبر نفس نموذج Lite‑V2 على مجموعة صور مستقلة تختلف بطرق دقيقة تحاكي شرائح من مختبر آخر — ما يسميه الباحثون «انزياح المجال». على مجموعة الاختبار غير المرئية هذه، انخفضت الدقة الإجمالية إلى حوالي 50%، وتراجع F1 المتوازن إلى نحو 0.33. استمر النموذج في التعرف على العديد من عينات السرطان لكنه واجه صعوبة بالغة مع النسيج الحميد، مُلصقًا تصنيفًا خاطئًا لجزء كبير منها كخبيث. يبيّن هذا أن الشبكة تعلمت تفاصيل مرتبطة ارتباطًا وثيقًا بمصدر البيانات الأصلي — مثل نمط الصبغة أو خصائص الماسح — بدلاً من توقيعات مرضية متينة وقابلة للنقل. تؤكد الدراسة أن النتائج المتوهجة على التحقق الداخلي قد تعطي إحساسًا كاذبًا بالأمان إذا لم تُختبر النماذج ببيانات مختلفة تمامًا.
ماذا يعني هذا لأدوات التشخيص المستقبلية بالذكاء الاصطناعي
للقارئ العام، الخلاصة ذات شقين. أولًا، يمكن للأنظمة المدمجة فعليًا أن تصل إلى أداء بمستوى الخبراء في صور نسيج القولون بينما تظل صغيرة وفعالة بما يكفي للنشر الواسع، مما يفتح الباب للكشف الأسرع ودعم أخصائيي الأمراض المثقلين بالعمل. ثانيًا، وذا أهمية متساوية، فإن نموذجًا يبدو «مثاليًا» على مجموعة بياناته المحلية قد يتعثر بشدة عند مواجهة صور من مستشفى جديد. يجادل المؤلفون بوجوب تركيز الأعمال المستقبلية على جعل هذه النماذج الخفيفة مقاومة لتغيرات الصبغات والماسحات وخصائص مجموعات المرضى — باستخدام استراتيجيات مثل التدريب المقاوم للاصطباغ، وتكييف المجال، ومجموعات بيانات أوسع متعددة المراكز. وحتى ذلك الحين، ينبغي أن يُنظر إلى الذكاء الاصطناعي كمساعد واعد بدلاً من صانع قرار مستقل في تشخيص السرطان.
الاستشهاد: Hanif, F., Raza, A. & Mohammed, H.A. Compact deep learning models for colon histopathology focusing performance and generalization challenges. Sci Rep 16, 5489 (2026). https://doi.org/10.1038/s41598-026-35119-y
الكلمات المفتاحية: سرطان القولون, علم الأمراض المجهري, التعلّم العميق, شبكات الالتفاف خفيفة الوزن, انزياح المجال