Clear Sky Science · ar
التنقيب في DrugBank باستخدام التعلم الآلي يكشف مرشحين جدد لتثبيط BCL-2
لماذا يُهم العثور على أدوية سرطان أكثر ذكاءً
خلايا السرطان كثيرًا ما ترفض أن تموت عندما يحين الوقت. العديد من الأورام تبقى على قيد الحياة عن طريق الإفراط في استخدام مجموعة من بروتينات "الحراس" المعروفة باسم BCL-2 التي تمنع برنامج الانتحار الداخلي للخلية. هناك أدوية تستهدف BCL-2 بالفعل، لكنها قد تسبب آثارًا جانبية ولا تصلح لكل مريض. تستكشف هذه الدراسة كيف يمكن للتعلم الآلي الحديث أن ينقّب عبر آلاف الأدوية الموجودة للعثور على مرشحين جدد وأكثر أمانًا قد يعطلون BCL-2 ويساعدون خلايا السرطان على الانتحار المبرمج.
كيف تختار الخلايا بين الحياة والموت
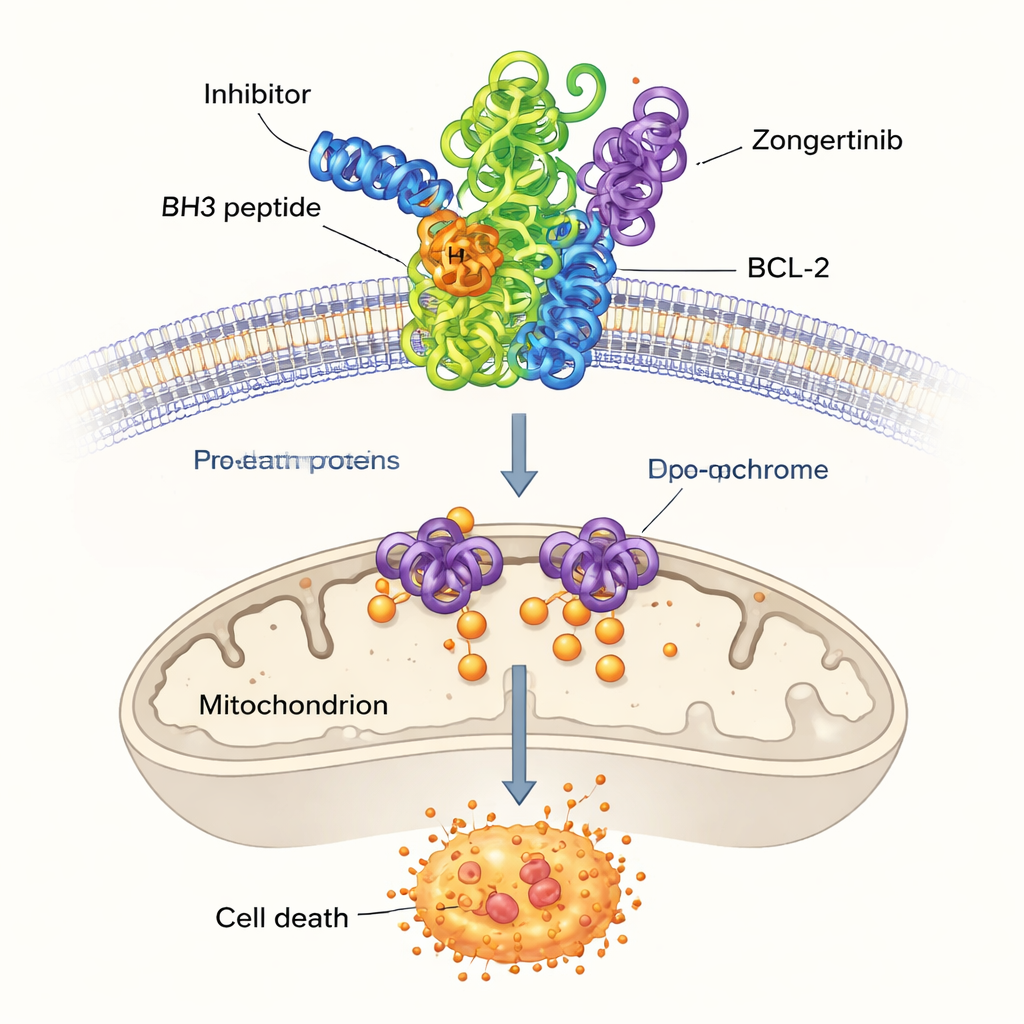
الأنسجة السليمة تتخلص باستمرار من الخلايا التالفة أو غير اللازمة عبر عملية مراقبة للانتحار الذاتي تُعرف بالابوبتوسيس أو الموت المبرمج للخلايا. تعمل مجموعة بروتينات تُسمى عائلة BCL-2 كمفتاح مركزي لهذا القرار. بعض الأعضاء تدفع الخلايا نحو البقاء، بينما يدفعها آخرون نحو الموت. في العديد من السرطانات، تُنتج أعضاء عائلة BCL-2 التي تُعزز البقاء، بما في ذلك BCL-2 وقريبها BCL-XL، بكميات زائدة. هذه الحماية الإضافية تسمح لخلايا السرطان بتجاهل إشارات الموت ومقاومة العلاج الكيميائي. لهذا السبب، أصبح حجب BCL-2 استراتيجية جذابة في علاج السرطان، لكن الأدوية الحالية غالبًا ما تصيب بروتينات ذات صلة أيضًا، مما يؤدي إلى آثار جانبية مثل انخفاض خطير في عدد الصفائح الدموية.
تعليم الحواسيب على التعرف على الجزيئات الواعدة
بدلًا من البحث عن مركبات جديدة من الصفر، لجأ الباحثون إلى قواعد بيانات الجزيئات التي تمت دراستها أو استخدامها كأدوية بالفعل. بدأوا بموارد عامة كبيرة اسمها ChEMBL، التي تحتوي على قياسات تجريبية لقوة ارتباط مركبات مختلفة بـ BCL-2. بعد تنظيف هذه المعلومات بعناية—إزالة التكرارات والقياسات غير المؤكدة والجزيئات الكبيرة أو غير الاعتيادية—توصلوا إلى 601 مركبًا موصوفًا جيدًا. تُرجمت كل جزيئة إلى نوع من البصمة الرقمية التي تلتقط ميزاتها البنائية. استُخدمت هذه البصمات لتدريب ومقارنة سبعة نماذج تعلم آلي مختلفة في مهمة تحديد ما إذا كانت جزيئة جديدة من المحتمل أن تكون مُثبّطًا قويًا لـ BCL-2 أو غير فعالة أساسًا. 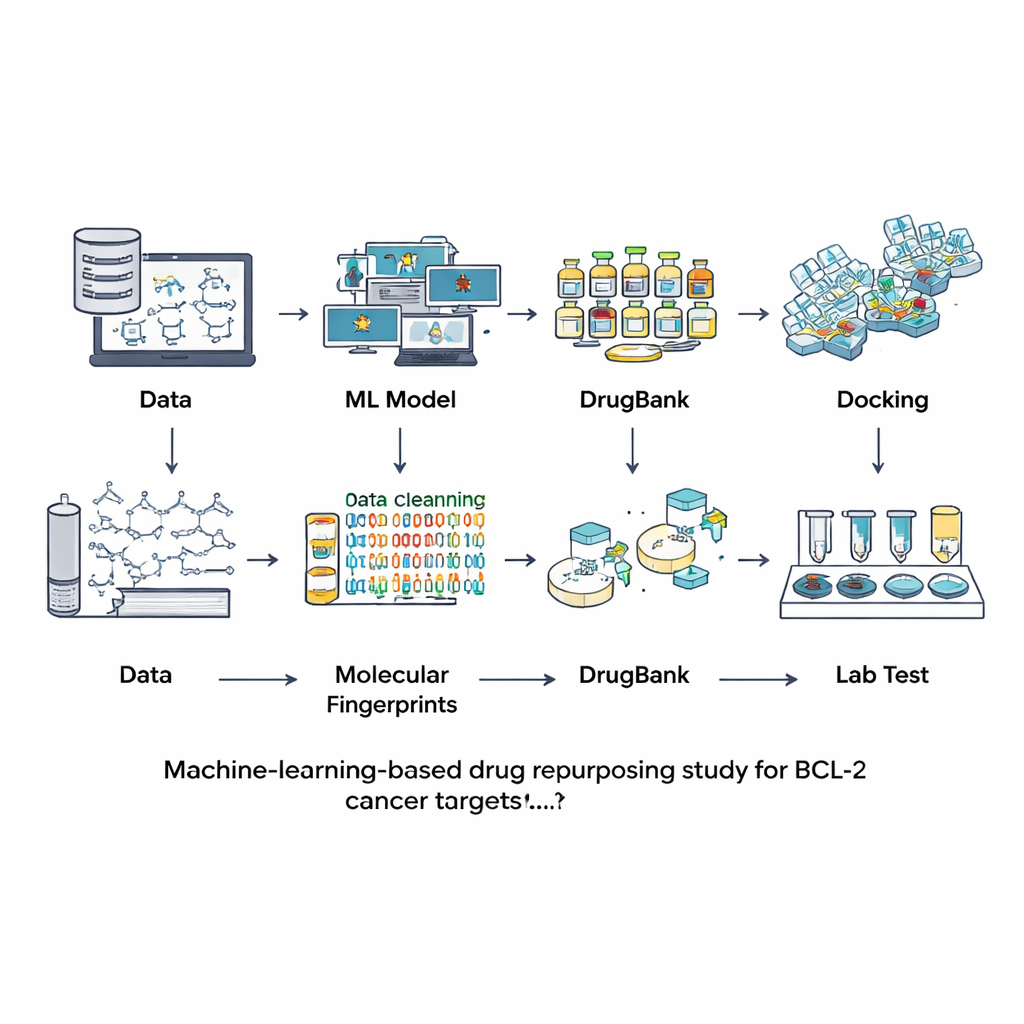
اختيار أفضل نموذج ومسح مكتبة أدوية
قيّم الفريق النماذج باستخدام مجموعة اختبار منفصلة لم تُستخدم أثناء التدريب، مفحصين ليس فقط كم مرة يصيب كل نموذج، بل أيضًا مدى قدرته على التمييز بين النشط والغير نشط ومدى توازن توقعاته. تفوّق نموذج يُدعى LightGBM—وهو طريقة تعزيز أساسها الأشجار حديثة—عبر معظم المقاييس، بما في ذلك الدقة العامة وقدرته على إعطاء احتمالات موثوقة. مع هذا النموذج المضبوط، اتجه الباحثون إلى DrugBank، مجموعة مُنقّحة تضم أكثر من 12,000 دواء مُوافق عليه أو تجريبي أو مسحوب. بعد حساب نفس نوع البصمات، سألوا LightGBM أي من هذه الجزيئات يشبه مرشحات محتملة لـ BCL-2. سجلت تسعة مركبات فقط درجات عالية، أي نحو عُشر واحد بالمئة من المكتبة بأكملها، ممّا أظهر أن الفحص الافتراضي كان انتقائيًا جدًا. كان أربعة من التسعة معروفين بالفعل كمثبطات لـ BCL-2، مما طمأن الفريق إلى صحة النهج.
من النتائج الحاسوبية إلى التفاعلات الجزيئية
من بين الجزيئات مرتفعة الدرجات الباقية، ركز الباحثون على ثلاثة لم تُربط سابقًا بـ BCL-2: Dersalazine وOpelconazole وZongertinib. لمعرفة ما إذا كان بإمكان هذه المرشحين أن تتلاءم بشكل معقول في جيب ارتباط BCL-2، استخدموا التثبيت الجزيئي الحاسوبي (الدوكنج)، وهي تقنية تتنبأ بكيفية احتواء جزيء صغير لسطح البروتين. أشارت المحاكاة إلى أن Opelconazole وZongertinib، على وجه الخصوص، يشكلان شبكات من التلامسات المواتية مع نفس الأحماض الأمينية الرئيسية التي تمسك بدواء مرجعي مدروس جيدًا، ABT-737. كانت قوة الارتباط المتوقعة قريبة من تلك الخاصة بالمثبطات المعروفة، مما يوحي بأن نموذج التعلم الآلي قد اكتشف فعليًا جزيئات قادرة على تعطيل BCL-2.
وضع التنبؤات قيد الاختبار في المختبر
الإشارات الحاسوبية مفيدة فقط إذا ثبتت صحتها في الظروف الواقعية. لذلك اختبر الفريق المرشحين الثلاثة في اختبار بيوكيميائي يقيس مدى قدرة مركب على منع BCL-2 من الارتباط بأحد شركائه الطبيعيين. على مدى تراكيز مختلفة، أظهر Dersalazine تأثيرًا طفيفًا. أما Opelconazole وZongertinib فقللا نشاط BCL-2 عند جرعات عالية، مع اقتراب Opelconazole من إيقاف الإشارة تمامًا. رغم أن هذه التراكيز أعلى مما سيكون مثاليًا لدواء جاهز للاستخدام السريري، إلا أنها تُظهر أن المرشحين يتفاعلون فعلًا مع BCL-2 وتُصادق على سلسلة الاكتشاف التي اتبعها الفريق.
ما يعنيه هذا لعلاجات السرطان المستقبلية
لغير المتخصص، الرسالة الأساسية هي أن الباحثين درّبوا نظامًا حاسوبيًا بنجاح للتعرف على شكل الجزيئات التي تُعيق BCL-2، ثم استخدموه للتنقيب في مكتبة كبيرة من الأدوية والمركبات الشبيهة بالأدوية الموجودة بالفعل. أعاد النهج اكتشاف أدوية معروفة لـ BCL-2 وأبرز مرشحين جددًا، ثبت أن اثنين منهما لهما نشاط مثبّط حقيقي في اختبارات المختبر. وبينما ما يزال هناك الكثير من العمل—تحسين الفعالية، وفهم السلامة، والاختبار في الخلايا والحيوانات—تُظهر هذه الدراسة كيف يمكن للتعلم الآلي والتنقيب الذكي في البيانات أن يسرِّع البحث عن أدوية سرطان أفضل من خلال إعادة استخدام وإعادة تقييم مركبات نعرفها بالفعل.
الاستشهاد: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
الكلمات المفتاحية: مثبطات BCL-2, التعلم الآلي, إعادة توظيف الأدوية, الاستماتة المبرمجة (الابوبتوسيس), علاج السرطان