Clear Sky Science · ar
شبكة عصبية بيانية مُطّعمة بمبادئ فيزيائية لتقريب أفـة الارتباط المبنية على الإرساء لـ DYRK2 في إعادة توظيف أدوية مرض ألزهايمر
لماذا هذا مهم بالنسبة لألزهايمر
يتزايد انتشار مرض ألزهايمر عالمياً، ومع ذلك فإن معظم الأدوية الحالية تخفف الأعراض فقط ولا توقف المرض. اختبارات الأدوية الجديدة في المختبر بطيئة ومكلفة، خاصةً للبروتينات الدماغية الأقل شهرة التي قد تكون مهمة للذاكرة وصحة الأعصاب. تبحث هذه الدراسة في اختصار ذكي: استخدام نموذج ذكاء اصطناعي واعٍ بالفيزياء للتنبؤ بمدى تمسك أدوية ألزهايمر الحالية ببروتين غير مدروس جيداً يدعى DYRK2، ما قد يفتح مسارات علاجية جديدة.
طريقة جديدة لمعالجة أدوية قديمة
بدلاً من تصميم مركبات جديدة من الصفر، يركز الباحثون على إعادة توظيف الأدوية—إيجاد استخدامات جديدة لأدوية معتمدة ومعروفة نسبياً بأمانها. يفحصون أربعة أدوية مألوفة لعلاج ألزهايمر (بريكسبيبرازول، دونيبيزيل، جالانتامين، وريفاستيغمين) ويتساءلون عن مدى إحكام ارتباط كلٍ منها ببروتين DYRK2، وهو كيناز بروتيني يشارك في نمو ووظيفة الخلايا العصبية. لم يُدرس DYRK2 كثيراً في سياق ألزهايمر، لكن أدلة مبكرة تربطه بالمشبكات المشبكية والمحاور والذاكرة، مما يجعله هدفاً مثيراً للاهتمام قد يكمل العلاجات الحالية.
تحويل الجزيئات إلى شبكات
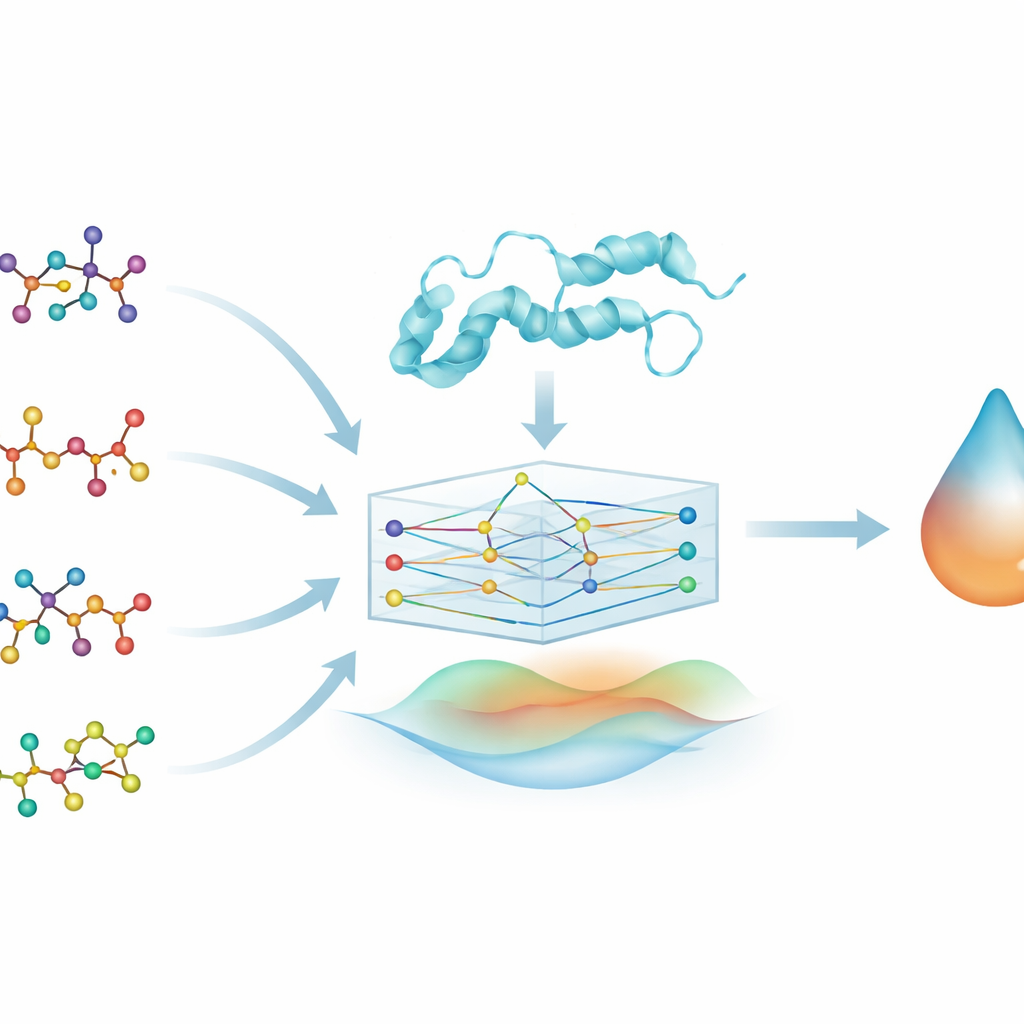
لاستكشاف علاقات الدواء–البروتين هذه، يحول الفريق كل جزيء دوائي إلى رسم بياني: تصبح الذرات نقاطاً والروابط الكيميائية خطوطاً تربط بينها. يفعلون شيئاً مماثلاً لبروتين DYRK2، ممثلين تسلسل الأحماض الأمينية كسلسلة من الوحدات المترابطة. نوع من نماذج التعلم الآلي يدعى الشبكة العصبية البيانية (GNN) يتعامل طبيعياً مع هذه المدخلات ذات الشكل البياني، وينقل المعلومات عبر الاتصالات ليتعلم أنماط الشكل والكيمياء. هذا يمكّن النموذج، المسمى PhysDual‑GCN، من «قراءة» الدواء وDYRK2 كشبكتين متفاعلتين بدلاً من سلاسل أو قوائم ميزات بسيطة.
دمج الفيزياء مع الذكاء الاصطناعي
معظم أدوات التعلم العميق في اكتشاف الأدوية تتعلم فقط من البيانات، مما قد يجعل آليات عملها الداخلية صعبة الفهم. هنا، يدمج المؤلفون عمداً أفكاراً فيزيائية أساسية حول كيفية تفاعل الذرات. إلى جانب الميزات المتعلمة من الرسم البياني، يحسب PhysDual‑GCN مقدارين طاقيين كلاسيكيين: واحد يلتقط التجاذب والتنافر الكهربائي بين الشحنات الجزئية، وآخر يصف قوى فان دير فالس من دفع وجذب. تدمج هذه الطاقات المستندة إلى الفيزياء مع التمثيل الداخلي للشبكة العصبية قبل أن يعطي مخرجاته المتنبئة بقوة الارتباط. بفاعلية، يتدرب النموذج على محاكاة سلوك برامج الإرساء الكلاسيكية—وخاصة AutoDock Vina والأدوات ذات الصلة—لكن بسرعة أكبر، مع البقاء مُرتكزاً على مبادئ فيزيائية مألوفة.
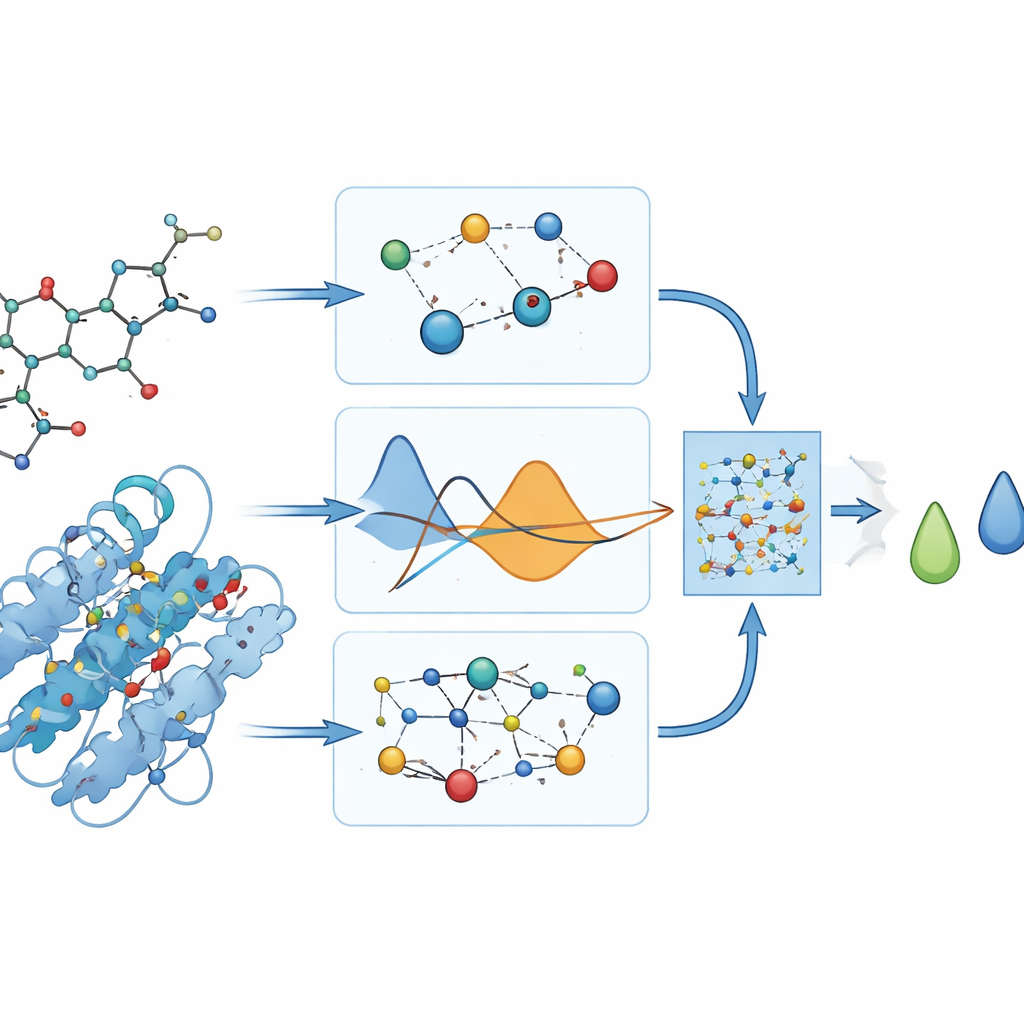
ما الذي يتنبأ به النموذج في الواقع
لأنه لا توجد قياسات مخبرية لمدى ارتباط هذه الأدوية بـ DYRK2، يعتمد المؤلفون على برامج الإرساء لتوفير درجات «مرجعية» لارتباطها بوحدات الطاقة. يتجنبون بعناية إدخال تلك الدرجات ضمن عملية التدريب، ويستخدمونها لاحقاً فقط لتقييم مدى تعلم PhysDual‑GCN. بالنسبة للأربعة أدوية، يعيد النموذج إنتاج قيم الإرساء بأخطاء متوسطة صغيرة (حوالي ثلث كيلو كالوري لكل مول) ويصنف المركبات بشكل صحيح: يظهر أن دونيبيزيل وبريكسبيبرازول هما الأقوى ارتباطاً، بينما يبدو أن جالانتامين وريفاستيغمين أضعف لكن لا تزال مستقرة نسبياً. تظهر هذه النتائج أن الشبكة العصبية البيانية الموجهة بالفيزياء يمكن أن تحل محل الإرساء التقليدي حسابياً في حالات البيانات المحدودة.
الوعود وحدود النهج
رغم هذه الأرقام المشجعة، يؤكد المؤلفون أن دراستهم لها حدود صارمة. فُحصت أربعة أدوية فقط، وتعتمد جميع التقييمات على برامج حاسوبية أخرى بدلاً من تجارب بيوكيميائية حقيقية. يُنمذج بروتين DYRK2 في المقام الأول كرسم بياني أحادي البعد للتسلسل، لا كهيكل ثلاثي الأبعاد كامل، لذا لا يستطيع النموذج حتى الآن أخذ شكل جيوب الارتباط التفصيلي بعين الاعتبار. الطاقات الفيزيائية نفسها مبسطة، باستخدام معلمات حقول قوى وقطع معيارية قياسية. نتيجة لذلك، ينبغي اعتبار العمل إثبات مبدأ: إنه يظهر أن الشبكات العصبية البيانية الموجهة بالفيزياء يمكنها متابعة درجات الإرساء الكلاسيكية عن قرب في بيئة بيانات منخفضة، لكنه لا يثبت بعد أن التنبؤات تطابق الواقع في المختبر أو العيادة.
ما الذي يعنيه هذا لأبحاث ألزهايمر المستقبلية
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن الخوارزميات الذكية الواعية بالفيزياء قد تساعد العلماء على استكشاف أهداف ألزهايمر جديدة مثل DYRK2 بسرعة أكبر بكثير من الطرق التقليدية وحدها. من خلال إبراز دونيبيزيل وبريكسبيبرازول كمرشحين واعدين للارتباط بـ DYRK2 وتقديم طريقة شفافة لتقريب نتائج الإرساء، يوفر PhysDual‑GCN نقطة انطلاق للدراسات المخبرية الأعمق. مع مكتبات أدوية أكبر، ومعلومات بروتينية ثلاثية الأبعاد أغنى، والتحقق التجريبي، قد يصبح هذا النوع من النماذج أداة عملية لفحص العلاجات المرشحة وتوجيه جهود إعادة توظيف الأدوية الرامية إلى إبطاء أو تغيير مسار مرض ألزهايمر.
الاستشهاد: Gider, V., Budak, C. A physics-informed graph neural network to approximate docking-based binding affinity for DYRK2 in Alzheimer’s drug repurposing. Sci Rep 16, 8357 (2026). https://doi.org/10.1038/s41598-026-35102-7
الكلمات المفتاحية: مرض ألزهايمر, إعادة توظيف الأدوية, الشبكات العصبية البيانية, ارتباط البروتين–الرابط, كيناز DYRK2