Clear Sky Science · ar
البنية البلورية لـ Echinococcus multilocularis cystatin B تكشف ميزة جديدة في الستيفينات الكلاسيكية
لماذا تهم أداة سريّة لطفيلي كبدي
داء الاستسقاء الكيسي الرئوي اسم طويل لعدوى دودة شريطية صغيرة تتصرف كثيراً مثل ورم ينمو ببطء في الكبد. غالباً ما تكون مميتة، والأدوية الحالية ضعيفة الفاعلية وقد تسبب آثاراً جانبية خطيرة. تدرس هذه الدراسة جزيئاً محدداً تصنعه الطفيلي، وهو بروتين يُدعى EmCystatin-B، لفهم كيف قد يساعد الدودة على التهرب من دفاعاتنا—وكيف يمكن أن يُستغل يوماً ما كهدف لعلاجات جديدة.
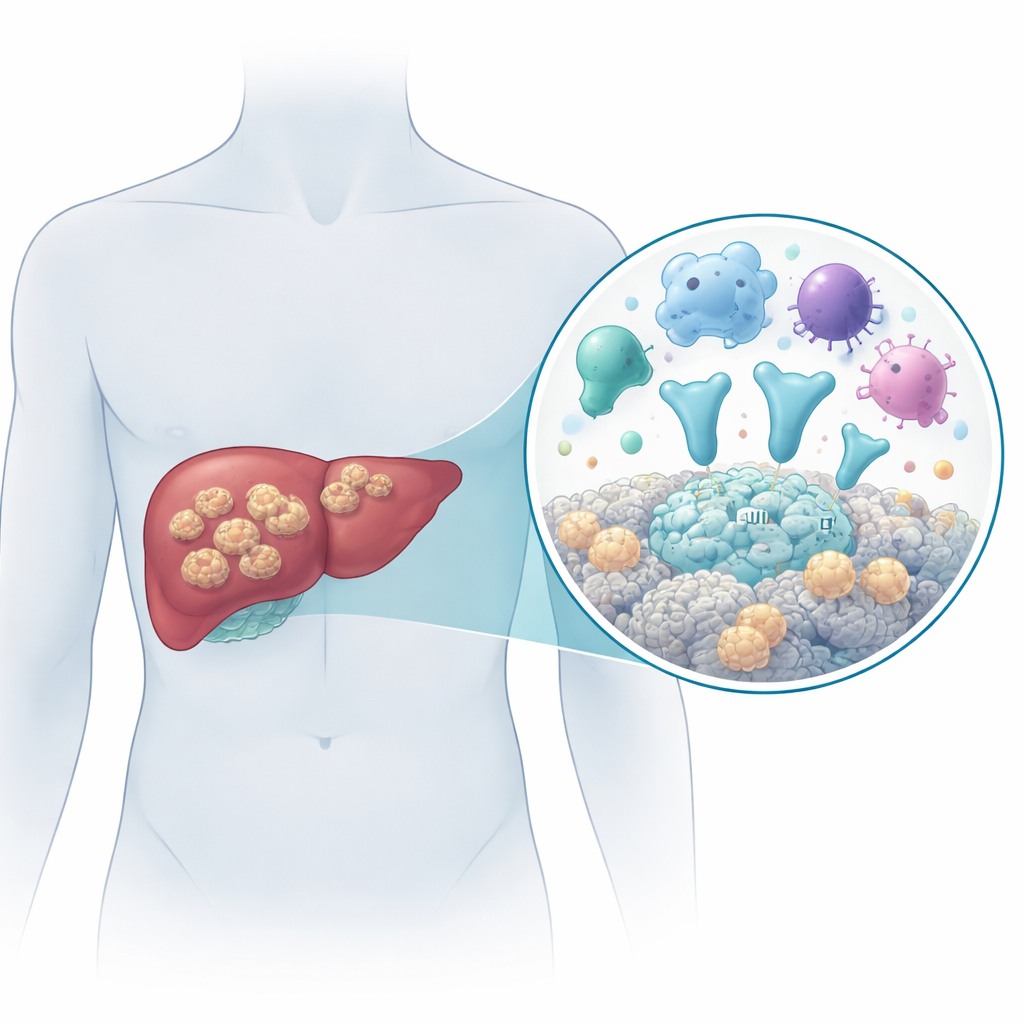
دودة شريطية خطيرة تنمو كورم
يسبب المرض الطور اليرقي للدودة الشريطية Echinococcus multilocularis. يُصاب الناس عن طريق ابتلاع بيض الطفيلي عن طريق الخطأ، على سبيل المثال في طعام أو ماء ملوث. بمجرد دخولها الجسم، تستقر اليرقات أساساً في الكبد وتُكوّن العديد من الأكياس الصغيرة المملوءة بالسائل التي تغزو الأنسجة المحيطة، وتمتد إلى أعضاء مجاورة مثل الطحال، وأحياناً تصل إلى مواقع بعيدة مثل الرئتين أو الدماغ. من دون علاج فعال، يموت أكثر من 9 من كل 10 مرضى خلال 10 إلى 15 سنة. تُعد الجراحة مع أدوية مضادة للطفيليات طويلة الأمد الخيار الأفضل حالياً، لكن التشخيص المبكر صعب والأدوية لا تضمن شفاء العدوى. لذلك من الضروري فهم كيفية تفاعل الطفيلي مع جسم الإنسان على المستوى الجزيئي.
بروتين طفيل يعرقل إنزيمات القطع
تصنع العديد من الحيوانات، بما في ذلك البشر، عائلة من البروتينات تسمى السيستاتينات التي تعمل كأقفال أمان على إنزيمات هضمية قوية تعرف بالبروتيازات المحتوية على السيستين. يمكن لهذه الإنزيمات أن تقطع بروتينات أخرى وهي مهمة لعمليات مثل تحلّل مكوّنات الخلايا المتقادمة وتنشيط الاستجابات المناعية. تعلم الطفيليات تصنيع بروتينات شبيهة بالسيستاتين للتداخل مع إنزيمات المضيف وجهازه المناعي. في هذا العمل، حدّد الباحثون بروتين شبيه بالسيستاتين من E. multilocularis وسمّوه EmCystatin-B. وجدوا أن جين EmCystatin-B أكثر نشاطاً بكثير في رؤوس اليرقات الناضجة (البروتوسكوليسات) مقارنة بنسيج الكيس المحيط، وأن البروتين موجود في السيتوبلازم ونواة خلايا الطفيلي، خصوصاً في الخلايا الجرثومية «الشبيهة بالخلية الجذعية» المنقسمة. أظهرت الاختبارات المختبرية أن EmCystatin-B يمكنه حجب نشاط الكاتيبسين B البشري بقوة، وهو بروتياز مهم يشارك في المناعة وإعادة تشكيل الأنسجة.
شكل مألوف مع لمسة غير متوقعة
لمعرفة كيفية بناء EmCystatin-B بالضبط، بلّور الفريق البروتين المنشّط واستخدم بلورة الأشعة السينية لحل بنيته ثلاثية الأبعاد بدقة تقارب الذرية. مثل أعضاء عائلة السيستاتين الأخرى، لكل وحدة من EmCystatin-B شكل مميز: قطعة حلزونية مركزية مدعومة بعدة سلاسل مسطحة تشبه الشريط، مكونة إسفيناً يندمج عادة في الموقع النشط للبروتياز. استناداً إلى تسلسلها وعدم وجود ببتيد إشارة واضح للإفراز، ينتمي EmCystatin-B إلى مجموعة «الستيفينات» من السيستاتينات، وهي عادة بروتينات صغيرة داخل خلوية لا تحتوي على روابط ثنائية الكبريتيد المثبّتة. بشكل مفاجئ، كشفت البنية أنه على الرغم من أن كل وحدة EmCystatin-B تحمل الطيّة المتوقعة، فإن طريقة ارتباط هذه الوحدات ببعضها غير عادية وخاصة بالأنواع مقارنة بالنظير البشري، سيستاتين B.
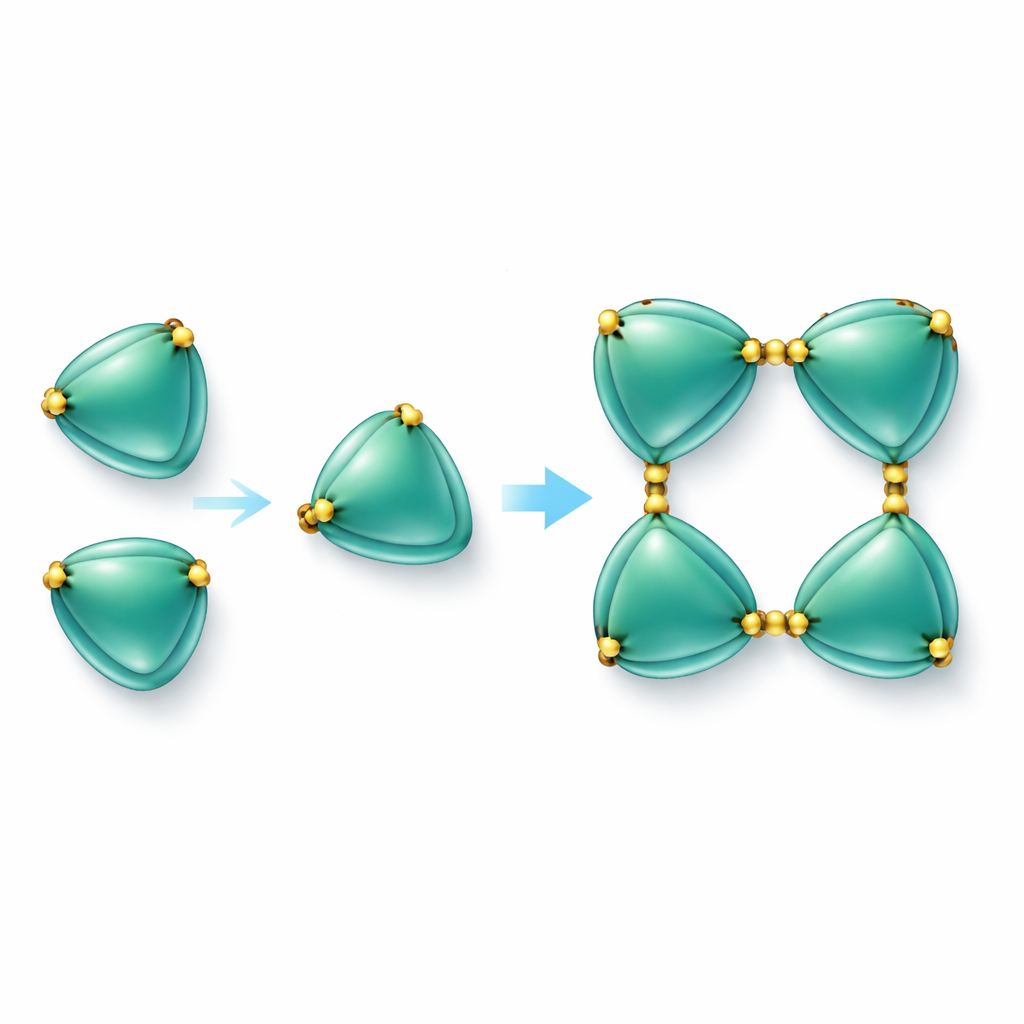
بناء سلاسل البروتين بروابط كبريت
أكثر الاكتشافات لفتاً للانتباه هو أن جزيئات EmCystatin-B لا تطفو ببساطة كوحدات منفردة. بدلاً من ذلك، يمكنها الانضمام معاً خطوة بخطوة لتشكيل ثنائيات (أزواج) ثم رباعيات (مجموعات من أربعة). آليتان مختلفتان تساعدان على تكوين الثنائيات الأولية. في إحداهما، يتأرجح جزء من جزيء فوق ويكمل بنية جاره، ظاهرة تعرف بتبادل النطاقات. وفي الأخرى، تُربط أزواج الجزيئات معاً بجسور ثنائية الكبريتيد—روابط كيميائية قوية بين الأحماض الأمينية المحتوية على الكبريت (السيستئين). في EmCystatin-B، يرتبط السيستئين في الموضع 4 بسيستئين في الموضع 76 لجزيء شريك. ثم تثبت أربعة من هذه الروابط المتبادلة الرباعية. هذا الاستخدام لعدة جسور ثنائية الكبريتيد بين الجزيئات يعد جديداً تماماً للستيفينات الكلاسيكية، التي عادة ما تفتقر لمثل هذه الروابط. عندما غيّر الباحثون هذه السيستئينات الأساسية إلى حمض أميني آخر، لم يعد البروتين قادراً على التجمع بكفاءة إلى مركبات أعلى الرتبة وانخفضت قدرته على تثبيط الكاتيبسين B بشكل حاد.
ماذا يعني ذلك لمحاربة العدوى
بالنسبة لغير المختص، الرسالة هي أن الطفيلي طوّر نسخة مُعاد توصيلها من عائلة بروتينات شائعة، مستخدماً «مسامير» كيميائية إضافية لربط عدة وحدات مثبطة معاً. يبدو أن هذا الشكل المتعدد الوحدات مهم لإخماد إنزيم المضيف الذي كان سيُساعد في السيطرة على العدوى. من خلال الكشف عن البنية الدقيقة لـ EmCystatin-B وتجميعاته الفريدة المرتبطة بثنائيات الكبريتيد، توسع الدراسة فهمنا لكيفية ضبط بروتينات السيستاتين بين الأنواع. على المدى الطويل، قد توجه هذه الرؤى تصميم أدوية إما لمنع تأثير EmCystatin-B الواقي للطفيلي أو لمحاكاة خصائصه المهدئة للمناعة لعلاج الأمراض الالتهابية.
الاستشهاد: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
الكلمات المفتاحية: داء الاستسقاء الكيسي الرئوي, Echinococcus multilocularis, سيستاتين ب, بنية البروتين, تعديل المناعة