Clear Sky Science · ar
تعطيل تجميع مركب الإنفلاماسوم NLRP3 عبر إعادة تشكيل الواجهات في مجال البيرين المحفزة بواسطة الرباط
لماذا يهم تهدئة الالتهاب الخارج عن السيطرة
العديد من الأمراض المزمنة — من التهاب المفاصل والنقرس إلى أمراض القلب والتنكس العصبي — تغذّيها منظومة إنذار مناعية مفرطة النشاط داخل خلايانا. جزء أساسي من هذا الإنذار، المسمى إنفلاماسوم NLRP3، يساعدنا في مكافحة العدوى لكنه قد يسبب التهابًا ضارًا عندما يخطئ في العمل. تصف هذه الدراسة جزيئًا صغيرًا جديدًا، اسمه E9، يستهدف خطوة مبكرة في تنشيط NLRP3، مما يفتح مسارًا جديدًا لتصميم أدوية تبريدية للالتهاب الضار دون إخماد الجهاز المناعي بالكامل.
منبه حريق خلوي له جانب مظلم
عندما تشعر أجسامنا بالخطر، تجمع الخلايا المناعية إنفلاماسوم NLRP3، وهو مركب بروتيني كبير يعمل كمنبه حريق جزيئي. بمجرد تكوّنه، يشغّل هذا الهيكل إنزيمًا يدعى كاسبيز-1، الذي بدوره ينشط مرسلين التهابيين قويين بما في ذلك السيتوكينات IL-1β وIL-18. هذه الإشارات ضرورية لمحاربة العدوى وإزالة الأنسجة المتضررة. لكن إذا ظل الإنفلاماسوم مفعلاً لفترة طويلة أو اشتغل في وقت غير مناسب، يساهم ذلك في حالات التهابية مزمنة تصيب المفاصل والأوعية الدموية والدماغ وأعضاء أخرى. لهذا السبب يبحث الباحثون حول العالم عن طرق دقيقة للتحكم بـNLRP3 دون قمع المناعة على نحو واسع.
البحث خارج أهداف الأدوية المعتادة
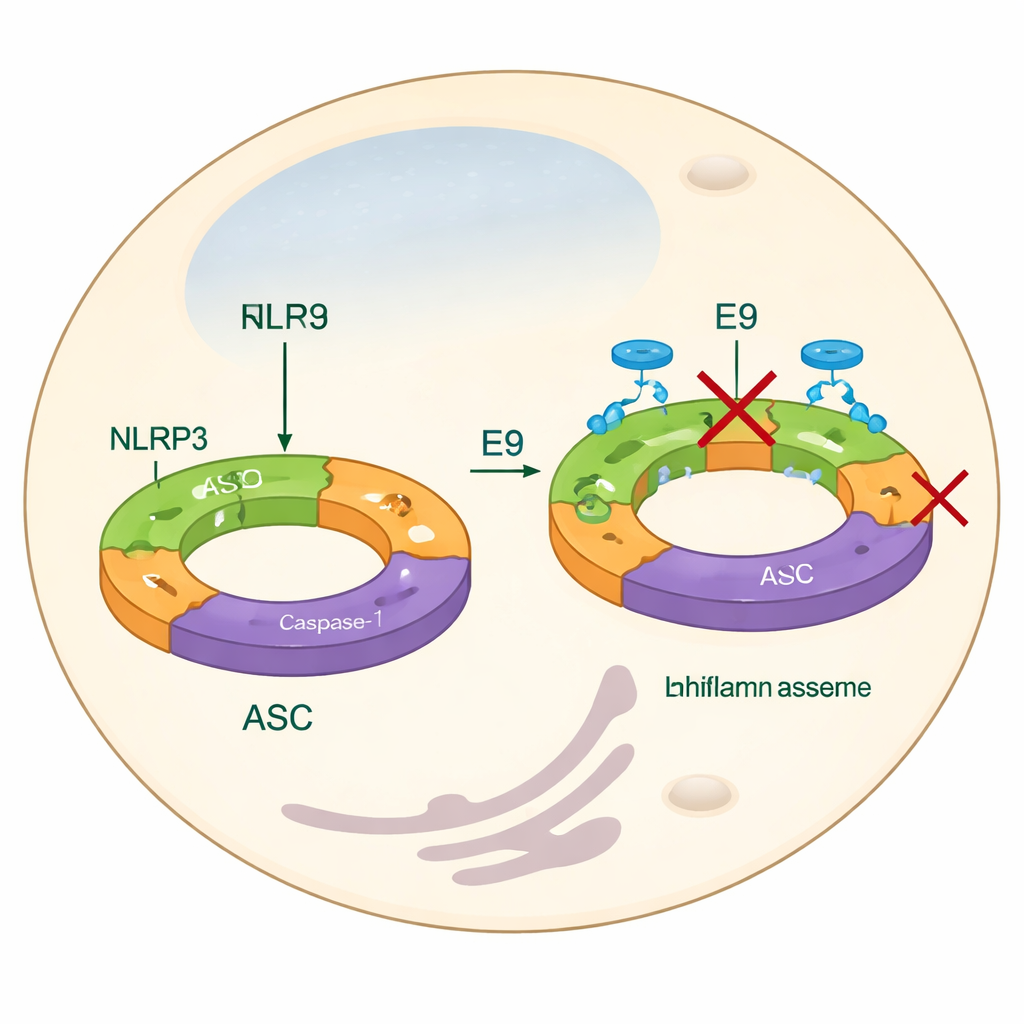
تركز معظم الاستراتيجيات الحالية لتهدئة NLRP3 على حجب منتجاته النهائية — مثل IL-1β — أو على مقاطعة مجال محرك مركزي يستخدم جزيئات طاقة مثل ATP. رغم فعالية هذه النهج أحيانًا، فقد تغفل خطوات التجميع المبكرة ولا تتعامل تمامًا مع كيفية اتصال بروتينات NLRP3 لتشكيل آلة وظيفية. في هذا العمل، ركّز المؤلفون بدلًا من ذلك على مجال البيرين، وهو جزء من NLRP3 يساعد الوحدات الفردية على الانتصاف معًا في خيوط طويلة. هذه الخيوط تجذب بعد ذلك بروتين ملَفّ آخر، ASC، الذي يتكتل إلى "بقع" مضيئة داخل الخلايا — علامة مرئية على تنشيط الإنفلاماسوم. عبر إيجاد مواد كيميائية تمنع مجالات البيرين من الالتقاء بشكل مناسب، يهدف الفريق إلى إيقاف تكوّن الإنفلاماسوم من الأصل.
العثور على جزيء يكسر السلسلة
فحص الباحثون مكتبة مكوّنة من 1500 جزيء صغير مُصنَّع حديثًا باستخدام اختبار ذكي قائم على الضوء. ربطوا قطعًا مقسومة من إنزيم اللوكويز إلى مجال البيرين في NLRP3؛ عندما تقترب اثنتان من مجالات البيرين من بعضهما، تعود شظايا الإنزيم لتتجمّع وتنتج ضوءًا. تسبّب المركبات التي منعت تلامس البيرين–بيرين في انخفاض إشارة الضوء. من هذا الفحص، حدّدوا أربعة مرشحين واعدين، وكان أحدهم — E9 — بارزًا لقدراته القوية والمتسقة على التثبيط. أظهرت قياسات تابعة باستخدام تقنية تُسمى التحرك الحراري المجهري أن E9 يرتبط بقوة بمجال البيرين عند تركيزات منخفضة جدًا (تحت الميكرو مول)، مما يؤكد أن تأثيره ليس صدفة بل نتيجة تفاعل محدد.
رؤية التأثير داخل خلايا حية
لاختبار ما إن كان E9 يعمل أيضًا في نظام حي، لجأ الفريق إلى خلايا شبيهة بالمناعية بشرية مُهندَسة لإنتاج نسخة فلورية من ASC. عند تحفيز هذه الخلايا بمكوّنات بكتيرية ومثير ثانٍ، ينشط NLRP3 وتتجمع بروتينات ASC في بقع مضيئة يمكن عدّها تحت الميكروسكوب. في وجود E9، انخفض عدد هذه البقع بشكل ملحوظ، بمستوى يقارن أو يتفوق على بعض مثبطات NLRP3 المعروفة. أظهر ذلك أن تعطيل تلامسات مجال البيرين يكفي لتقليل تجميع الإنفلاماسوم والخطوات الأولى للموت الخلوي الالتهابي، على الأقل تحت ظروف المعمل.
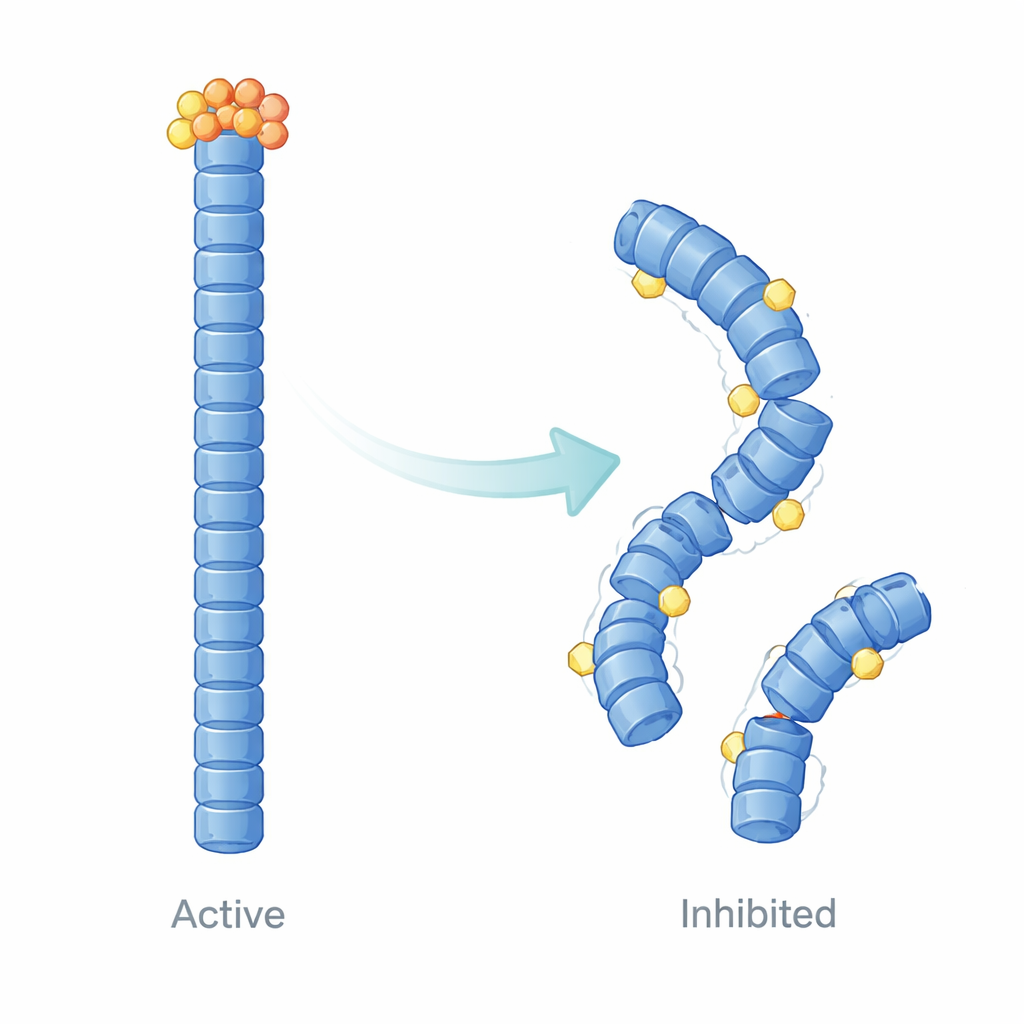
كيف يعيد E9 تشكيل سقالة الإنفلاماسوم
إلى جانب قياس الترابط، استخدم المؤلفون نمذجة هيكلية محوسبة ومحاكاة ديناميات جزيئية لتصوير كيف يغير E9 سلوك خيوط NLRP3 بمرور الوقت. تشير حساباتهم إلى أن E9 يستقر عند أسطح اتصال محددة حيث تلتقي مجالات البيرين، ميسّرًا تليينًا وإعادة تشكيل دقيقة للخيط. بدلًا من بنية متماسكة وتعاونية موحدة، يصبح الخيط غير متكافئ: مناطق قريبة من E9 المرتبط تكتسب مرونة أكبر وتفقد محاذاتها الدقيقة، بينما تصبح أجزاء أخرى معزولة ديناميكيًا. تُخفّض هذه التحولات الحركات واسعة النطاق والتواصل الضيق اللازمين لتجنيد ASC بكفاءة، مما يوفر تفسيرًا فيزيائيًا لانخفاض تكوّن البقع المرصود داخل الخلايا.
ماذا قد يعني هذا للعلاجات المستقبلية
بشكل مجمل، تضع النتائج E9 كنموذج أولي لفئة جديدة من الأدوية المستهدفة للإنفلاماسوم تعمل عن طريق تعطيل الواجهات بين لبنات NLRP3 بدلاً من حجب استخدامه للطاقة أو منتجاته النهائية. رغم أن العمل الحالي مقتصر على تجارب في أنابيب الاختبار، ومحاكاة حاسوبية، وخلايا مزروعة — وهناك حاجة لدراسات أوسع في الحيوانات والبشر — فإنه يبيّن أن جزيئات صغيرة مصممة بعناية يمكنها إعادة تشكيل سقالة الإنفلاماسوم نفسها. بالنسبة للمرضى الذين تقودهم آليات التهاب خارجة عن السيطرة، قد توفر مثل هذه الأدوية المركزة على الواجهات يومًا ما تحكمًا أدق، مقلِّلةً التنشيط المناعي الضار مع إبقاء الدفاعات الأساسية إلى حد كبير سليمة.
الاستشهاد: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
الكلمات المفتاحية: إنفلاماسوم NLRP3, مجال البيرين, مثبط جزيء صغير, المناعة الفطرية, البيبرُوبتوزيس