Clear Sky Science · ar
TTF2 كعلامة حيوية محتملة وهدف للعلاج المناعي في تشخيص وتنبؤ الورم الدبقي
لماذا تهم هذه الدراسة لسرطان الدماغ
الأورام الدماغية المعروفة بالورم الدبقي تعد من بين أخطر أنواع السرطان، حيث يعيش معظم المرضى بضع سنوات فقط بعد التشخيص. بحاجة الأطباء بشكل عاجل إلى طرق أفضل للتنبؤ بسير المرض وإلى أهداف علاجية جديدة، خصوصاً للعلاجات المناعية الحديثة. تركز هذه الدراسة على جزيء غير معروف على نطاق واسع، TTF2، وتطرح سؤالاً بسيطاً بعواقب كبيرة: هل يمكن أن تساعد مستويات TTF2 في أورام الدماغ الأطباء على تشخيص الورم الدبقي بدقة أكبر، توقع البقاء على قيد الحياة، وحتى توجيه العلاجات المناعية المستقبلية؟
إشارة جديدة مخفية في جينات الورم
الورم الدبقي ليس مرضاً واحداً بل مجموعة متنوعة من أورام المخ تختلف في سرعة نموها واستجابتها للعلاج. الأدوات الحالية، مثل الفحص المجهري وبعض العلامات الجينية، لا تفسر تماماً سبب تحسّن بعض المرضى بينما يتدهور وضع آخرين بسرعة. لجأ الباحثون إلى قواعد بيانات جينية سرطانية عامة كبيرة من الولايات المتحدة والصين للبحث عن أدلة جزيئية إضافية. ركزوا على TTF2، بروتين يشارك في إيقاف نشاط الجينات، وقد رُبط بعدة سرطانات أخرى لكنه لم يدرس بعمق في الورم الدبقي.
مستويات عالية من TTF2، مخاطر أكبر
بالمقارنة بين آلاف العينات، وجد الفريق أن مستويات TTF2 أعلى بكثير في نسيج الورم الدبقي مقارنة بالنسيج الدماغي الطبيعي. داخل الأورام، كانت الأورام ذات أعلى مستويات TTF2 تميل إلى أن تكون أكثر تقدماً، تنتمي إلى أنواع فرعية أكثر عدوانية، وتظهر لدى مرضى أكبر سناً. عند متابعة نتائج المرضى، ظهر نمط واضح: الأشخاص الذين احتوت أورامهم على TTF2 أعلى عموماً سجلوا بقاء إجمالي أقصر وتقدماً مرضياً متكررًا بمعدل أعلى. وحتى بعد احتساب تأثير العلامات القوية القائمة مثل درجة الورم، ووضع طفرة IDH، والتغير الصبغي المسمى حذف 1p/19q المشترك، بقي TTF2 علامة تحذيرية مستقلة. بنى الفريق نموذجًا تنبؤيًا يجمع TTF2 مع هذه العوامل القياسية، وقد طابق التنبؤات فعلياً معدلات البقاء لسنة و3 سنوات و5 سنوات في مجموعتي مرضى منفصلتين.
دلائل من محيط الورم
لفهم سبب ارتباط TTF2 بالنتائج السيئة، فحص الباحثون الجينات الأخرى التي ترتفع وتنخفض مع TTF2 وما تمثّله هذه المجموعات الجينية من عمليات حيوية. أظهرت الأورام ذات TTF2 المرتفع نشاطاً أقوى في المسارات المرتبطة بالإشارات المناعية، وإنتاج الأجسام المضادة، والتواصل الخلوي، فضلاً عن مسارات سرطانية معروفة مثل PI3K–AKT. باستخدام أدوات حسابية تستنتج مزيج الخلايا المناعية من أنماط التعبير الجيني، حلّلوا بعد ذلك البيئة الدقيقة للورم. كانت الأورام الغنية بـTTF2 غنية أيضاً بأنواع من الخلايا المناعية—خلايا T المساعدة من النمط Th2 والبلعميات والعدلات—التي غالباً ما ترتبط باستجابة مناعية مكبوتة، كما كانت أقل احتواءً على الخلايا التغصنية البلازمية الشكل التي قد تساعد على تحفيز مناعة أقوى.
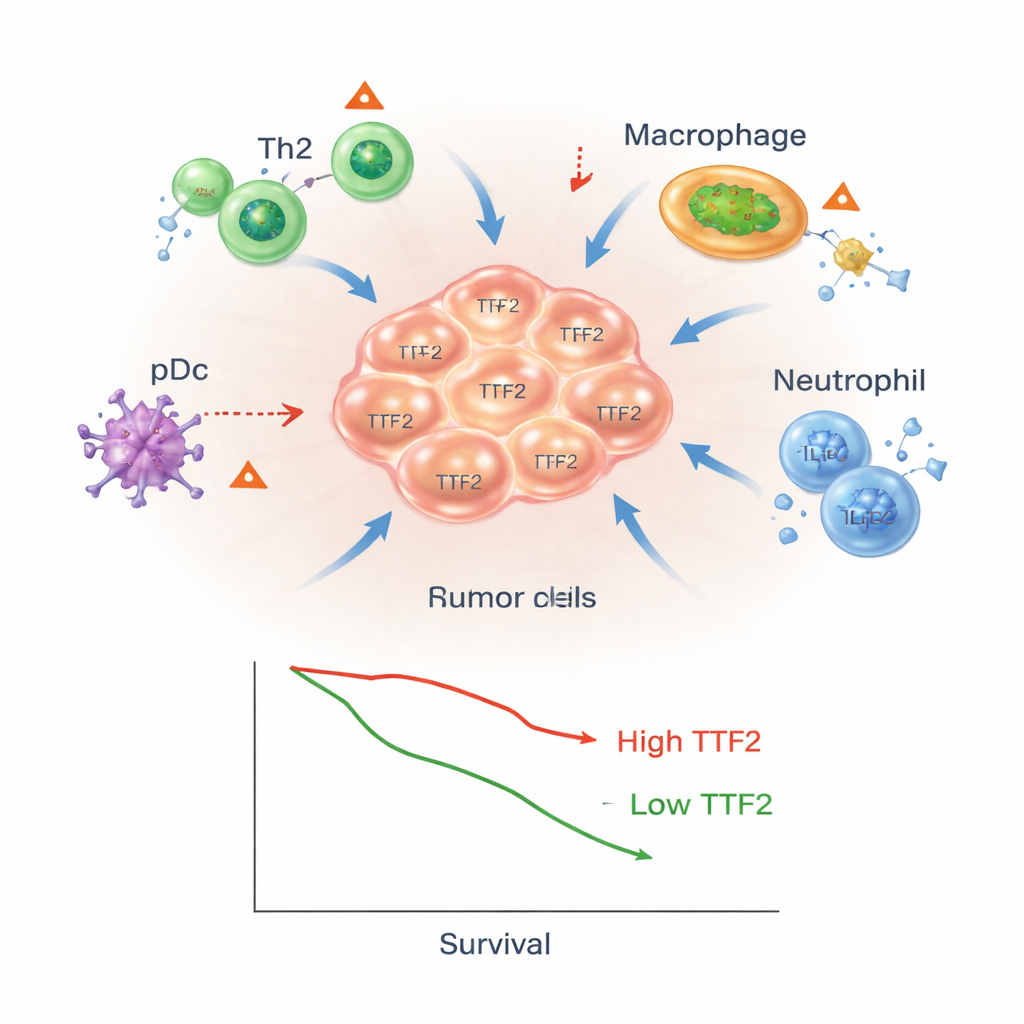
كيف قد يساعد TTF2 الأورام على الاختباء
تقترح هذه النتائج أن TTF2 لا يقتصر دوره على كونه علامة للأورام الخطيرة؛ بل قد يساهم فعلياً في تشكيل درع وقائي حولها. يقترح المؤلفون أنه من خلال التأثير على كيفية إيقاف تشغيل الجينات، يمكن لـTTF2 تعديل مستويات رسوليات مناعية مهمة والكينوكينات—الجزيئات التي تجذب أو تبعد الخلايا المناعية. وقد يوجّه ذلك خلايا T نحو حالة مهيمنة من النمط Th2 الأقل فعالية في قتل الخلايا السرطانية ويشجع تراكم البلعميات والعدلات التي تدعم الورم. ورغم أن هذه الأفكار تنبثق من تحليل بيانات أكثر منها من تجارب مخبرية مباشرة على TTF2، فإنها تقدم نموذجاً قابلاً للاختبار لكيفية مساهمة هذا الجزيء في دعم نمو الورم وهروبه المناعي.
ماذا يعني ذلك للمرضى
تخلص الدراسة إلى أن TTF2 مفرط الإنتاج بقوة في الأورام الدبقية وأن المستويات الأعلى مرتبطة بشكل موثوق ببقاء أسوأ وسمات مرضية أكثر عدوانية. بالنسبة للمرضى، يفتح هذا احتمالين واعدين. أولاً، قد يساعد قياس TTF2 في عينات الورم الأطباء على تحسين التشخيص وتخصيص تقديرات المخاطر بما يتجاوز الاختبارات القياسية الحالية. ثانياً، إذا أكدت الأعمال المخبرية المستقبلية أن TTF2 يساعد الأورام على التهرب من الجهاز المناعي، فقد تصبح أدوية تحيد أو تعدل TTF2—أو مساراته اللاحقة—جزءاً من تركيبات علاجية جديدة تجعل العلاج المناعي أكثر فعالية لمرضى هذا السرطان الدماغي المدمر.
الاستشهاد: Shi, D., Chen, F., Chen , Z. et al. TTF2 as a potential biomarker and immunotherapy target in glioma diagnosis and prognosis. Sci Rep 16, 7653 (2026). https://doi.org/10.1038/s41598-026-35049-9
الكلمات المفتاحية: ورم دبقي, TTF2, علامة حيوية لأورام الدماغ, البيئة المناعية الدقيقة للورم, هدف علاج مناعي