Clear Sky Science · ar
اللمفوما غير الهودجكينية للخلايا B المرتبطة بفيروسات التهاب الكبد تنطوي على اختلال تنظيمي في التعبير الجيني عبر الآليات فوق الجينية والرامية للحمض النووي الريبي وتغير في نسخ snoRNA
لماذا تهم فيروسات الكبد الجهاز المناعي
تُعرف فيروسات التهاب الكبد B وD بشكل رئيسي بإحداثها تلفًا في الكبد، لكن تزداد الأدلة على أنها قد تساهم أيضًا في تحفيز أنواع معينة من سرطانات الدم. تستكشف هذه الدراسة كيف يمكن أن يغير العدوى المزمنة بهذه الفيروسات سلوك خلايا B — المدافعين الرئيسيين في جهاز المناعة — بطرق تزيد من خطر الإصابة باللمفوما غير الهودجكينية للخلايا B، وهي مجموعة من السرطانات التي تنشأ من هذه الخلايا نفسها.
متابعة المرضى في بيئة انتشرت فيها العدوى
للتحقيق في هذه الروابط، درس الباحثون مرضى في منغوليا، وهي دولة تسجل بعض أعلى معدلات التهاب الكبد B وD المزمن في العالم. جمعوا عينات دم من خمس مجموعات: أشخاص مصابون بالتهاب الكبد B فقط، أشخاص مصابون بكل من التهاب الكبد B وD، مرضى لديهم كل من العدوى ولمفوما الخلايا B، مرضى باللمفوما بدون عدوى فيروسية، ومتطوعون أصحاء. ومن هذه العينات عزلوا خلايا B المحيطية — خلايا B المتداولة التي تتجول في مجرى الدم — واستخدموا تسلسل الحمض النووي الريبي لقراءة أي الجينات كانت مفعّلة أو موقوفة في كل مجموعة.
خلايا مناعية تبدو مكتئبة الوظيفة
عند مقارنة أنماط نشاط الجينات، وجد الفريق أن خلايا B لدى المرضى المصابين المزمنين تحمل بصمة من الكبت المناعي الواسع. بالمقارنة مع خلايا B لدى الأشخاص الأصحاء ومرضى اللمفوما غير المصابين بالفيروس، أظهرت خلايا المصابين نشاطًا منخفضًا في شبكات الجينات المرتبطة بتنشيط المناعة والاستجابة للإشارات الالتهابية. أشارت تحليلات المنظمين العلويين إلى أن محفزات مناعية مهمة، مثل السيتوكينات الرئيسية ومسارات مستقبلات خلايا B، كانت عمليًا مكبوتة، بينما كانت عدة جزيئات معيقة لهذه المسارات أكثر نشاطًا. بشكل عام، تصوّر البيانات خلايا B أقل استجابة وأكثر قمعًا خلال العدوى المزمنة بالتهاب الكبد.
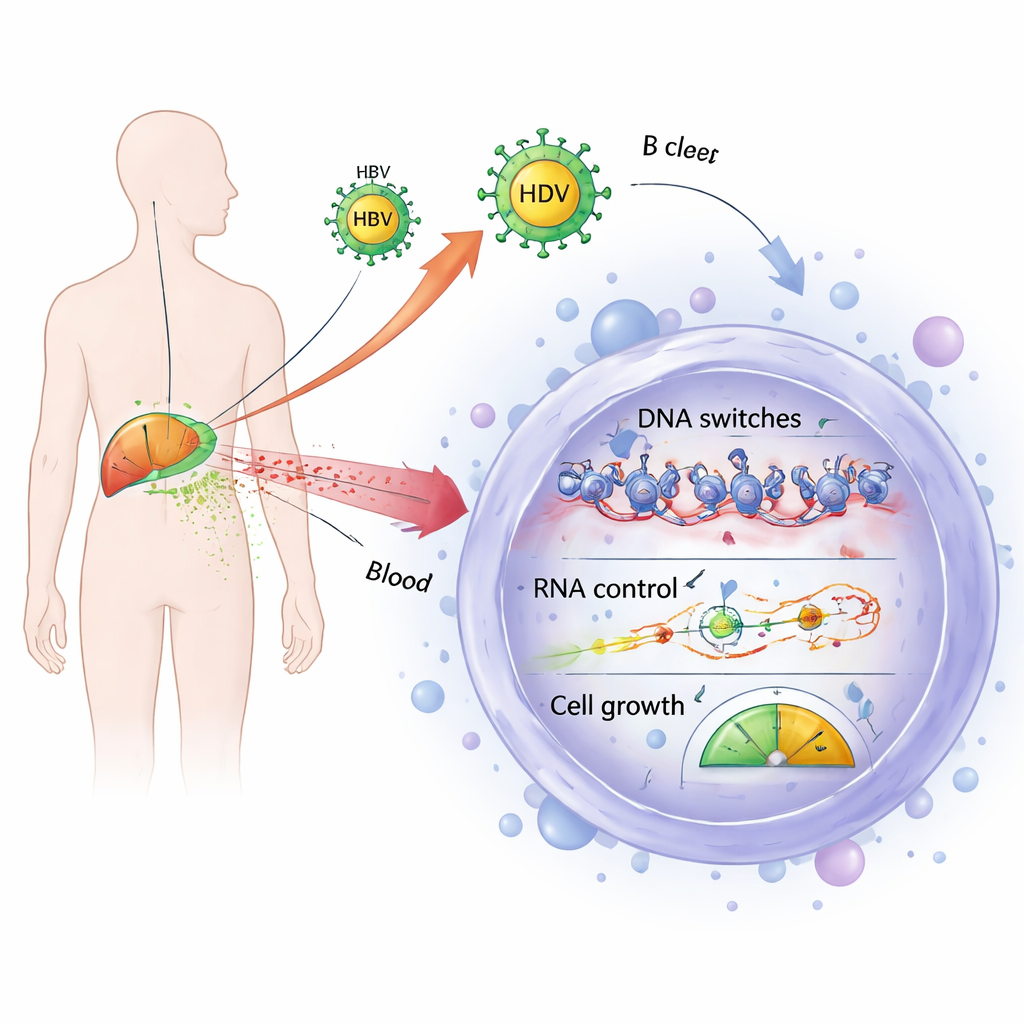
مشكلات مشاركة في التحكم الجيني في الخلايا المصابة والخبيثة
ركز الباحثون بعد ذلك على الجينات التي كانت نشطة باستمرار في جميع مجموعات المرض — المرضى المصابون ومرضى اللمفوما على حد سواء — مقارنة بالمتبرعين الأصحاء. حدّدوا 185 جينًا من هذا النوع ووجدوا أن العديد منها يشارك في التحكم في كيفية تعبئة وقراءة الحمض النووي (التنظيم فوق الجيني) وكيفية معالجة الرسائل الريبية وكبتها. شمل ذلك مكونات متعددة من مجمعات إعادة تشكيل الكروماتين وإنزيمات تضيف أو تزيل العلامات الكيميائية من بروتينات الهيستون التي تشكّل إمكانية الوصول إلى الجينات. كما شمل لاعبين رئيسيين في الآلات التي تستخدمها الميكروRNAs لإغلاق الرسائل المستهدفة. وبما أن تكون خلايا B طبيعيًا يعتمد على ضوابط دقيقة لهذه الأنظمة، فإن فرط نشاطها في كل من اللمفوما المرتبطة بالفيروس وغير المرتبطة به يشير إلى مسار مشترك قد يدفع خلايا B نحو التحول الخبيث.
ارتفاعات غير معتادة في الرنايات الصغيرة داخل الخلايا المصابة
من أبرز النتائج ما كان خاصًا بالمرضى المصابين بالفيروس: زيادة واسعة في الرنا النووي الصغير المنخري (snoRNA) في خلايا B الخاصة بهم. تعيش هذه الجزيئات الصغيرة عادة في النوية الخلوية، حيث تساهم في تعديل رنا الريبوسومي وبناء الريبوسومات، وهي مصانع إنتاج البروتينات. في عدوى التهاب الكبد B وD، تُعرف هذه الفيروسات باختطاف وظائف النوية لدعم تكاثرها. هنا، وجد الفريق 69 snoRNA مميزًا تغيّر نشاطها، معظمها ازداد في خلايا B المصابة، وبخاصة في الحالات المصابة بالتهاب الكبد B فقط. وقد رُبط كثير من هذه snoRNA مسبقًا بأنواع سرطانية في أعضاء أخرى، فتعمل أحيانًا كجينات مُحَرِّضة للورم أو كمثبطات للورم، وبعضها يمكن أن يغيّر مباشرة استقرار أو ترجمة رسائل مرسال محددة.
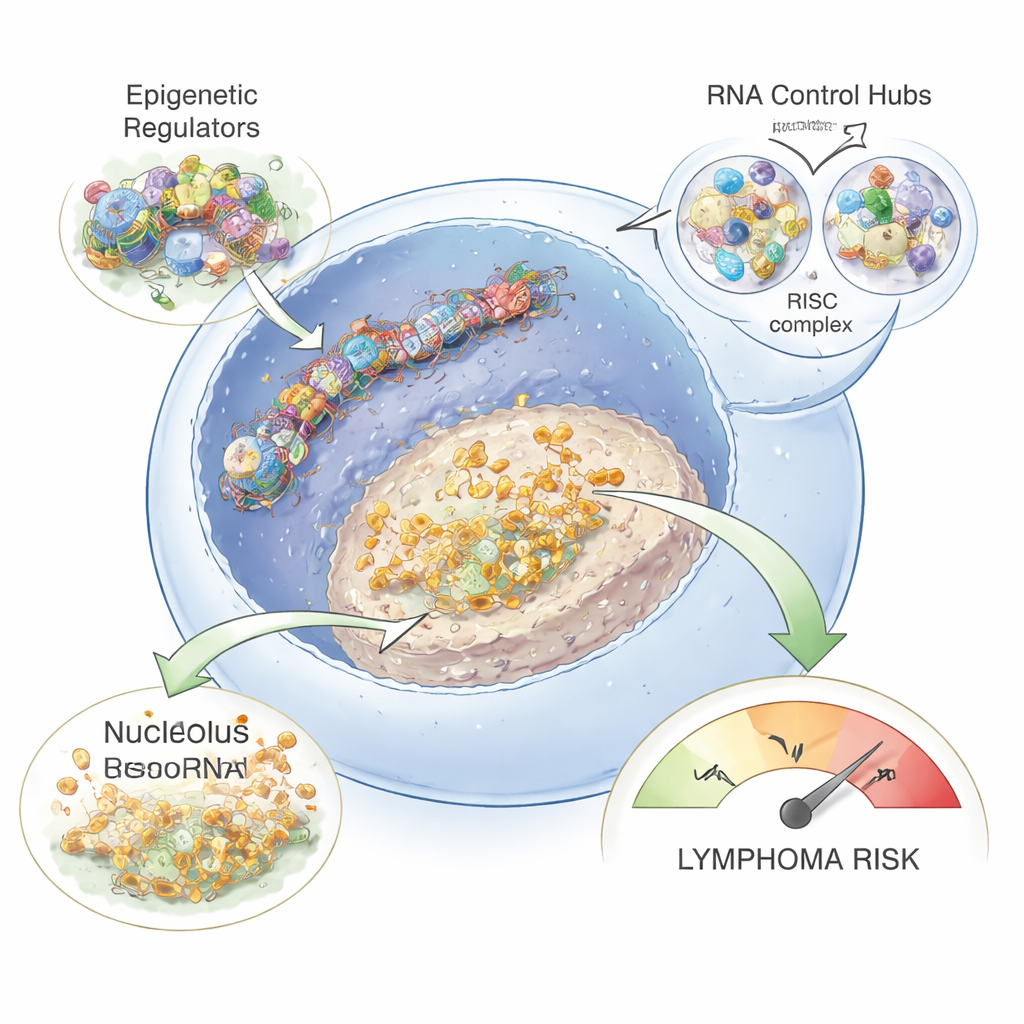
كيف قد تؤدي هذه التغيرات إلى اللمفوما
بربط مستويات snoRNA مع جينات أخرى، أظهرت الدراسة أن snoRNA المرتفعة ميّالّة إلى التحرك بالتوازي مع جينات تشارك في إنتاج الريبوسومات ومجمعات الريبونوكليوبروتين. هذا يشير إلى أن العدوى المزمنة بالتهاب الكبد قد تعيد بشكل دقيق توصيف كيفية بناء خلايا B للريبوسومات ومعالجة الحمض الريبي، مما قد يغيّر أيّ البروتينات تُنتج وبأي كميات. مقترنةً مع فرط نشاط نظم التنظيم فوق الجيني وآلات كبت الميكروRNA، قد تهيئ هذه التحولات أرضية خصبة لحدوث طفرات وإشارات نمو مضبوطة بشكل خاطئ تؤدي في نهاية المطاف إلى دفع خلايا B نحو اللمفوما. وعلى الرغم من أن العمل لا يثبت بعد إصابة كل خلية B مباشرة بالفيروس، فقد كشف المؤلفون عن مواد وراثية لفيروس التهاب الكبد B في خلايا B لمريض واحد على الأقل، مما يدعم فكرة أن الفيروسات يمكن أن تصيب هذه الخلايا وتدفع مباشرة بعض التغيرات الملحوظة.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن فيروسات الكبد قد تؤثر في خطر السرطان أبعد من الكبد من خلال إعادة تشكيل دقيقة لكيفية قراءة الخلايا المناعية لحمضها النووي وبناء آلياتها الداخلية. تبرز الدراسة ثلاثة مشتبهين متداخلين — المنظمات فوق الجينية، مجمعات كبت الرنا، وsnoRNA — التي تبدو مُضطربة في كل من خلايا B المصابة والخبيثة. قد تثمر هذه المسارات في النهاية عن مؤشرات حيوية جديدة لتحديد المرضى الأكثر عرضة لخطر اللمفوما وفرض أهداف دوائية جديدة تعمل في أشكال المرض المرتبطة بالفيروس وغير المرتبطة به. في الوقت الراهن، تعزز النتائج أهمية الوقاية وعلاج التهاب الكبد B وD المزمنين ليس فقط لحماية الكبد، بل أيضًا لحماية الجهاز المناعي من تغييرات تعزز السرطان على المدى الطويل.
الاستشهاد: Henning, A.N., Budeebazar, M., Boldbaatar, D. et al. Hepatitis virus-associated B cell non-Hodgkin’s lymphoma involves dysregulated epigenetic and RNA-mediated regulatory gene expression and altered snoRNA transcription. Sci Rep 16, 5003 (2026). https://doi.org/10.1038/s41598-026-35041-3
الكلمات المفتاحية: التهاب الكبد B, التهاب الكبد D, لمفوما الخلايا B, التنظيم فوق الجيني, snoRNA