Clear Sky Science · ar
درجات حرارة انتقال الزجاج للسوائل المشكلة للزجاج النقية والمخاليط الثنائية
لماذا يهم تباطؤ السوائل في الحياة اليومية
العديد من المواد التي نعتمد عليها — من شاشات الهواتف الذكية وتغليف البلاستيك إلى الأطعمة المعاد تجفيفها والأدوية — ليست صلبة بالمعنى التقني بل زجاجية: سوائل أصبحت حركتها بطيئة جداً فتبدو مجمدة. فهم متى يتحول السائل المتدفق إلى زجاج، وكيف تتغير درجة «التجمّد» هذه عند خلط المواد، أمر أساسي لجعل المنتجات أكثر أماناً واستقراراً وطول عمر. يقدم هذا البحث طريقة جديدة لحساب تلك الحرارة الحرجة مباشرة من كيفية استرخاء الجزيئات وتحركها في المادة، ويمتد بهذه الفكرة إلى المخاليط مثل خليط السكريات وأنظمة السكر–الماء المستخدمة في الغذاء والأدوية.
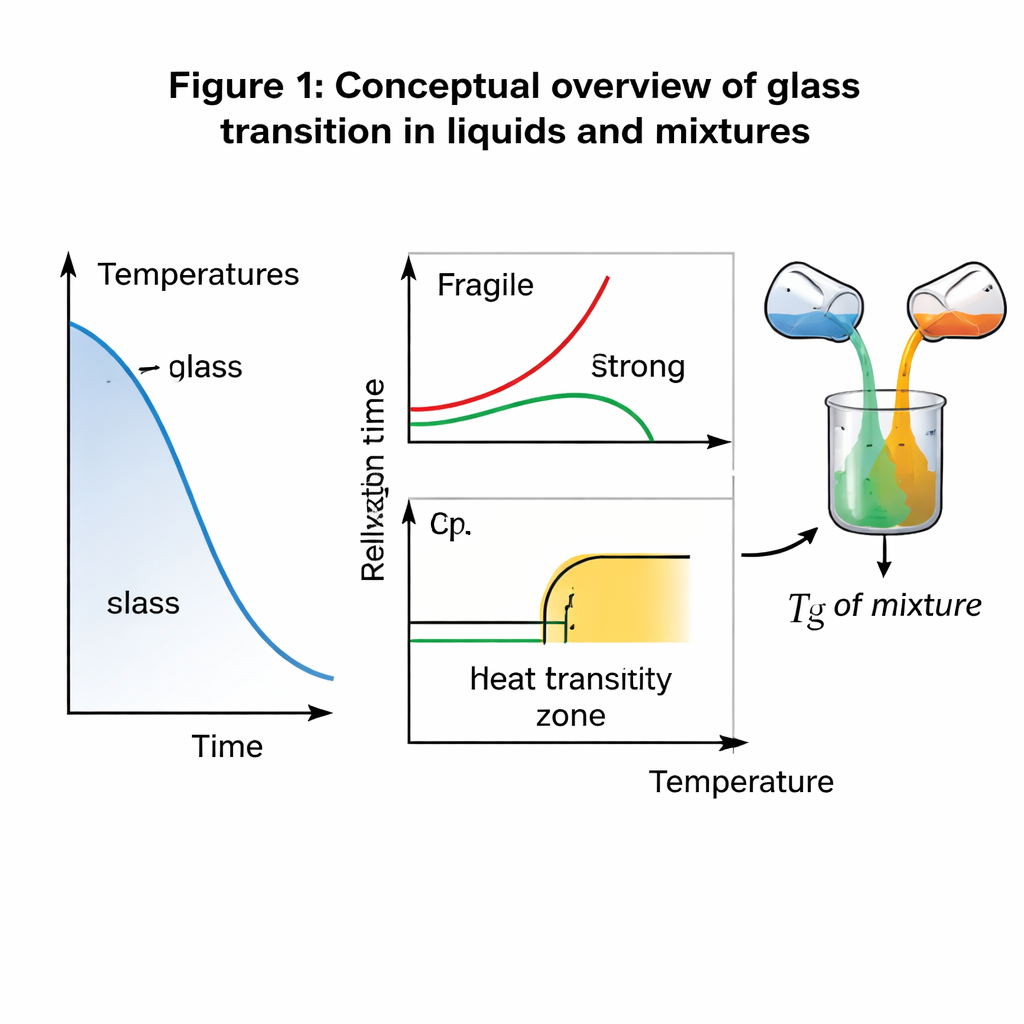
من الذوبات الحادة إلى التجمّد التدريجي
البلورات مثل الثلج أو ملح الطعام تذوب عند درجة حرارة واضحة وحادة. تتصرف المواد الزجاجية بشكل مختلف. عندما يبرد سائل مكوّن للزجاج، تبطؤ جزيئاته تدريجياً حتى يصل، عند درجة حرارة الانتقال إلى الحالة الزجاجية (Tg)، إلى عدم القدرة على إعادة الترتب بسرعة تكفي لمواكبة تغير درجة الحرارة. تخرج المادة عن حالة التوازن وتتصرف كصلبة صلبة لكنها غير مرتبة. تقليدياً، وصف العلماء Tg بطريقتين: من الناحية الحرارية عبر قفزة في السعة الحرارية (كمية الحرارة اللازمة لتسخين المادة)، ومن الناحية الديناميكية عبر الزمن الذي تستغرقه إعادة الترتبات الجزيئية. قاعدة عملية شائعة تقول إن Tg هو حيث يصل زمن الاسترخاء البنيوي إلى نحو 100–1000 ثانية — لكن ذلك إلى حد كبير مجرد اتفاق مريح أكثر من كونه مبدأ راسخاً في الفيزياء.
صلة أنظف بين الزمن والحرارة ومعدل المسح
يبني المؤلفون على فكرة كلاسيكية تربط مباشرة معدل تغيير درجة الحرارة في تجربة (معدل المسح) بسرعة تغير زمن الاسترخاء مع الحرارة. جوهرياً، يعرف الانتقال الزجاجي كنقطة يصبح فيها مقياس الزمن للاسترخاء البنيوي قابلاً للمقارنة مع مقياس زمن مسح الحرارة. باستخدام نماذج قياسية تصف كيف يعتمد زمن الاسترخاء على الحرارة، يحولون هذا الشرط إلى معادلات رياضية صريحة لـ Tg. تتضمن هذه المعادلات دالة رياضية خاصة (دالة لامبرت W) التي أصبحت متاحة مؤخراً على نطاق واسع في برامج علمية، مما يجعل من العملي حل مثل هذه المسائل بيانياً بدلاً من الاعتماد فقط على الملاءمة العددية.
لماذا زمن الزجاج «الكوني» مجرد خرافة
بالمعادلات الجديدة، يبيّن المؤلفون أن زمن الاسترخاء عند الانتقال الزجاجي، الذي يُفترض غالباً أنه قيمة «مخبرية» ثابتة، يعتمد فعلياً بشكل كبير على كل من معدل المسح وطاقة التنشيط للمادة — الحاجز الطاقي الفعّال الذي يتحكم في حركة الجزيئات. عند سرعة مسح معينة، يمكن أن يكون لِمادّات ذات طاقات تنشيط أعلى أو قيم Tg أعلى أزمنة انتقال زجاجية تختلف بما يصل إلى عدة درجات من الحجم. تؤكد المحاكاة باستخدام نماذج الانتقال الزجاجي الشائعة أنه على الرغم من أن طرق تحديد Tg المختلفة (مثل النقطة التي ينحني فيها منحنى السعة الحرارية بأشد ما) ليست متطابقة تماماً، فإنها تعطي درجات حرارة متشابهة جداً، مع إظهار واضح أنه لا يوجد زمن استرخاء وحيد عالمي ينطبق على جميع مكوِّنات الزجاج.
كيف تتشارك مخاليط مكوّنات الزجاج خصائصها
نادراً ما تكون المواد الواقعية نقية. في خلطات البوليمر والمنتجات الغذائية أو الأدوية غير المتبلورة، تُخلط مادتان أو أكثر مكوّنة للزجاج، ويحتاج المصنعون إلى معرفة كيف يعتمد Tg للمزيج على التركيب. تجريبياً، يوصف ذلك غالباً بمعادلة غوردون–تايلور، التي تستخدم ثابت ملاءمة ظل معناه الفيزيائي غير واضح ومثار جدل. يقترح المؤلفون بديلاً ديناميكياً: يفترضون أن معلمات حركية رئيسية — مثل طاقات التنشيط الفعّالة وغيرها من الكميات ذات الصلة — تمزج بطريقة بسيطة مستندة إلى كسور الكتلة لكل مكوّن. من هذه «قواعد الخلط الديناميكية المثالية» يستدلون على تعبير عام لـ Tg للمزيج ويظهرون أنه في حالة حدية تظهر معادلة غوردون–تايلور المألوفة طبيعياً، مع ربط ثابت الملاءمة بطاقة التنشيط أو هشاشة المكونات (مقياس لمدى حدة تباطؤ استرخائها عند التبريد).
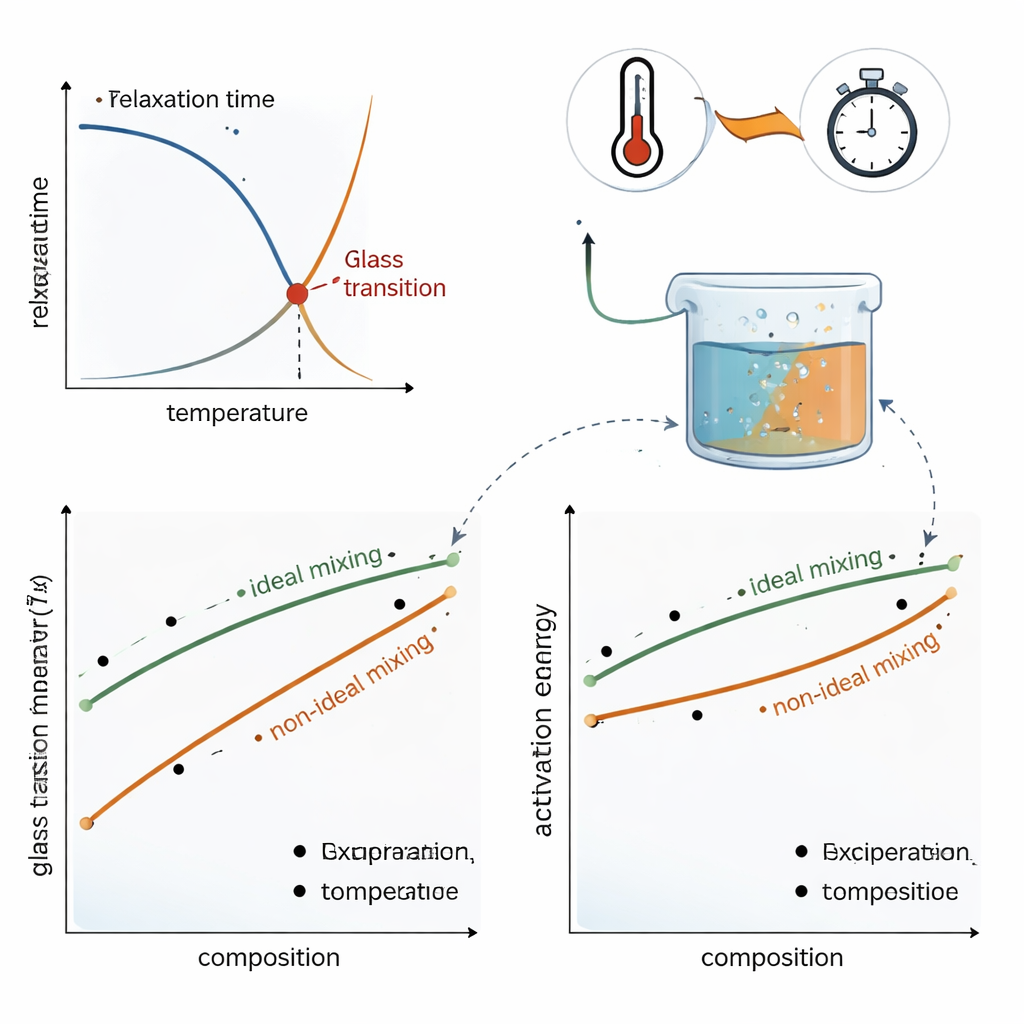
المخاليط الحقيقية: متى تنهار القواعد المثالية
لاختبار إطارهم، يفحص المؤلفون بيانات من نظامين ذيْن أهمية عملية. في مخاليط السكريات سكروز وتريهالوز — شائعة في حفظ الطعام والأحياء — تختلف Tg والطاقة الفعالة قليلاً فقط عما تتنبأ به قواعد الخلط الديناميكية المثالية؛ تعديلات متواضعة على قواعد الخلط تلتقط المنحنيات المرصودة. ومع ذلك في مخاليط سكروز–ماء، يكون السلوك شديد اللا مثالية: إضافة كميات صغيرة من الماء تقلل طاقة التنشيط وTg أكثر بكثير مما يوحي به معدل متوسط بسيط. بالسماح للقواعد بأن تكون غير خطية، يمكن للنموذج الجديد أن يعيد إنتاج الاعتماد الكامل والمنحني لكل من Tg وطاقة التنشيط على التركيب، مما يعكس كيف يرخّ الماء بشدة الشبكة الجزيئية لزجاج السكر.
الرسالة العملية للمواد والمنتجات اليومية
ببساطة، تُظهر هذه الدراسة أن درجة الحرارة التي يصبح عندها السائل زجاجاً لا يحكمها مقياس زمني سحري واحد، بل كيف تستجيب الحركات الداخلية للسائل بسرعة معينة من التبريد أو التسخين. يمتد المنطق الحركي نفسه بطبيعة الحال إلى المخاليط، حيث تظهر علاقة غوردون–تايلور الشائعة كحالة خاصة من قواعد ديناميكية أكثر عمومية. للتقنيين الذين يصممون شاشات هواتف أقوى، أو أغذية تدوم طويلاً، أو أدوية أكثر استقراراً، يقدم هذا الإطار طريقة أكثر تأسيساً فيزيائياً للتنبؤ بضوابط وضبط درجات الانتقال الزجاجي لكل من المواد النقية والمخاليط المعقدة.
الاستشهاد: Kocherbitov, V., Argatov, I. Glass transition temperatures of pure glass-forming liquids and binary mixtures. Sci Rep 16, 1317 (2026). https://doi.org/10.1038/s41598-026-35024-4
الكلمات المفتاحية: الانتقال إلى الحالة الزجاجية, زمن الاسترخاء, الهشاشة, مخاليط مكوِّنة للزجاج, معادلة غوردون–تايلور