Clear Sky Science · ar
رؤى مِيكانيكية حول تثبيط تفاعل البوليميراز بواسطة الميلانين وتخفيفه باستخدام NanoPCR
لماذا يمكن للأصباغ الداكنة أن تخفي أدلة حمض نووي حيوية
عندما يعتمد المحققون أو الأطباء على اختبارات الحمض النووي، يفترضون أن المادة الجينية في العينة يمكن نسخها بنقاء في المختبر. لكن الأصباغ الداكنة مثل الميلانين، التي تمنح الشعر والجلد وبعض الأنسجة لونها، يمكن أن تقوّض خفية خطوة النسخ هذه المعروفة باسم PCR. تكشف هذه الدراسة كيف يتداخل الميلانين مع اختبارات الحمض النووي وتستكشف حلّاً يعتمد على تقانة النانو قد يجعل تحديد الهوية الوراثية أكثر موثوقية في عينات غنية بالأصباغ من مسارح الجرائم وما بعدها.
كيف يدعم النسخ الضخم للحمض النووي علوم الطب الشرعي الحديثة
تفاعل البوليميراز المتسلسل (PCR) هو العمود الفقري لاختبارات الحمض النووي الحديثة. يستخدم إنزيمًا مقاومًا للحرارة، إنزيم تاك، لصنع ملايين النسخ من مقاطع صغيرة من الحمض النووي حتى يمكن قراءتها ومقارنتها. في العمل الشرعي، هذا أساسي لبناء ملفات تعريف STR (التكرارات المتتالية القصيرة) التي تساعد في تحديد الهوية من آثار مثل جذع الشعرة، شظايا الجلد، أو الرفات المحترقة والمتحللة. مع ذلك، نادرًا ما تصل العينات الواقعية نقية؛ غالبًا ما تحمل معها «مسببات مشاكل» كيميائية يمكن أن تعرقل PCR وتحرم المحللين من ملفات تعريف حمض نووي واضحة وصالحة للمحكمة.
الميلانين: الصبغة التي تعترض الطريق
الميلانين، نفس الصبغة التي تحمي بشرتنا وشعرنا من ضوء الشمس، يتبين أنه أحد أكثر عوامل تثبيط PCR عنادًا في العينات الجنائية. حتى لو شكّل نسبة قليلة من كتلة الشعرة، فإن بنيته المعقدة واللزجة تتيح له الالتحام بالبروتينات وأيونات المعادن، ويمكنه أن يعوق لقاء الحمض النووي مع إنزيم البوليميراز. أظهرت أعمال سابقة أن الميلانين يقلل كفاءة PCR ويتسبب في ملفات تعريف جزئية أو فاشلة، لكن الآلية الدقيقة لتعطيله لعملية النسخ لم تكن واضحة. غالبًا ما تُسفر العينات الغنية بالميلانين—مثل الشعر الداكن، الأنسجة المصبوغة، أو الرفات المحترقة—عن فقدان إشارات الحمض النووي، انخفاض ارتفاع القمم، واختلال توازن الأليلات ما يقلل القيمة الإثباتية للملف.
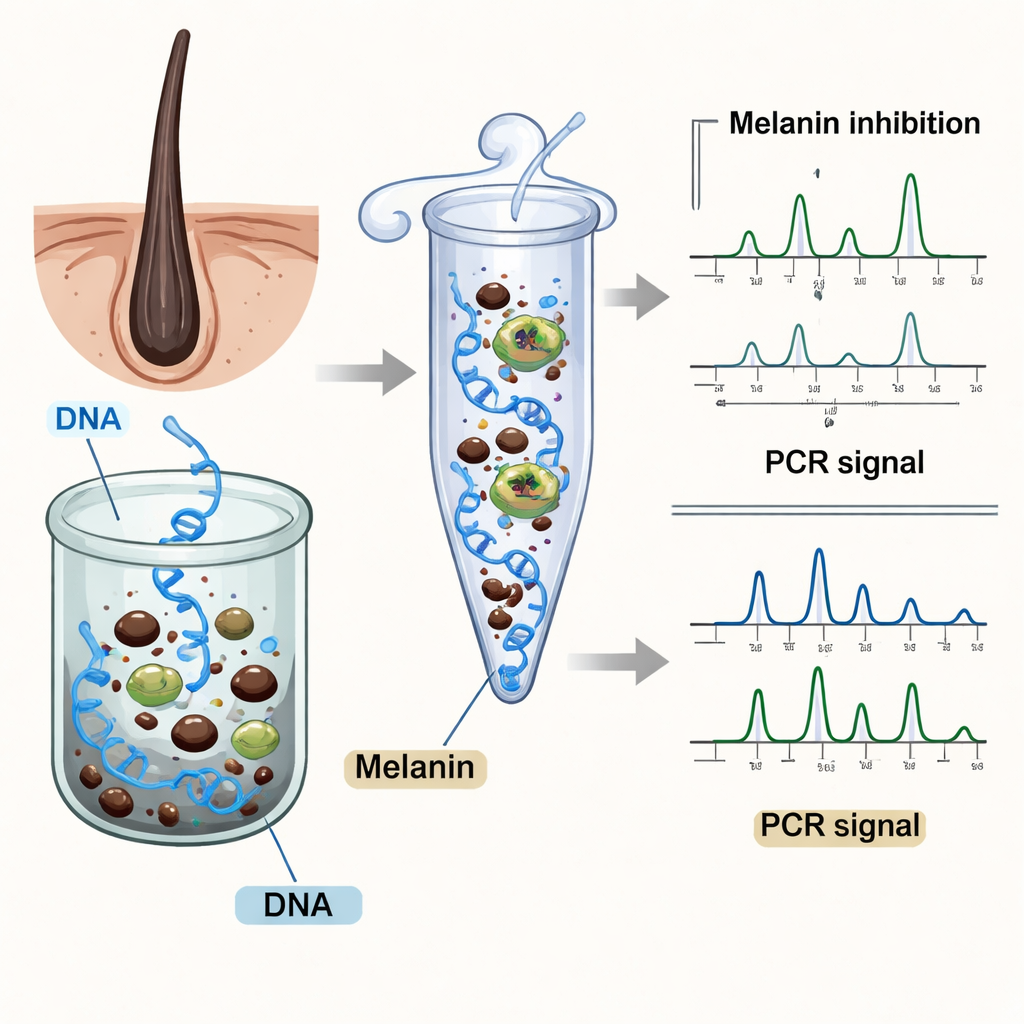
تقريبًا إلى مستوى التداخل بين الميلانين وإنزيم PCR
استخدم المؤلفون النمذجة الحاسوبية والاختبارات المخبرية لمراقبة، فعليًا، تفاعل الميلانين مع إنزيم تاك على المستوى الجزيئي. كشفت المحاكاة التفصيلية لبنية الإنزيم أن الميلانين يستقر في مناطق رئيسية عادةً ما تثبت الحمض النووي وتساعد في إضافة الوحدات البنائية أثناء النسخ. على وجه الخصوص، يشكل الميلانين تواصلات ثابتة غير تساهمية مع أحماض أمينية محددة تبطن النواة الحفازة ومجرى ربط الحمض النووي، مما يزعزع شكل الإنزيم بشكل طفيف. وأكد اختبار الفلورة الذي يتتبع التغيّرات حول بقايا التربتوفان أن الميلانين يرتبط بالإنزيم بقوة معتدلة وبشكل قابل للانعكاس. تدعم هذه المعطيات مجتمعة فكرة أن الميلانين يعمل كمثبط تنافسي متعدد الأوضاع—يشغل مساحات واتصالات يحتاجها إنزيم تاك، مما يبطئ أو يشوّه تفاعل النسخ دون تدمير دائم للإنزيم.
كيف يبدو هذا في ملفات تعريف الحمض النووي الحقيقية
لمعرفة التأثير العملي، أجرى الفريق تأشيب STR على حمض نووي تعرض للميلانين. بدت النتائج كأنها شريط باركود تالف: بعض العلامات الغنية بالمعلومات، مثل SE33 وPenta E، اختفت تمامًا؛ وأظهرت علامات أخرى إشارات ضعيفة وارتفاعات قمم غير متوازنة. انخفضت شدة الإشارة الإجمالية وتباين النمط عبر قنوات الصبغة، بما يتوافق مع تدخل غير متساوٍ. هذا النوع من التلاشي الانتقائي والاختفاء يثير قلقًا خاصًا في العمل القضائي، حيث يمكن لفقدان عدد قليل من العلامات القوية أن يضعف وضوح الهوية أو يعقّد تفسير العينات المختلطة. ومن المثير للاهتمام أن بعض المواقع أظهرت أحيانًا إشارات مرتفعة بشكل غير متوقع، ويعزو المؤلفون ذلك إلى الطبيعة العشوائية المتقطعة لتفاعل PCR تحت الضغط بدلاً من أي تحسّن حقيقي—تذكير آخر بأن التفاعلات المثبطة قد تضلّل إذا قِيّمت من خلال قمم معزولة فقط.
الجسيمات النانوية وبروتين مألوف يتدخلان للإنقاذ
لأن إزالة الميلانين مباشرة قد تزيل أيضًا الحمض النووي الثمين، استكشف المؤلفون مساعدين «داخل الأنبوب» يحيدون المانع بدلًا من إزالته. قارنوا ثلاث إضافات: جسيمات ذهبية عادية، والبروتين الشائع ألبومين مصل البقرة (BSA)، والجسيمات الذهبية المغلفة بـBSA. قدمت الجسيمات الذهبية العادية استردادًا جزئيًا فقط للإشارة. أما BSA الحر، وهو مساعد معروف في PCR، فقدم أقوى استعادة عامة لارتفاع القمم وتوازن الأليلات، لكن فقط عند تركيزات مرتفعة وحسّاسة، ومع تباين أكبر بين العينات. النهج الهجين—الجسيمات الذهبية المغلفة بـBSA—حقق توازنًا: حسّن الإشارة واسترداد العلامات بشكل ملحوظ، مقتربًا من أداء BSA الحر، مع استخدام كميات أقل بكثير من البروتين وإنتاج ملفات تعريف أكثر اتساقًا وقابلة للتكرار. تعمل الجسيمات النانوية كدعامة ثابتة تعرض BSA بطريقة تمتص الميلانين بفاعلية وتحمي البوليميراز أثناء دورات التسخين والتبريد.
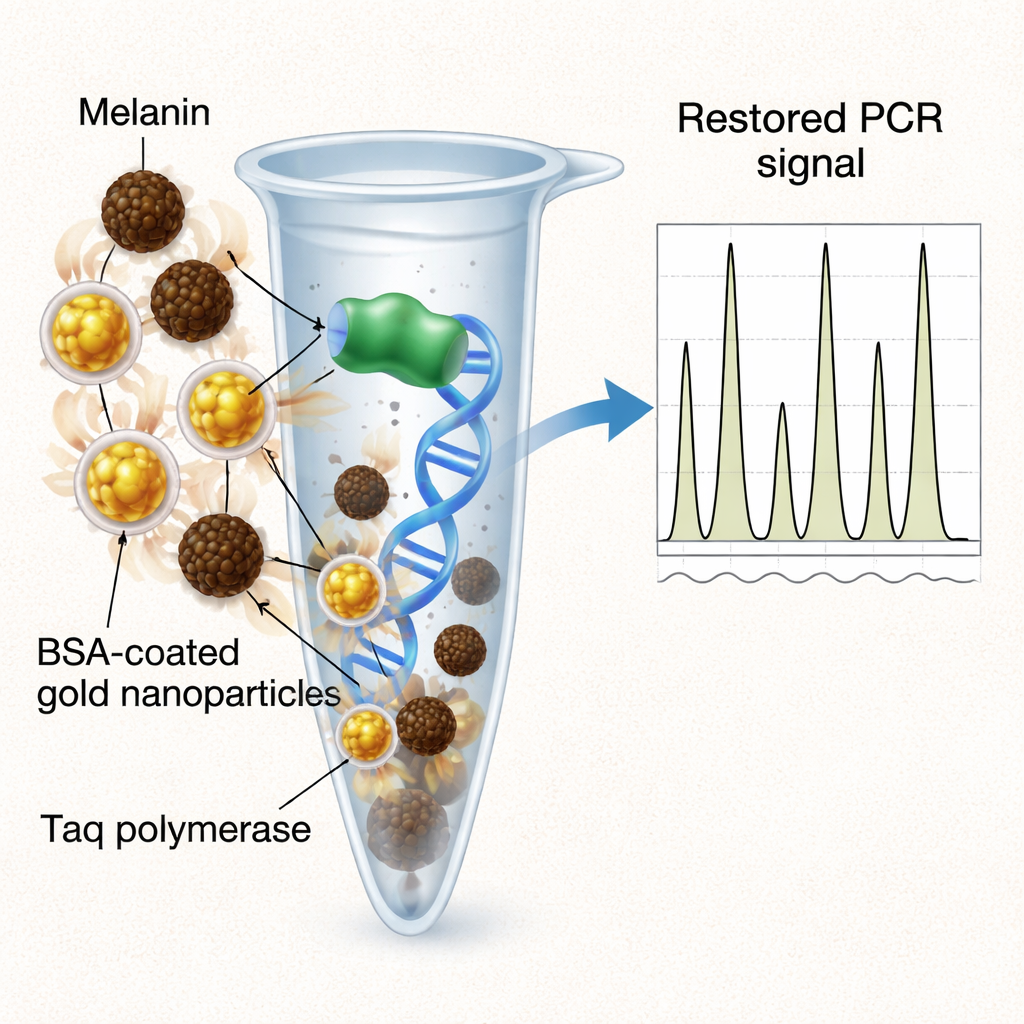
ما يعنيه هذا للاختبارات الحقيقية للحمض النووي
لغير المتخصصين، الخلاصة أن الصبغة الداكنة في عينات الأدلة يمكن أن تعطل اختبارات الحمض النووي بصمت عبر تعطيل الإنزيم ذاته الذي يجعل الاختبار ممكنًا. توضح هذه الدراسة ليس فقط كيف يحدث هذا التدخل على المستوى الذري، بل تُظهر أيضًا أن المواد النانوية المصممة بعناية—جسيمات ذهبية مكسوة بطبقة رقيقة من بروتين مألوف—يمكن أن تنقذ إشارات الحمض النووي دون فقدان المادة أو إدخال شوائب. رغم أن التحقق الإضافي على عينات قضائية حقيقية لا يزال مطلوبًا، تشير النتائج إلى وجود إضافات منخفضة الجرعة وأكثر متانة قد تساعد مختبرات الطب الشرعي والتشخيص الطبي وحتى دراسات الحمض النووي القديمة على قراءة المعلومات الوراثية من مواد صعبة وغنية بالأصباغ بشكل أكثر موثوقية.
الاستشهاد: Vajpayee, K., Srivastava, S., Sharma, S. et al. Mechanistic insights into melanin-induced PCR inhibition and its NanoPCR-based mitigation. Sci Rep 16, 5467 (2026). https://doi.org/10.1038/s41598-026-35010-w
الكلمات المفتاحية: حمض نووي جنائي, تثبيط PCR, ميلانين, جسيمات ذهبية نانوية, تقانة نانوية في علم الوراثة