Clear Sky Science · ar
الأساس البنيوي للديوسجينين كمنشط عكسي لمستقبل الارتباط بحمض الريتينويك المرتبط باليتيم γ
لماذا يهم مركب نباتي ومفتاح مناعي
العديد من الحالات المزمنة — من أمراض المناعة الذاتية مثل التصلب المتعدد والصدفية إلى السمنة والسكري من النوع الثاني — يُحفَّز بها إشارات مناعية مفرطة أو إشارات أيضية خاطئة. لطالما سعى العلماء إلى أدوية أكثر أمانًا قادرة على تنظيم هذه الإشارات بدقة. تستقصي هذه الدراسة كيفية ارتباط الديوسجينين، جزيء طبيعي يوجد في بعض النباتات الطبية والبطاطا البرية (اليام)، ببروتين منظم للمناعة يُدعى RORγ ويحوِّله إلى حالة أقل نشاطًا. فهم هذا التفاعل على مستوى ذري قد يفتح الباب لعلاجات أكثر رقة واستهدافًا مبنية على هيكل نباتي مألوف.
مِقوَم رئيسي للمناعة والأيض
RORγ هو جزء من عائلة كبيرة من «المستقبلات النووية» — بروتينات داخل الخلايا تُشغِّل أو تُطفئ الجينات استجابةً لجزيئات صغيرة. هذا البروتين على وجه الخصوص هو متحكم رئيسي في مجموعة من خلايا المناعة المعروفة بخلايا Th17، التي تنتج الإشارة الالتهابية IL-17A وترتبط بأمراض مناعية ذاتية مثل التصلب المتعدد والصدفية والتهاب المفاصل الروماتويدي ومرض كرون. يؤثر RORγ أيضًا في تطور الخلايا الدهنية واستجابة الجسم للإنسولين، مما يربطه بالسمنة والسكري. وبفضل هذا الامتداد الواسع، أصبح RORγ هدفًا دوائيًا جذابًا، لكن العديد من الجزيئات الصناعية التي ترتبط به واجهت مشاكل تتعلق بالسلامة أو الانتقائية أو الفعالية في البشر.
علاج تقليدي يكشف عن رائد واعد
الديوسجينين هو جزيء يشبه الستيرويد يُستخلص من نباتات تشمل أنواعًا من ديوسكوريا (اليام البري) وعدة أعشاب طبية تقليدية. دُرِس لأثره المضاد للالتهاب، والمضاد للسرطان، والمضاد للسكري، وفوائده القلبية الوعائية في نماذج خلوية وحيوانية. أشارت أعمال سابقة إلى أن الديوسجينين قد يؤثر على مسار RORα/γ ويكبِّح استجابات Th17 الضارة، لكن لم يكن واضحًا ما إذا كان يتصل مباشرةً بـRORγ، أو كيف قد يغيّر سلوك البروتين. للإجابة عن ذلك، فحص الباحثون مكتبة من المركبات الطبيعية باستخدام اختبار ارتباط حساس وحددوا الديوسجينين كمُرتبط قوي بمنطقة ربط الليجاند في RORγ.
كيف يدفع الديوسجينين RORγ إلى العكس
درس الباحثون كيف يؤثر الديوسجينين على قدرة RORγ في استقدام بروتينات مساعدة تعزّز (مُنَشِّطات مشتركة) أو تُخمد (مُكمّمات مشتركة) نشاط الجينات. على نحو مفاجئ، شجّع الديوسجينين RORγ على الارتباط بكلا النوعين من الشركاء، وهو نمط يختلف عن نمط مضاد طبيعي معروف هو حمض الأورسوليك. في اختبارات خلوية تقيس تشغيل الجينات، قلّل الديوسجينين نشاط RORγ بشكل متزايد مع زيادة الجرعة، وكانت الفعالية ضمن نطاق دون الميكرو مولي. هذا السلوك يطابق تعريف «منشط عكسي»: مركب لا يكتفي بحجب النشاط الأساسي بل يدفع المستقبل فعليًا نحو حالة إيقاف حتى عندما يكون مُفعلًا عادةً.
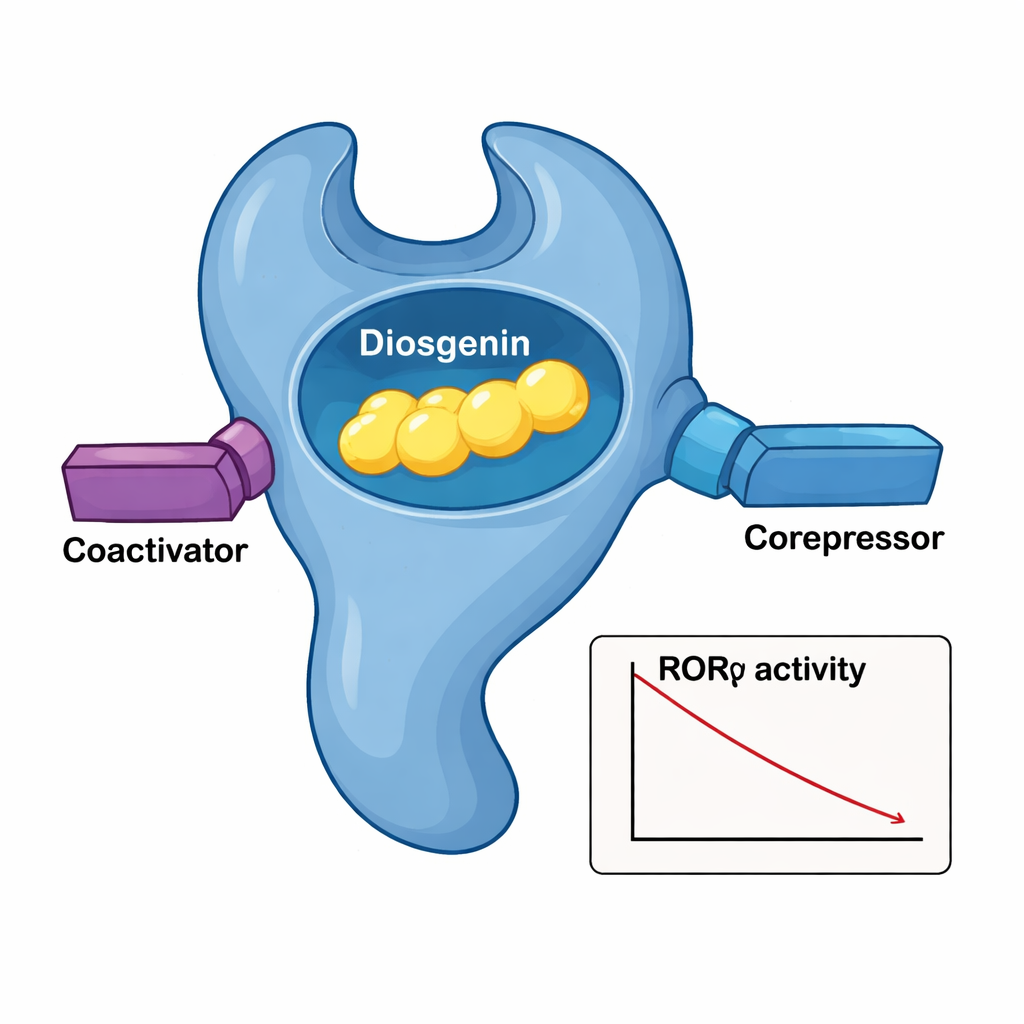
لمحة قريبة عن المصافحة الجزيئية
لرؤية كيف يتناسب الديوسجينين داخل RORγ بدقة، حلّل الفريق البنية البلورية ثلاثية الأبعاد لمجال ربط الليجاند في البروتين مع وجود الديوسجينين بداخله. ينطوي المستقبل على حزمة متداخلة من الحلقات α تشكل جيبًا يحتضن جسم الديوسجينين الشبيه بالستيرويد. تشكّل شبكة من الاتصالات الكارهة للماء بين عدة أحماض أمينية قفازًا مخصّصًا حول العمود الفقري للجزيء، بينما يشكل مجموعة هيدروكسيل حرجة على الديوسجينين روابط هيدروجينية بوساطة الماء مع بقايا أرجينين اثنين. عندما تغيّرت بقايا الجيب هذه واحدًا تلو الآخر، انخفضت قدرة الديوسجينين على إسكات RORγ، مما أكد أهميتها. أظهرت المقارنات الهيكلية مع مركب RORγ–حمض الأورسوليك أن الديوسجينين يحافظ على حلقة ذيلية رئيسية (AF‑2) في وضع «شبيه بالنشط» حتى وهو يدفع النسخ الجيني الكلي نحو الانخفاض، ما يفسر قدرته على جذب كل من المنشطات المشتركة والمكممات المشتركة في آن واحد.
من البنية البلورية إلى أدوية مستقبلية
تسلط الصورة التفصيلية لتفاعل الديوسجينين–RORγ الضوء على ميزتين ملحوظتين لتصميم الأدوية. أولًا، يظهر جيب المستقبل مرونة كافية للتعرف على أشكال ليجاند مختلفة، ما يعني أن الكيميائيين يمكنهم تعديل هيكل الديوسجينين لتحسين الانتقائية تجاه RORγ وتقليل الارتباط غير المرغوب بمستقبلات نووية أخرى. ثانيًا، يجعل الأصل الطبيعي للديوسجينين وسُمّيته المنخفضة المعروفة في النماذج قبل السريرية منه نقطة انطلاق جذابة مقارنةً ببعض المركبات الصناعية الكاملة التي توقفت في التجارب. ببساطة، تكشف هذه الدراسة كيف يمكن لجزيء مستمد من نبات أن يرتبط بمفتاح مركزي للمناعة والأيض ويدفعه إلى الخلف، مقدمة قالبًا بنيويًا لتطوير علاجات أكثر أمانًا وفعالية لأمراض مرتبطة بـRORγ.
الاستشهاد: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
الكلمات المفتاحية: ROR غاما, ديوسجينين, أمراض مناعية ذاتية, مستقبل نووي, منشط عكسي