Clear Sky Science · ar
التوصيف النسخي للاختلال في الاقتران البديل في عضلات الهيكل العظمي لمرضى الساركوبينيا
لماذا تفقد العضلات قدرتها مع التقدم في العمر
الساركوبينيا—الفقدان التدريجي لكتلة العضلات وقوتها مع التقدم بالعمر—هي أحد الأسباب الرئيسية التي تجعل كبار السن يواجهون صعوبات في المهام اليومية، من صعود الدرج إلى حمل البقالة. تتعمق هذه الدراسة داخل العضلات المسنة على مستوى الـRNA، الرسائل التي تخبر الخلايا أي بروتينات تصنع. يبين المؤلفون أنه في الساركوبينيا تُقصَّ وتُلَصق كثير من رسائل الـRNA بطرق غير طبيعية، مما قد يخل بإنتاج الطاقة في العضلة ويشير إلى أهداف علاجية جديدة.
فقدان العضلات ونظام «تحرير» الجينات في الجسم
جيناتنا مكتوبة في الـDNA، لكن الخلايا تعمل بنسخ RNA من تلك الجينات. قبل أن تُستخدم رسالة الـRNA، تقصّها الخلايا عادة وتربط أجزاءها—تمامًا كتحرير فيلم—بحيث يمكن لجين واحد أن ينتج عدة نُسخ من البروتين. تُعرف هذه العملية بالاقتران البديل، وهي نشطة بشكل خاص في العضلات التي تحتاج بروتينات مضبوطة بعناية للانقباض والإصلاح والتكيف مع التمرين. عندما يخطئ الاقتران، قد تُنتَج نسخ بروتينية خاطئة أو تُفقد نسخ مهمة، مما يساهم في أمراض مثل الضمور العضلي وبعض اضطرابات الدماغ. افترض المؤلفون أن طبقة مخفية مماثلة من سوء تحرير الـRNA قد تكون دافعة للساركوبينيا.
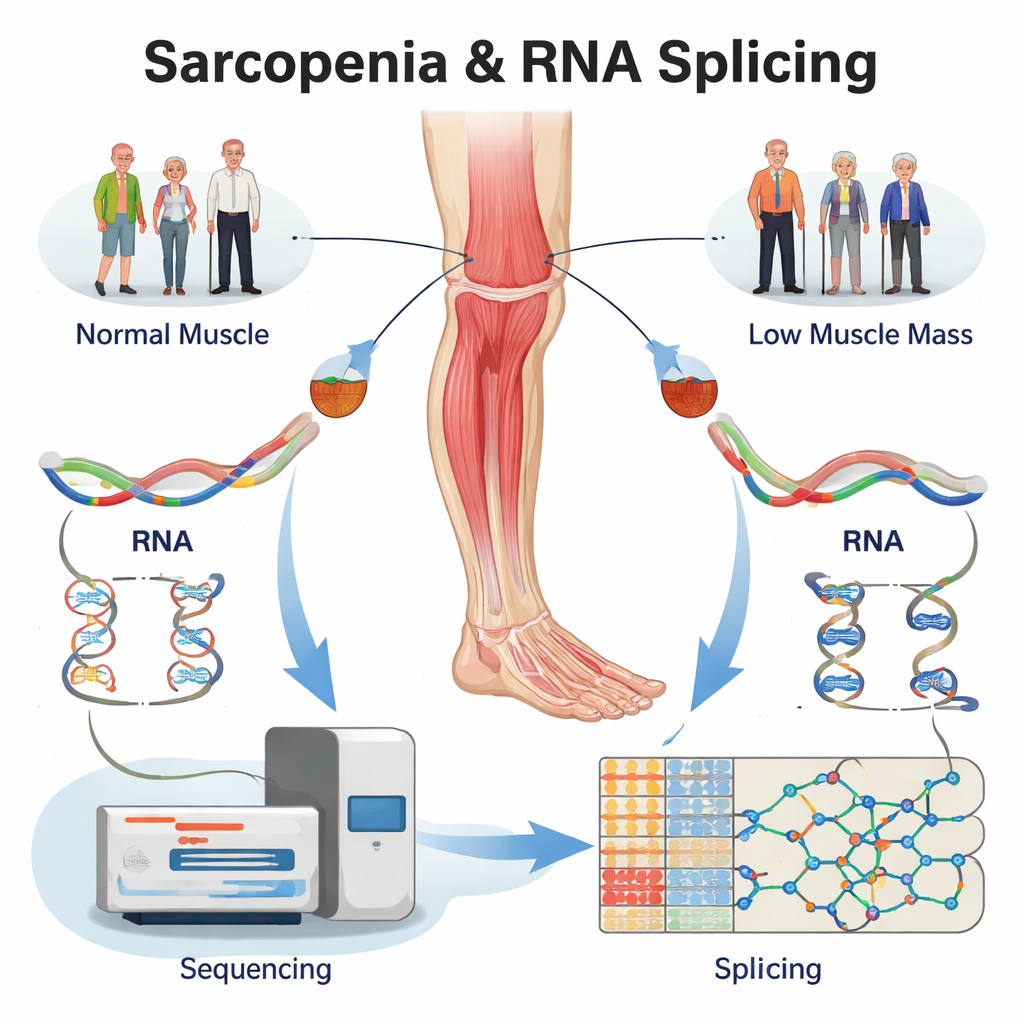
إعادة قراءة بيانات موجودة للعثور على أخطاء RNA المخفية
بدلاً من تجنيد متطوعين جدد، أعاد الفريق تحليل مجموعة بيانات كبيرة لتسلسل الـRNA مأخوذة من خزعات عضلات الفخذ البشرية. جاءت العينات من أربع مجموعات: كبار السن المصابون بساركوبينيا كاملة، أشخاص لديهم انخفاض في كتلة العضلات فقط، أشخاص لديهم ضعف قوة العضلة فقط، وأصحاء متطابقون في العمر كمجموعة ضابطة. باستخدام برامج متخصصة، أكدوا أولًا أن مئات الجينات كانت مرتفعة أو منخفضة في العضلات المريضة. والأهم من ذلك، نظروا بعد ذلك إلى كيفية اقتران كل جين من نسخ الـRNA، فردّوا أكثر من 5000 تغيير في الاقتران عبر المجموعات الثلاث المشكلة مقارنة بالعضلات السليمة. تركزت هذه التغيرات في بعض الأنواع الأساسية—مثل تخطي إكسون، أو اختيار موقع قطع بديل—وهي أنماط معروفة بتغيير هيكل البروتين بشكل قوي.
مصانع الطاقة ومسارات «مؤشر الوقود» الخلوي تتعرض للاضطراب
ظهرت تغييرات الاقتران في جينات تقع في قلب بيولوجيا العضلة. كثير من الجينات المتأثرة تبني أجزاء من الميتوكوندريا، مصانع الطاقة الصغيرة التي تشغّل انقباض العضلات. في عضلات الساركوبينيا، أظهرت 16 جينًا مشاركة في الفسفرة التأكسدية—العملية التي تحول المواد المغذية إلى طاقة قابلة للاستخدام—اقترانًا متغيرًا، خاصة مكونات المجمعات الميتوكوندرية المسؤولة عن نقل الإلكترونات وضخ البروتونات. ظهرت تغييرات أخرى في جينات تصنع أو تستخدم NAD⁺، الجزيء الرئيسي لطاقة الخلية والإصلاح. بدلًا من أن تكون ببساطة أكثر أو أقل وفرة، أنتجت إنزيمات مهمة مثل CD38 وPARP2 وعدد من السرتوينات نسخ RNA مختلفة، مما يوحي بأن التوازن بين إنتاج NAD⁺ واستهلاكه مشوّه على مستوى الاقتران. كما تجمع الجينات المتأثرة في مسارات إشارة معروفة في العضلات، بما في ذلك مسارات AMPK وFoxO، التي تعمل كمؤشرات وقود وقوات استجابة للإجهاد في الخلية.
أنماط مشتركة عبر مراحل مختلفة—وعبر الأنواع
لافت أن العديد من نفس الجينات أظهرت تغييرات في الاقتران ليس فقط لدى الأشخاص المصابين بالساركوبينيا الكاملة، بل أيضًا لدى الذين لديهم انخفاض في كتلة العضلات فقط أو ضعف في القوة فقط. هذا يشير إلى أن الاقتران غير الطبيعي يبدأ مبكرًا ويعبر وجوهًا سريرية مختلفة للمرض. لاختبار ما إذا كان يمكن استنساخ هذه التغيرات في نموذج حيواني، سبب الباحثون هزالًا عضليًا في فئران بواسطة الستيرويد ديكساميثازون، وهو طريقة معيارية لمحاكاة بعض ميزات الساركوبينيا. طوّرت الفئران قوة قبضة أضعف وأداء أسوأ في اختبارات الجري والتوازن. عندما قام الفريق بتسلسل RNA لعضلات الفئران، وجدوا مرة أخرى مئات الجينات ذات اقتران متغير. تداخل نحو خُمس هذه الجينات مع جينات الساركوبينيا البشرية، وكان العديد منها مشاركًا في التحكم بالنسخ وبنية الكروماتين والاقتران نفسه—مفاتيح على مستوى أعلى يمكنها إعادة تشكيل مخرجات البروتين الكلية للخلية.
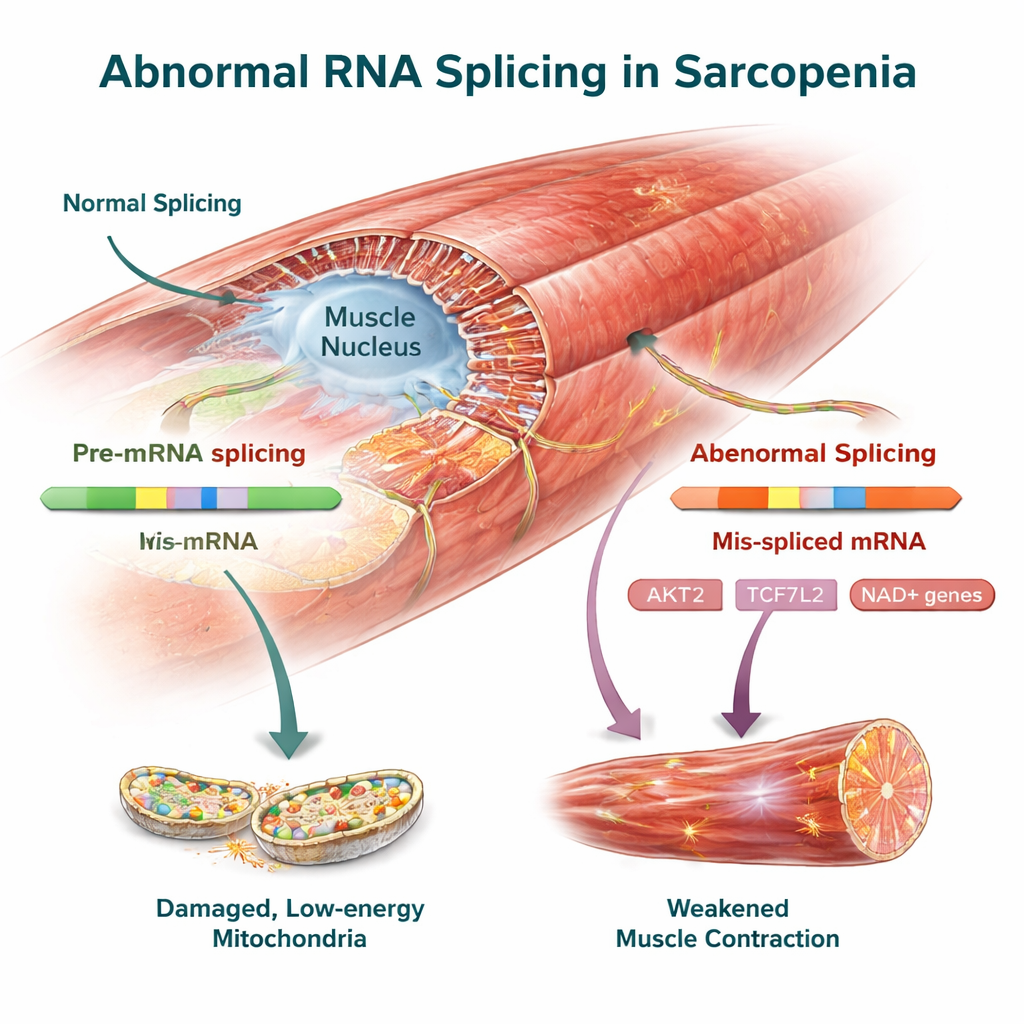
جينات رئيسية للتحكم بالعضلات كأهداف علاجية محتملة
من بين التغيرات العابرة للأنواع كانت عدة جينات مرتبطة بالفعل بصحة العضلات. أظهر AKT2، منظم مركزي للنمو وبناء البروتين في العضلات، تحولات اقتران مميزة في كل من البشر والفئران قد تضعف قدرته على الحفاظ على كتلة العضلات. حملت TCF7L2، جزء من مسار إشارات Wnt، إلى جانب FMNL2 وUSP40، التي تساعد على تنظيم الهيكل الداخلي للعضلة ومراقبة جودة البروتين، أيضًا نسخ RNA متغيرة. أكد الفريق هذه التغيرات في الاقتران تجريبيًا في عضلات الفأر، مما يعزز الحجة بأنها سمات حقيقية للمرض وليست أخطاء ناتجة عن تحليل البيانات.
ماذا يعني هذا للوقاية من الهشاشة
لغير المتخصصين، الرسالة هي أن الساركوبينيا ليست مجرد عضلات «تبلى» أو جينات تُشغّل أو تُطفأ. إنها تتضمّن أيضًا سوء تحرير واسع النطاق لرسائل الـRNA التي توجه كيف تصنع خلايا العضلات وتحافظ على آلياتها، وخصوصًا الأنظمة التي تولد الطاقة وتحسّ بالإجهاد. وبما أن الاقتران يمكن، من الناحية النظرية، تصحيحه بأدوية RNA مصممة بدقة، فإن أخطاء الاقتران المحافظة المكتشفة هنا—لا سيما في جينات مثل AKT2 وTCF7L2—تقدّم مجموعة جديدة من المؤشرات لعلاجات قد تساعد العضلات المسنة على الحفاظ على قوتها لفترة أطول.
الاستشهاد: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
الكلمات المفتاحية: الساركوبينيا, شيخوخة العضلات, اقتطاع الـRNA, الميتوكوندريا, AKT2