Clear Sky Science · ar
نموذج ظاهري لاستقرار ترانسثيريتين
لماذا هذا مهم للمرضى والأسر
أميلويدوزيس الترنسثيريتين حالة خطيرة ينفك فيها بروتين دموي طبيعي، الترنسثيريتين (TTR)، وتكوّن شظاياه رواسب ضارة في القلب والأعصاب. تهدف أدوية جديدة مثل تافاميديس وأكوراميديس إلى إبقاء هذا البروتين في شكله الآمن ذي الأربع وحدات، وقد حسّنت بالفعل النتائج للعديد من المرضى. ومع ذلك يواجه الأطباء أثرًا محيّرًا لدى المرضى المعالجين: مستويات TTR في الدم ترتفع بأكثر من 30%، وليس واضحًا سبب ذلك. تستخدم هذه الورقة نموذجًا مبسطًا قائمًا على الرياضيات لاستكشاف ما قد يحدث داخل الجسم وما يعنيه ذلك بشأن كيفية عمل هذه الأدوية فعليًا. 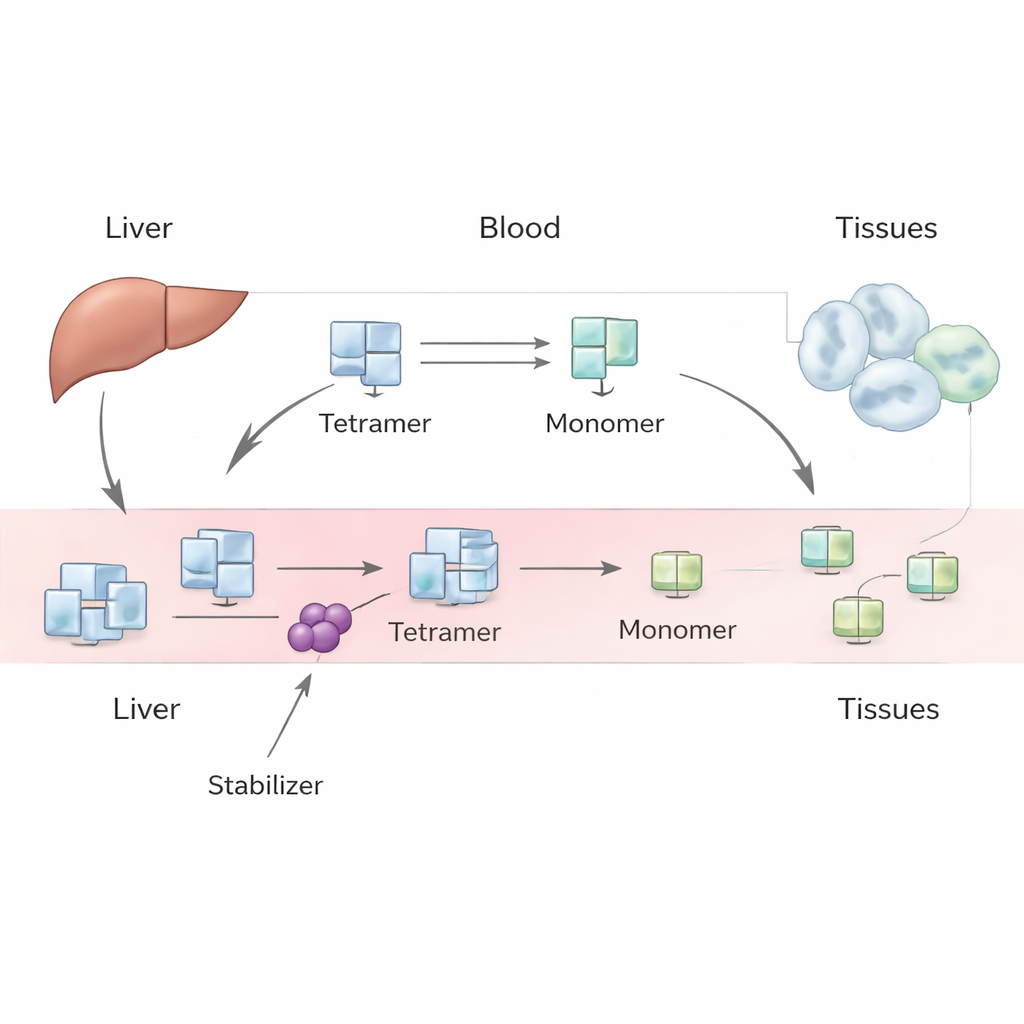
بروتين يمكن أن يساعد أو يؤذي
يُنتَج TTR أساسًا في الكبد ويتداول في الدم عادةً كمجموعة مستقرة من أربع وحدات متطابقة، تُعرف بالتترامر. ينقل هرمون الغدة الدرقية وفيتامين A. في ظروف معينة، بما في ذلك التقدم في السن أو طفرات جينية موروثة، قد ينفك هذا التترامر إلى وحدات مفردة، أو مونو ميرات. يمكن أن تنطوي هذه المونومرات بشكل خاطئ وتلتصق معًا مشكلة خيوط أميلويدية تضر الأنسجة وتؤدي إلى أميلويدوزيس الترنسثيريتين في القلب (اعتلال عضلة القلب) أو الأعصاب (الاعتلال العصبي). تصمم أدوية مثل تافاميديس وأكوراميديس للارتباط بالتترامر وجعله أصعب انفصالًا، مما يبطئ تقدم المرض. لكن عند بدء المرضى هذه الأدوية، ترتفع مستويات TTR المقاسة في الدم بصورة موثوقة، وهذه الزيادة أكبر مما توحي به تجارب المختبر البسيطة.
بناء صورة بسيطة لنظام معقد
يتعامل المؤلفون مع هذا اللغز عبر نموذج ظاهري—يركز على السلوك الكلي القابل للملاحظة بدل التفاصيل المجهرية كلها. في إطارهم، تنتج الكبد تترامرات TTR بمعدل ثابت تدخل بعدها مجرى الدم. حالما تكون في الدوران، يمكن أن تنفصل التترامرات إلى مونو ميرات وتعاود التجمع، ويمكن حذف كل من التترامرات والمونومرات من الدم عبر الالتهام الخلوي والتحلل. بكتابة معادلتين للتوازن الكتلي للتترامرات والمونومرات، يستكشف الفريق سيناريوهات مختلفة: واحد تعود فيه المونو ميرات في الغالب لتكوين التترامرات، وآخر تُزال فيه بسرعة، وحالة وسطى يكون فيها كلا العمليتين مهمتين. يستخدمون دراسات تتبع بشرية تاريخية وبيانات مختبرية حديثة لتقدير كميات رئيسية، مثل سرعة إزالة التترامرات، وسرعة انفصالها، ومدى قوة تأثير الأدوية في إبطاء هذا التفكك.
لماذا تثبيت التترامر وحده لا يكفي
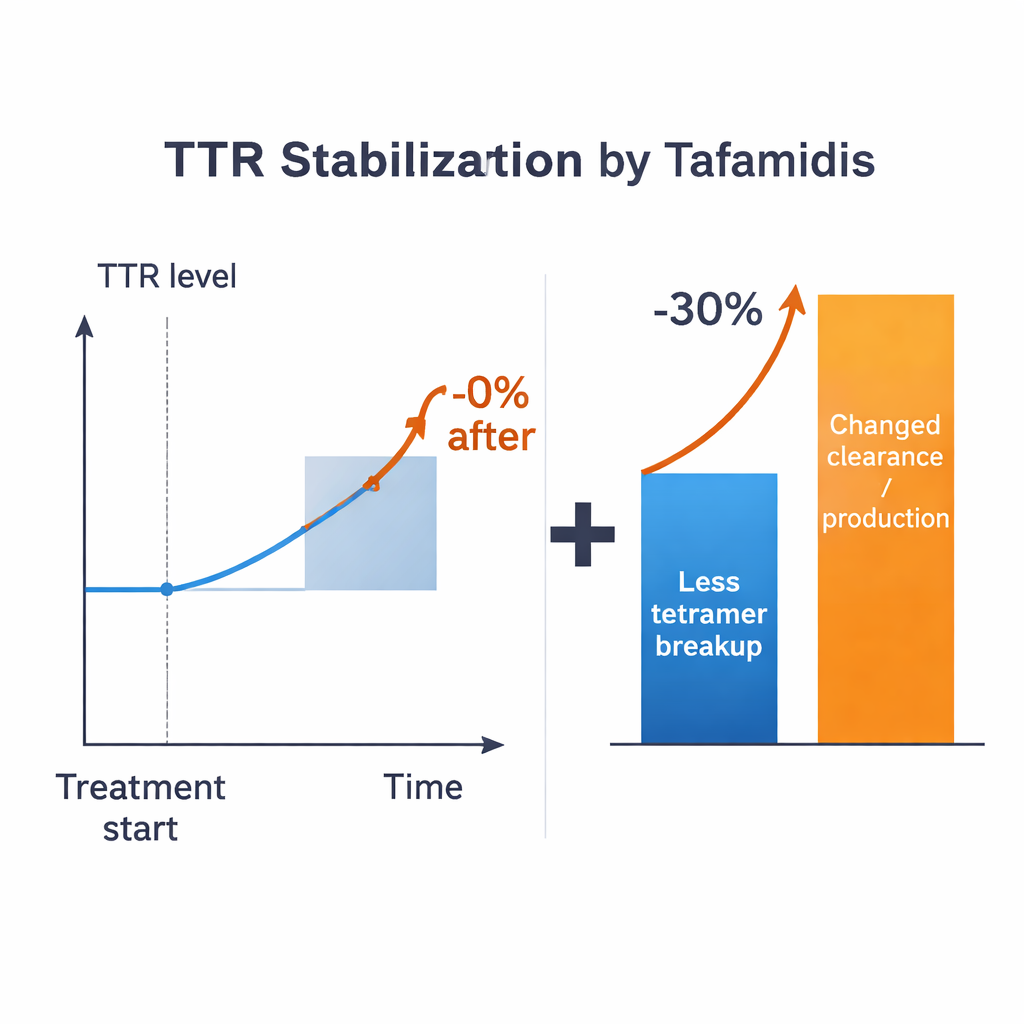
مسلحين بهذه التقديرات، يطرح الباحثون سؤالًا مباشرًا: إذا كان الدواء قادرًا على منع تفكك التترامرات تمامًا، كم سترتفع مستويات TTR في الدم؟ عبر جميع النظم المعقولة، تكون الإجابة متواضعة—على ترتيب 15% كحد أقصى للقيم النموذجية للمعاملات، وغالبًا أقل، اعتمادًا على كيفية تعامل النظام مع المونو ميرات. هذا بعيد جدًا عن الزيادة >30% التي لوحظت سريريًا لدى المرضى المعالجين. يبقى التباين قائمًا حتى مع السماح بشكوك سخية في المعاملات المعروفة. وبالتالي يقترح النموذج أن إبطاء تفكك التترامر وحده لا يفسر الأثر السريري الكامل. يجب أن تكون عمليات أخرى تتحكم في سرعة تصنيع TTR أو التقاطه داخل الخلايا أو تحلّله قد تغيرت أيضًا عند وجود أدوية التثبيت.
دلائل من مستويات الدواء وتجارب ذكية
لربط تعرض الدواء بسلوك TTR، يجمع المؤلفون نموذج حرائك دوائية بسيط لتافاميديس (كيفية تحرك الدواء في الجسم مع الزمن) مع اختبارات متخصصة "تبادل الوحدات الفرعية". في هذه التجارب، تُخلَط تترامرات TTR الموسومة وغير الموسومة في بلازما بشرية، ويكشف التبادل التدريجي للوحدات الفرعية عن تواتر انفصال التترامرات. قياس هذه العملية عند تراكيز دوائية مختلفة يعطي رابطًا مباشرًا مستندًا إلى البيانات بين مستوى تافاميديس والاستقرار الفعّال للتترامر، من دون الحاجة لمعرفة كمية الدواء المرتبطة بالألبومين أو هرمون الغدة الدرقية. هذا الرابط الظاهري يدخل النموذج ويتجاوز بوضوح العديد من المجهولات البيوكيميائية. ومع ذلك، حتى مع هذه الميزة، تقصي الحسابات ارتفاع TTR المتوقع ليظل نحو نصف الزيادة السريرية المرصودة، مما يعزز الفكرة بأن تغييرات في الإزالة أو الابتلاع الخلوي أو التحلل أو حتى التوليف يجب أن تكون جزءًا من القصة.
ماذا يعني ذلك للمضي قدمًا
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن هذه الأدوية المثبتة تفعل على الأرجح أكثر من مجرد "لصق" تترامرات TTR معًا. من المرجح أنها تؤثر أيضًا في كيفية إنتاج الجسم للبروتين أو إزالته أو إعادة تدويره. يجادل المؤلفون بأن النماذج البسيطة والشفافة مثل نموذجهم قوية لأنها تكشف عن مثل هذه الفجوات في فهمنا وتشير إلى تجارب ملموسة—على سبيل المثال، قياس مباشرة لسرعة إزالة المونو ميرات، أو مدى سرعة ابتلاع الأشكال المختلفة لـTTR من قبل الخلايا، أو ما إذا كان يُعامل TTR المرتبط بالدواء بصورة مختلفة عن البروتين غير المرتبط. إجابات أفضل على هذه الأسئلة لن تعمل فقط على تحسين علاج أميلويدوزيس الترنسثيريتين، بل قد تكشف أيضًا قواعد عامة عن أمراض أخرى تتحول فيها بروتينات طبيعية إلى تكتلات ضارة.
الاستشهاد: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
الكلمات المفتاحية: أميلويدوزيس الترنسثيريتين, تثبيت البروتين, تافاميديس, نمذجة الحرائك الدوائية, أمراض الأميلويد