Clear Sky Science · ar
التداخل بين التحلل الذاتي وp38 MAPK أثناء موت الخلايا المحفَّز بالسالينوميسين في ميلانوما مقاومة للسيزبلاتين
لماذا يهم هذا البحث
تُعد الميلانوما واحدة من أخطر أنواع سرطان الجلد، ويرجع ذلك جزئياً إلى أن الأورام كثيراً ما تتعلم تجاهل أدوية العلاج الكيميائي القياسية مثل السيزبلاتين. تستقصي هذه الدراسة ما إذا كان مضاد حيوي غير عادي يُدعى سالينوميسين قادراً على اختراق تلك المقاومة، وتغوص في آليات إعادة التدوير الخلوية وأنظمة الاستجابة للإجهاد لفهم كيفية عمل الدواء. لأي شخص مهتم بسبب عودة بعض السرطانات بعد العلاج—وكيف يمكننا التفوق عليها—يقدّم هذا العمل نافذة على قرارات البقاء أو الموت الخفية التي تتخذ داخل خلايا الورم.
عندما تتوقف خلايا السرطان عن الاستجابة للعلاج
السيزبلاتين دواء فعّال يُستخدم ضد العديد من الأورام الصلبة، لكن خلايا الميلانوما كثيراً ما تتكيّف وتصبح أصعب في القتل. بنى الباحثون سلالة خلوية لميلانوما الفأر تم تدريبها على مقاومة السيزبلاتين ثم اختبروا عليها السالينوميسين. في الأطباق المختبرية، قلّلت جرعات متزايدة من السالينوميسين عدد خلايا الميلانوما الحية بشكل حاد، وأطلقت علامات كلاسيكية لموت الخلايا المبرمج، وألغت قدرتها على تكوين مستعمرات جديدة حتى بعد تعرّض قصير. في الفئران الحاملة لأورام ميلانوما مقاومة للسيزبلاتين، أدت حقن السالينوميسين إلى إبطاء النمو بشكل ملموس، مما قلّص حجم الورم ووزنه دون سمّية ظاهرة. تقترح هذه النتائج مجتمعة أن السالينوميسين قادر على استهداف خلايا الميلانوما التي لم تعد تستجيب للعلاج الكيميائي القياسي. 
إجهاد خلوي، موجات كالسيوم ونظام إعادة تدوير تحت ضغط
لكي يعرف الفريق ما الذي يفعله السالينوميسين داخل الخلية، ركّز على الشبكة الإندوبلازمية، متاهة غشائية تساعد على طي ومعالجة البروتينات الجديدة. يتصرف السالينوميسين مثل ناقل أيونات ويعطّل تدفّق الجسيمات المشحونة عبر الأغشية، ما قد يسبّب خللاً في عمل هذا العضو الخلوي. رصد الباحثون تنشيطاً قوياً لعلامات بروتينية تظهر عندما تتعرّض آليات طي البروتين في الخلية لضغط. في الوقت نفسه، كشفوا عن تيّار من الكالسيوم يتسرّب من الشبكة الإندوبلازمية إلى الوسط المحيط ونحو الميتوكوندريا، مصانع طاقة الخلية. عندما عطّلوا قدرة الميتوكوندريا على امتصاص هذا الكالسيوم، ماتت الخلايا بسهولة أكبر، ما يشير إلى أن الميتوكوندريا تعمل عادةً كعازل لتأخير الموت أثناء إجهاد السالينوميسين.
إعادة التدوير الذاتي تتحول إلى اختناق قاتل
تعتمد الخلايا على عملية توصف غالباً بأنها «الالتقام الذاتي» للبقاء في ظروف صعبة: تغلف المواد التالفة في حويصلات صغيرة وترسلها إلى مقصورات حمضية للتفكيك وإعادة الاستخدام. عزّز السالينوميسين بقوة المراحل الأولية لهذه المسار، مرفوعاً مستويات البروتينات التي تدفع تشكيل هذه الحويصلات. لكن الأهم أن الفريق وجد أن خطوة التنظيف النهائية كانت معطّلة. تراكمت العلامات التي كان من المفترض أن تُهضم بدلاً من ذلك، وأظهرت الصور المجهرية هياكل شبيهة بالفراغات كبيرة لم تندمج بشكل صحيح مع الجسيمات الحالّة، وحدات الهضم في الخلية. أشارت اختبارات إضافية إلى أن أغشية الجسيمات الحالّة أصبحت مسرَّبة ونشِطت إنزيمات هضمية معينة في المكان الخطأ. النتيجة هي نوع من اختناق خلوي: تستمر حزم إعادة التدوير في التكوّن لكنها لا تُزال بكفاءة، مما قد يحوّل عملية كانت وقائية إلى مُحرّك لموت الخلية.
مفتاح إشارة الإجهاد الذي يمكن توجيهه ضد الورم
قطعة أخرى من اللغز هي عائلة من الإنزيمات المستشعِرة للإجهاد والمعروفة مجتمعة باسم بروتينات كيناز الـ MAP. فعّل السالينوميسين ثلاثة فروع من هذا النظام، لكن فرعاً واحداً على وجه الخصوص، المسمى p38، برز بوضوح. عندما عطّل الباحثون p38، قتل السالينوميسين عدداً أكبر من خلايا الميلانوما وتسبب في زيادة لافتة في عدد وحجم الفراغات السيتوبلازمية. كان لتثبيط إنزيم معتمد على الكالسيوم يُدعى كالباين تأثير مشابه، سواء على تراكم الفراغات أو على البقاء على المدى الطويل. على النقيض، قلّل دواء يعزّز إعادة التدوير بكفاءة أكبر (الرابامايسين) من التراكم الضار لحويصلات إعادة التدوير وحمى الخلايا من تأثير السالينوميسين. تشير هذه التجارب إلى أنّه تحت ضغط السالينوميسين، يساعد كل من p38 والكالباين خلايا الميلانوما على استخدام استجابة إعادة تدوير بطيئة وغير كاملة كتكتيك نجاة—وأن تعطيل هذا الملجأ يجعل الدواء أكثر فتكاً. 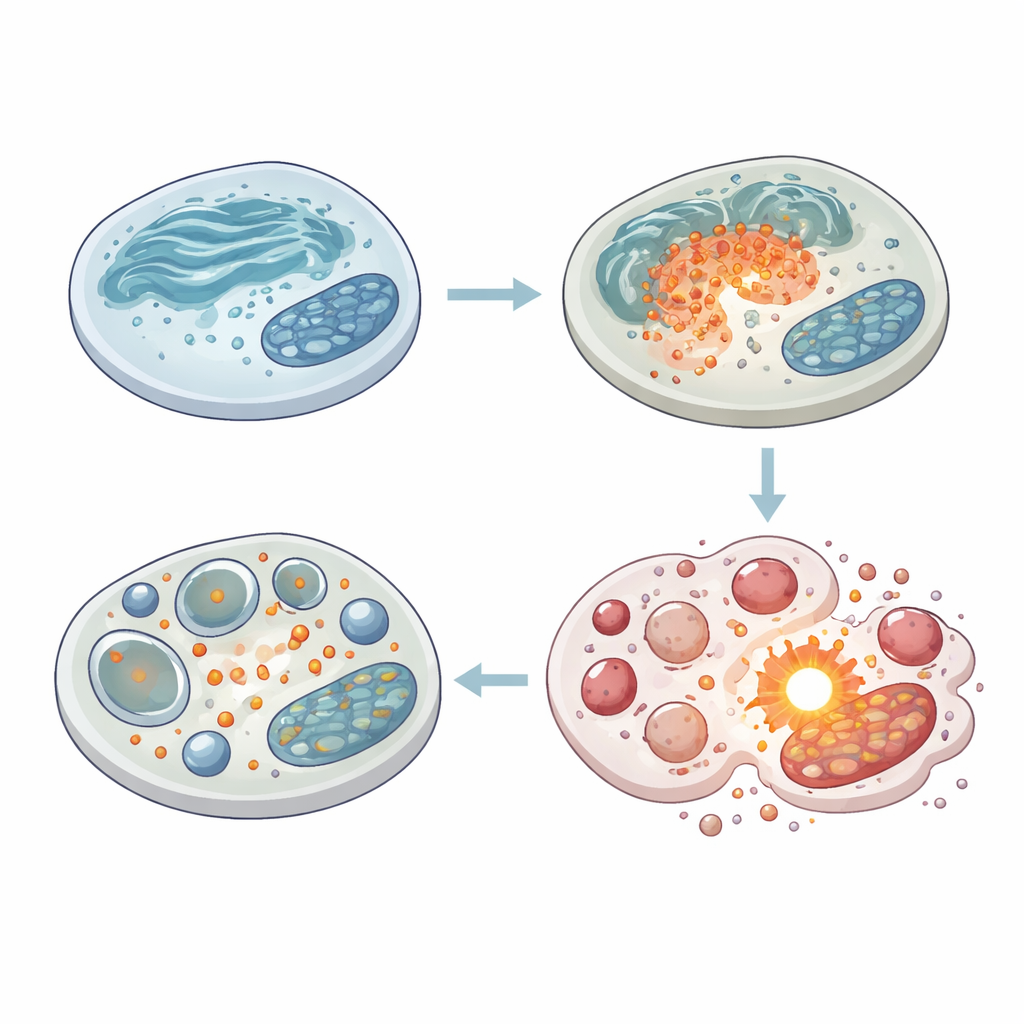
ما الذي قد يعنيه هذا لرعاية السرطان المستقبلية
بشكل عام، تصوّر الدراسة السالينوميسين كعامل ذا حدين يدفع خلايا الميلانوما المقاومة للسيزبلاتين إلى إجهاد داخلي شديد، ويغمرها بالكالسيوم، ويعطّل نظامها للتعامل مع الفضلات، وفي النهاية يدفعها نحو الموت المبرمج. في الوقت نفسه، تحاول الخلايا الدفاع عن نفسها باستخدام استجابة إعادة التدوير الموجّهة بواسطة p38 ومسارات نجاة أخرى. للمرضى، الرسالة العملية هي أن السالينوميسين—أو نظائر محسّنة منه—قد تُقرَن يوماً ما بأدوية تعطل هذه مسارات النجاة، مثل مثبطات p38 أو مانعات التحلل الذاتي، لإسقاط خلايا الميلانوما العنيدة بشكل انتقائي مع استخدام جرعات أدنى من كل دواء. على الرغم من أن العمل الكثير لا يزال مطلوباً قبل أن تصل هذه الاستراتيجية إلى العيادة، تقدّم الدراسة خارطة طريق مفصّلة عن نقاط الضعف التي قد تستغلها العلاجات التوافقية.
الاستشهاد: Tyagi, M., Patro, B.S. Interplay between autophagy and p38 MAPK during salinomycin-induced cell death in cisplatin-resistant melanoma. Sci Rep 16, 9640 (2026). https://doi.org/10.1038/s41598-025-34796-5
الكلمات المفتاحية: ميلانوما, مقاومة الأدوية, سالينوميسين, التحلل الذاتي, العلاج التوافقي