Clear Sky Science · ar
تنشيط مستقبلات M1mAChR يحسن العجز في التعلم المكاني والذاكرة لدى الفئران المعرضة لنقص الأكسجة المتقطع المزمن
لماذا يؤثر التنفّس الليلي على ذاكرتك
يتوقف العديد من الأشخاص المصابين بانقطاع التنفّس أثناء النوم الانسدادي عن التنفّس مرارًا أثناء الليل، ما يسبب هبوطات حادة في مستوى الأكسجين في الدم. بخلاف الشخير الصاخب والنعاس خلال النهار، يمكن لهذه النوبات القصيرة الشبيهة بالاختناق أن تتلف بهدوء مناطق في الدماغ مسؤولة عن التعلّم والذاكرة. استخدمت هذه الدراسة نموذجًا من الفئران لتطرح سؤالًا بسيطًا لكنه مهم: هل يمكن لتعزيز نوع واحد محدد من الإشارات الدماغية بشكل لطيف أن يحمي دوائر الذاكرة من الضرر الناجم عن تكرار نوبات انخفاض الأكسجين؟
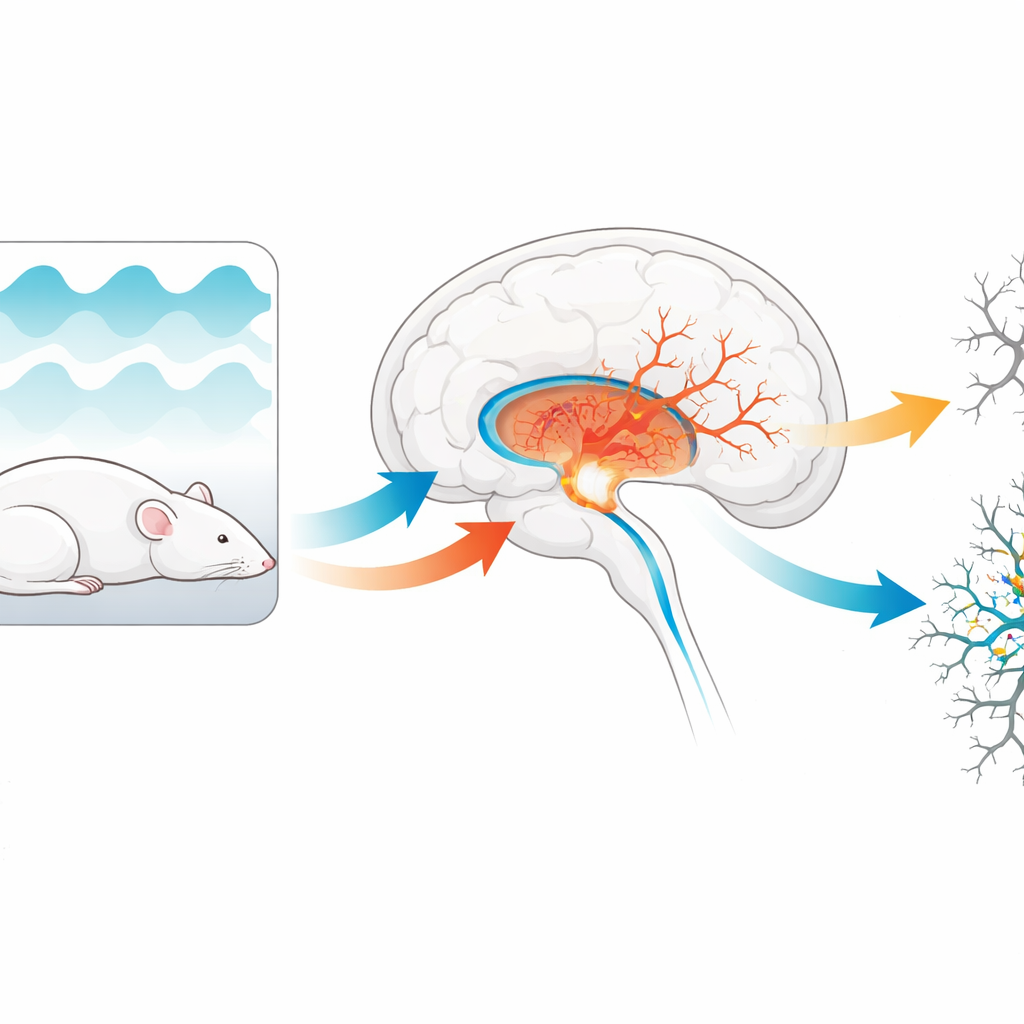
النوم، هبوط الأكسجين، ومركز ذاكرة ضعيف التحمل
يتّسم انقطاع التنفّس أثناء النوم الانسدادي بنقص الأكسجة المتقطع المزمن—دورات سريعة من انخفاض وعودة الأكسجين. الحُصين، بنية عميقة في الدماغ حاسمة لتشكيل الذكريات المكانية واليومية، حساس بشكل خاص لهذا النوع من الضغط. أظهرت أعمال سابقة أن ظروفًا شبيهة بالاختناق يمكن أن تقلّل من كثافة الخلايا العصبية وتعطل المحادثات الكيميائية بينها. برز نظامان إشارتيان في هذه القصة: عائلة من المستقبلات التي تستجيب للمرسال الأسيتيل كولين (المهمّة للانتباه والذاكرة) ومرحل داخلي يسمى مسار JAK2/STAT3 الذي يساعد الخلايا على التأقلم والبقاء في مواجهة الضغط.
اختبار ضغط شبيه بالانقطاع التنفّسي في المختبر
لتقليد انقطاع التنفّس، وضع الباحثون فئرانًا سليمة في غرفة نزلت وعلت فيها مستويات الأكسجين مرارًا طوال ثماني ساعات يوميًا لمدة أربعة أسابيع. تعرضت بعض الحيوانات لدورات الأكسجين فقط، بينما تلقت مجموعات أخرى أدوية إما تمنع مرحل JAK2/STAT3 أو تنشّط مستقبل M1 للموسكاريني من الأسيتيل كولين، وهو مفتاح حساس للأسيتيل كولين في الحُصين. بعد ذلك قيّمت الفريق قدرة الفئران على تعلّم موقع منصة مخفية في متاهة مائية ثم تذكّر موقعها لاحقًا. كما فحصوا أنسجة الدماغ لحساب الخلايا العصبية ولمعرفة كمية البروتينات الرئيسية مثل مستقبل M1 وSTAT3.
ما فعله انخفاض الأكسجين للتعلّم والخلايا العصبية
واجهت الفئران المعرضة لنمط الأكسجين الشبيه بالانقطاع صعوبات في المتاهة المائية. اتّخذت مسارات أطول للعثور على المنصة وعندما أُزيلت قضت وقتًا أقل في البحث في المنطقة الصحيحة—علامات على تراجع التعلّم المكاني والذاكرة. تحت المجهر، كانت خلاياهم العصبية في الحُصين أقل عددًا وأكثر فوضوية وأظهرت مظاهر ضرر. على المستوى الجزيئي، انخفض كل من إجمالي STAT3 وشكله النشط، وكذلك كمية مستقبل M1 في الحُصين. باختصار، خفّضت نوبات انخفاض الأكسجين المتكررة فعالية المسارات التي يُعتقد أنها تساعد الخلايا العصبية على مواجهة الضغوط ودعم الذاكرة.
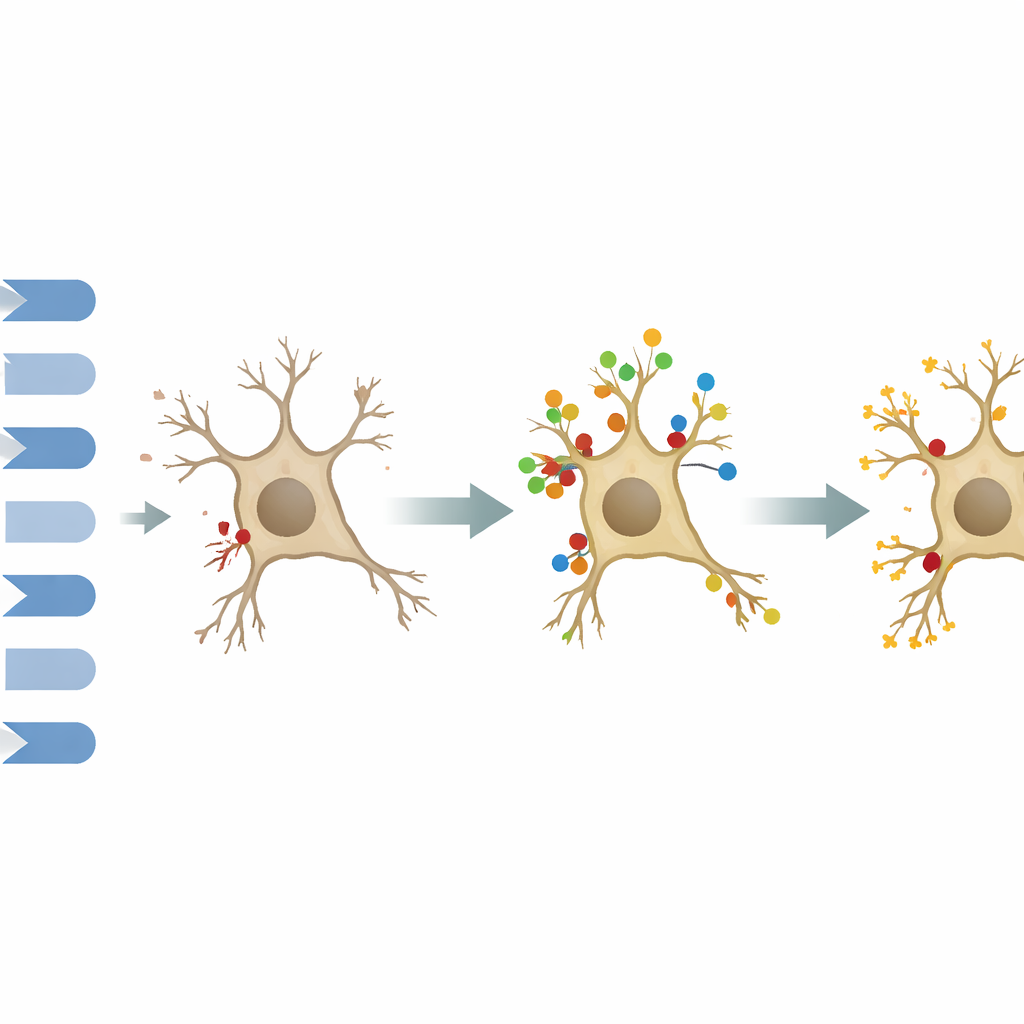
مفتاح وقائي يعتمد على وجود مسار معين
أعاد تنشيط مستقبل M1 بواسطة دواء انتقائي، VU0364572، جزءًا من هذه المشكلات. تعلّمت الفئران المعالجة المتاهة بسرعة أكبر وبحثت بدقة أكبر عن موقع المنصة السابق، وأظهرت أنسجتهم الحُصينية بنية محفوظة بشكل أفضل ومستويات أعلى من مستقبل M1. بالمقابل، فإن حجب JAK2—المنشط الرئيس لمسار STAT3—بواسطة الدواء AG490 لم يحسّن السلوك وحتى ألغى فوائد تنشيط M1 عندما أُعطي الدواءان معًا. ومن المثير للاهتمام أن أيًا من العلاجين لم يستعد مستويات بروتين STAT3 في هذه الظروف، ما يشير إلى أن ما يهم قد يكون سلامة مسار الإشارة بدلاً من كميته الإجمالية.
ماذا يعني هذا للأشخاص القلقين بشأن الشخير والذاكرة
للقارئ العام، الخلاصة أن استجابة الدماغ لتقلبات الأكسجين أثناء النوم ليست ثابتة؛ يمكن دفعها نحو الضرر أو الحماية اعتمادًا على المفاتيح الكيميائية المفعّلة. في هذه الدراسة على الفئران، أضر نقص الأكسجين المتقطع المزمن دوائر الذاكرة وخفّض كلًا من مستقبل سطحي رئيسي ومرحل الاستجابة للضغط الداخلي. ساعدت زيادة نشاط مستقبل M1 الفئران على التفكير والتذكّر بشكل أوضح رغم ضغط الأكسجين، لكن ذلك لم يحدث إلا عندما ظلّ مسار JAK2/STAT3 سليمًا. ومع أن هذه النتائج ما زالت بعيدة عن أن تصبح علاجًا للبشر، فهي تبرز استراتيجية واعدة: الجمع بين رعاية فعّالة لانقطاع التنفّس وأدوية تدعم شبكات الذاكرة الضعيفة، بدلاً من التركيز على الأكسجين وحده.
الاستشهاد: Huang, Q., Hu, C., Liu, H. et al. Activation of M1mAChR’s improves spatial learning and memory deficits in rats exposed to chronic intermittent hypoxia. Sci Rep 16, 8836 (2026). https://doi.org/10.1038/s41598-025-34689-7
الكلمات المفتاحية: انقطاع التنفّس أثناء النوم الانسدادي, نقص الأكسجة المتقطع, الحُصين, التعلّم والذاكرة, مستقبلات الأسيتيل كولين