Clear Sky Science · ar
جسيمات نانوية محملة بسكّريات عنب الثعلب تكبح تقدم سرطان الثدي عبر تثبيط تعبير YAP1 لتحث على الفيروبتوز وتغير التمثيل الطاقي
مركبات التوت تلتقي بسرطان الثدي
يعرف كثير من الناس توت الڭوجي كـ«طعام خارق» في الشاي ومزيج الوجبات الخفيفة. تتجاوز هذه الدراسة ذلك بكثير، وتستقصي ما إذا كان يمكن تحويل سلاسل السكر الرئيسية من هذه الثمار إلى دواء دقيق وصغير ضد سرطان الثدي. من خلال دراسة سلوك هذه الجزيئات الطبيعية عند تغليفها داخل جسيمات نانوية وتسليمها إلى خلايا الثدي في المختبر، يكشف الباحثون نهجًا جديدًا لدفع الخلايا السرطانية نحو الانهيار الذاتي مع جعل الخلايا الطبيعية أقل عرضة للتحول الخبيث.
تشغيل وإيقاف مفتاح النمو
في صلب العمل يوجد بروتين يدعى YAP1، يعمل كمفتاح نمو داخل الخلايا. عندما يكون YAP1 مفرط النشاط، تبدأ خلايا الثدي الطبيعية في التصرف بشكل أقرب للخلايا السرطانية: تتكاثر أسرع، تقاوم الموت الخلوي، تعيد ترتيب هيكلها الخلوي الداخلي، وتزداد قدرتها على الانغراز في الأنسجة المحيطة. أجبر الفريق خلايا ثدي طبيعية على إنتاج كمية زائدة من YAP1 ولاحظ كل هذه التغيرات الخطرة، إلى جانب زيادة في مصانع الطاقة الخلوية، الميتوكوندريا. عند معالجة الخلايا ببلميرات Lycium barbarum (LBPs) المستخرجة من توت الڭوجي، تراجعت هذه السلوكيات الشبيهة بالسرطان بشدة وانخفضت مستويات YAP1. بعبارة أخرى، استطاعت سكريات الثمرة خفض هذا المفتاح الذي يحفز النمو.
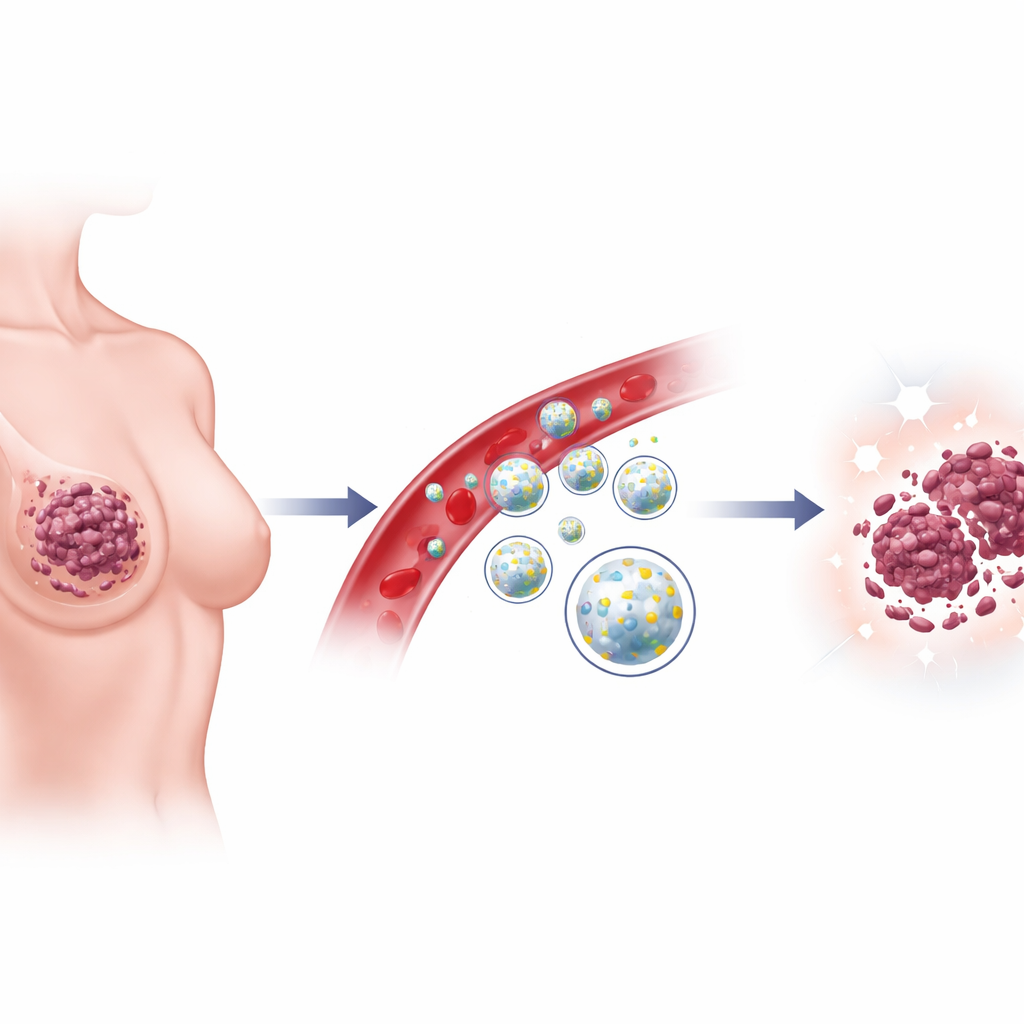
دفع الخلايا السرطانية نحو نوع خاص من الموت
ثم انتقل العلماء إلى خلايا سرطان الثدي العدوانية. هنا أيضًا ارتبطت المستويات العالية من YAP1 بنمو سريع، ومقاومة قوية للموت الخلوي، وقدرة كبيرة على الانغراز. أبطأت معالجة LBPs انقسام الخلايا، أضعفت السقالة الداخلية للخلايا، وقللت الانغراز. والأهم من ذلك أن المركبات وجهت الخلايا السرطانية نحو الفيروبتوز، وهو شكل من أشكال الموت الخلوي يُغذَّى بالحديد وتلف مركبات الدهن في أغشية الخلايا. انخفضت مؤشرات الحماية التقليدية ضد هذا النوع من الموت، بينما ارتفعت الإشارات التي تفضّله وتراكم الحديد داخل الخلايا. إن خفض YAP1 باستخدام أدوات جينية أحدث تأثيرات مماثلة، وإضافة تلك الأدوات إلى LBPs زاد التأثير، مما يربط عمل سكريات الثمرة ارتباطًا وثيقًا بهذا المفتاح الواحد للنمو.
بناء ناقل توصيل أذكى
لوحدها، ليست LBPs أدوية مثالية: فهي جزيئات كبيرة محبة للماء تتحلل بسهولة ولا تنتقل بكفاءة في الجسم. لتجاوز هذا العائق، غلف الباحثون هذه السكريات في كرات دقيقة مصنوعة من بلاستيك قابل للتحلل حيويًا يُدعى PLGA، مكونين جسيمات نانوية محملة بـ LBPs (LBPs NPs). كانت هذه الجسيمات متجانسة في الحجم، مستقرة في المحاليل، وتم ابتلاعها بسهولة بواسطة خلايا سرطان الثدي، حيث تراكمت داخل جسد الخلية. مقارنةً بالـ LBPs الحرة، شكل الجسيمات النانوية أبطأ نمو الخلايا السرطانية بشكل أقوى، عطل سقالتها الداخلية، خفّض غزوها، وزاد نسبة الخلايا التي تخضع للموت المبرمج. كذلك أدت الجسيمات النانوية عملًا أفضل في خفض YAP1 وشريكه TAZ، بينما رفعت النسخة «المعطلة» من YAP1 الموسومة بالفوسفوريلation.
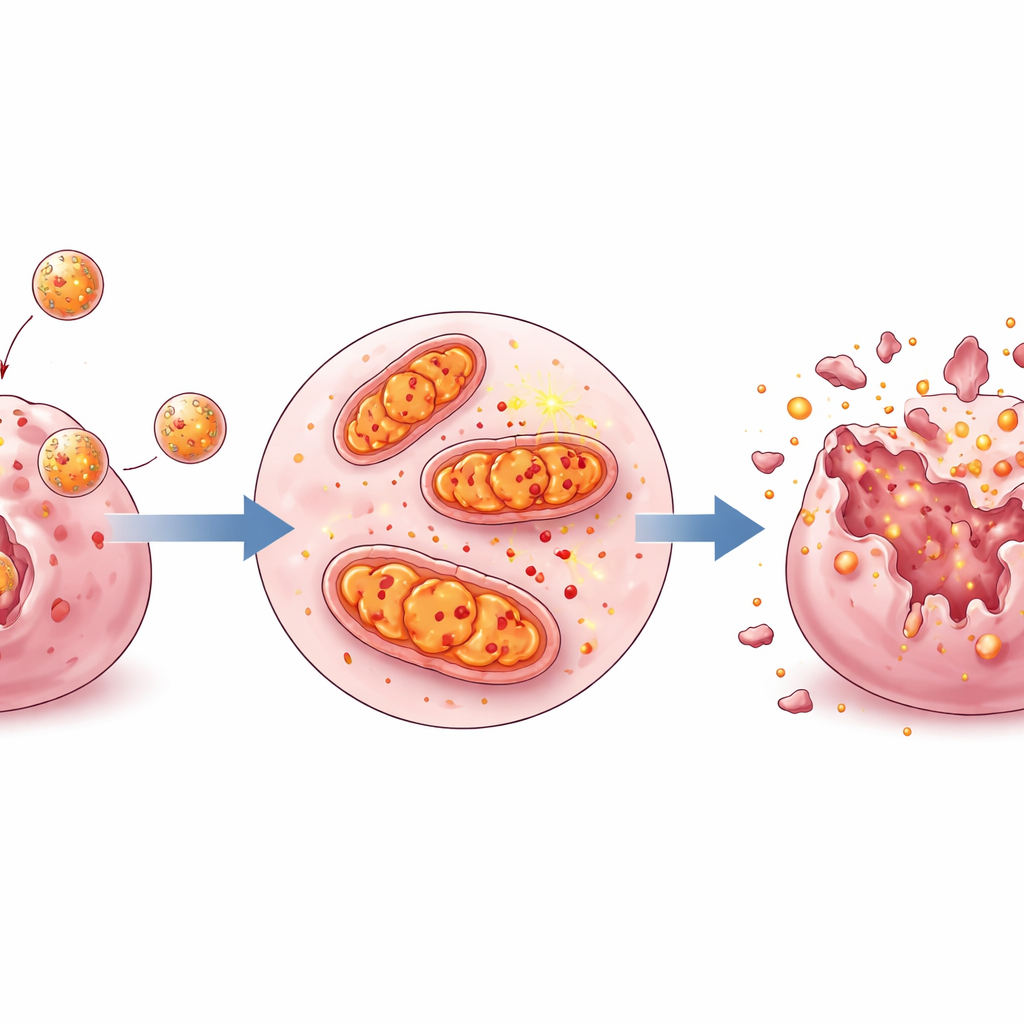
استنزاف طاقة الخلية وتحريك الحديد
عند فحص الخلايا السرطانية المعالجة، وجد الفريق أن LBPs وخاصة LBPs NPs أضعفت وظيفة الميتوكوندريا وإنتاج الطاقة. انخفضت القدرة الغشائية الميتوكوندرية، وهو مقياس رئيسي لكفاءة هذه المحطات، بعد المعالجة، وأنتجت الخلايا كمية أقل من ATP، عملة الطاقة الأساسية. في الوقت نفسه، أظهرت أصباغ وحمّرات حسّاسة للحديد تراكمًا أكبر للحديد، ممهّدة الخلايا للفيروبتوز. انخفضت البروتينات التي تحمي الخلايا عادةً من هذا الضرر المحفز بالحديد، بينما ازدادت تلك التي تعزز الضرر. عندما أضاف الباحثون مانعًا معروفًا للفيروبتوز، انعكست هذه التغيرات جزئيًا، مؤكدة أن الجسيمات النانوية كانت بالفعل تدفع هذا الشكل المحدد من الموت الخلوي.
ماذا قد يعني ذلك للرعاية المستقبلية
بمفهوم مبسط، تقترح الدراسة أن سكريات توت الڭوجي المصممة بعناية والمقدمة عبر جسيمات نانوية يمكن أن تطفئ محرك نمو رئيسي في خلايا الثدي، تجفف طاقة الخلايا السرطانية، وتدفعها نحو انهيار مُتحكم فيه مدفوع بالحديد. أُجريت هذه الدراسة في أطباق خلوية، وليست في حيوانات أو مرضى، لذا فهي خطوة مبكرة لإثبات الفكرة وليست علاجًا جاهزًا. ومع ذلك، تشير إلى مستقبل يمكن فيه إقران المركبات الطبيعية بأنظمة توصيل ذكية لتعطيل آليات نمو السرطان بشكل انتقائي وتفعيل برامج الانتحار الذاتي المدمجة داخله.
الاستشهاد: Zhao, F., Yang, S., He, T. et al. LBPs NPs suppress breast cancer progression by inhibiting YAP1 expression to induce ferroptosis and alter energy metabolism. Sci Rep 16, 9257 (2026). https://doi.org/10.1038/s41598-025-34454-w
الكلمات المفتاحية: سرطان الثدي, جسيمات نانوية, بُلميرات توت الڭوجي (سكّريات عنب الثعلب), الفيروبتوز, مسار هيبو YAP1