Clear Sky Science · ar
تثبيت مستهدف لعامل التحسس لنقص الأكسجة 1‑ألفا (HIF1A) خلال النضج المختبري لمجمعات الخلايا الحامية–البويضة البقرية يزيد معدلات الانتساخ إلى مرحلة الكيسة الأريمية
لماذا يهم تعديل استشعار الأكسجين في البويضات
تعتمد تربية الماشية الحديثة بشكل كبير على الأجنة المصنوعة في المختبر، لكن النجاح بعيد عن أن يكون مضمونا: فقط حوالي ثلث الخلايا البويضية تصل إلى مرحلة الكيسة الأريمية الحاسمة، عندما تكون جاهزة للزرع في بقرة. تطرح هذه الدراسة سؤالاً قد يبدو بسيطاً لكنه ذو صلة واسعة بتربية الحيوانات والتكاثر المساعد: إذا كنا نقلد بشكل أقرب ظروف الأكسجين المنخفض التي تتعرض لها البويضات طبيعياً داخل المبيض — عن طريق تعزيز لطيف لبروتين رئيسي مستشعر للأكسجين — هل يمكننا مساعدة المزيد من الأجنة على التطور بنجاح؟
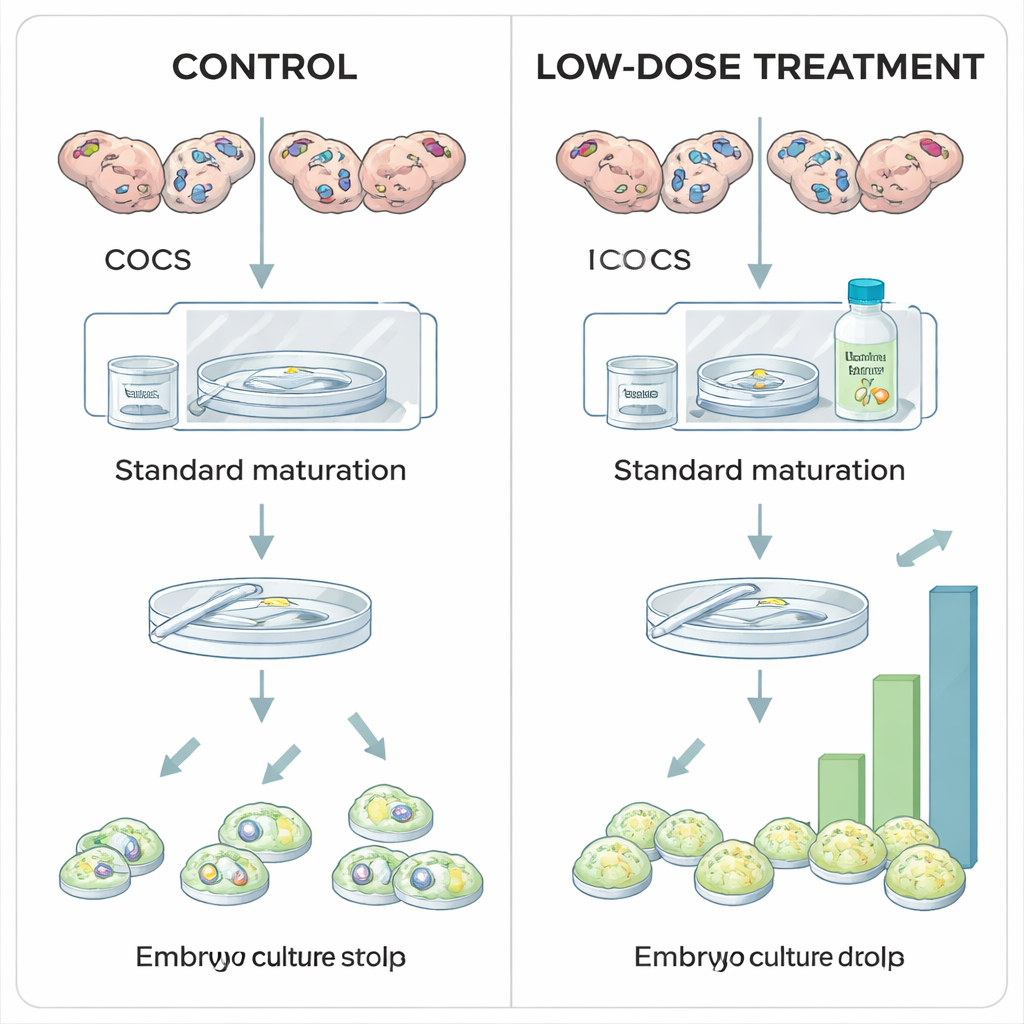
الحياة تبدأ في بيئة منخفضة الأكسجين
داخل المبيض، تُحاط كل بويضة نامية بعنقود داعم من الخلايا يعرف بالخلايا الحامية، وتشكل معاً مجمع الخلايا الحامية–البويضة. على الرغم من أن إمداد الدم إلى المبيض يزداد مع نمو الجريبات، فإن الأوعية الدموية تتوقف قبل محيط البويضة المباشر. يجب أن ينتشر الأكسجين من المسافات، مما يخلق جيباً معتدلاً منخفض الأكسجين، أو نقص الأكسجة، حول البويضة النامية. في هذه البيئة، يساعد مستشعر خلوي يُدعى HIF1A الخلايا على التكيف من خلال تعديل الأيض وإنتاج الهرمونات. أظهرت أعمال سابقة أن تعطيل HIF1A يضر بنضج البويضة ويقلص بشدة تكوين الأجنة، مما يسلط الضوء على هذا البروتين كمنسق مركزي لكفاءة البويضة — أي قدرة البويضة على الإخصاب والتطور إلى جنين سليم.
استخدام دواء لضبط حساسية البويضة للأكسجين
استكشف الباحثون ما إذا كان تثبيت HIF1A بشكل معتدل أثناء النضج المختبري للبويضات البقرية يمكن أن يعزز إنتاج الأجنة. في البروتوكولات التقليدية خارج الجسم، تُنضج مجمعات الخلايا الحامية–البويضات تحت مستويات أكسجين هواء عادية، لأسباب عملية أكثر منها بيولوجية. هنا، قُسمت البويضات المجمعة من مبايض مسالخ إلى مجموعات وعُرضت خلال فترة النضج التي استمرت 24 ساعة لجرعات مختلفة من روكسادستات، وهو دواء مستخدم بالفعل في الطب البشري لعلاج فقر الدم. يعمل روكسادستات عن طريق تثبيط عائلة من الإنزيمات تُدعى برويل هيدروكسيليزات (PHDs) التي عادة ما تضع وسمًا لـ HIF1A لتدميره عندما يتوفر الأكسجين بكثرة. من خلال تثبيط PHDs، يسمح روكسادستات بتراكم بروتين HIF1A حتى عند مستويات أكسجين أعلى، معيداً جزئياً الإشارة الخاصة بنقص الأكسجة التي ستشعر بها البويضة في الجسم الحي.
المزيد من الكيسات الأريمية بجرعة مناسبة، والضرر عند المستويات الأعلى
عندما فحص الفريق كيفية أداء البويضات والأجنة بعد المعالجة، ظهرت نمطية واضحة. لم تغير جرعة منخفضة من روكسادستات (25 ميكرومولار) عدد البويضات التي أنهت النضج أو نسبة البيوض المخصبة التي بدأت الانقسام، لكنها زادت بشكل كبير النسبة التي وصلت إلى مرحلة الكيسة الأريمية. بعبارة أخرى، لم تتأثر الخطوات المبكرة، ومع ذلك أكملت مزيد من الأجنة الرحلة الصعبة لتصبح كيسات أريمية — ما يشير إلى أن تثبيت HIF1A المعتدل يحسّن الجودة الجوهرية للبويضة. على النقيض من ذلك، خفضت أعلى جرعة (100 ميكرومولار) نسبة البويضات التي نضجت على الإطلاق، وعندما طُبق نفس المثبط لاحقاً خلال فترة زراعة الأجنة التي استمرت ثمانية أيام، قطعت الجرعات العالية تشكيل الكيسات الأريمية بشكل حاد دون تغيير الانقسام الخلوي المبكر. تشير هذه النتائج إلى أن "الكم الكافي فقط" من نشاط HIF1A خلال النضج مفيد، بينما الإفراط في الكمية أو استمرار التفعيل مضر.
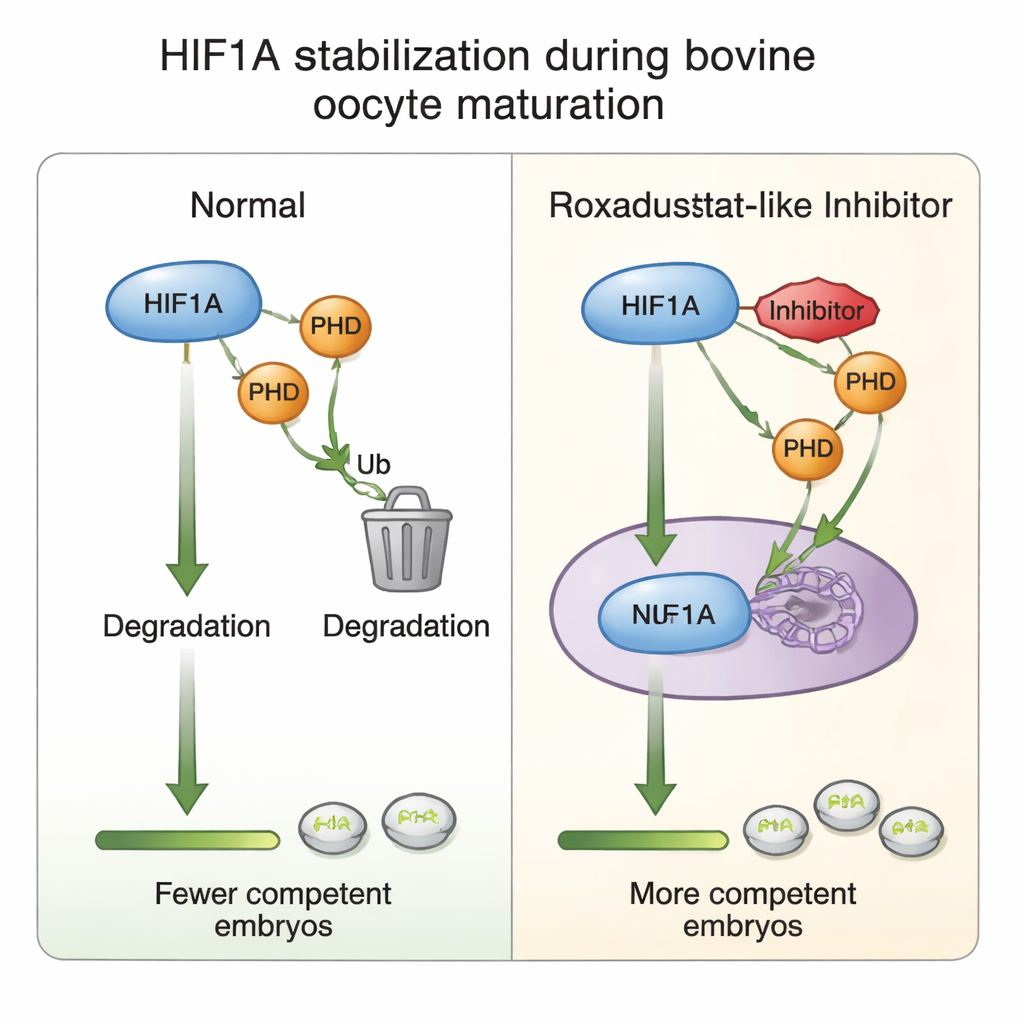
ما يحدث داخل خلايا الدعم المحيطة بالبويضة
لفهم كيف يعمل هذا الضبط الكيميائي، فحص المؤلفون خلايا الحماية التي تحيط بكل بويضة. وجدوا أن النضج عموماً يرفع نشاط جينات HIF1A، لكن إضافة روكسادستات خفضت بشكل متناقض رسالة HIF1A المرسال (mRNA) مع بقاء مستويات بروتين HIF1A ثابتة — تلميح إلى أن الخلايا قد تخفّض إنتاج الجين بمجرد أن يُثبّت البروتين بدرجة كافية، وهو نوع من المكابح المدمجة ضد الإفراط في التنشيط. ارتفعت مستويات PHD2، وهو الأكثر حساسية للأكسجين من بين إنزيمات PHD، استجابةً للدواء، مما يعزّز دوره كجزء من حلقة استشعار الأكسجين. عند الجرعات الأعلى من الدواء، انخفضت مؤشرات تكاثر الخلايا والمصفوفة اللزجة التي تساعد خلايا الحماية على التوسع حول البويضة، بما يتماشى مع الانخفاض الملحوظ في النضج وتكوين الأجنة. يدعم كل هذا الفكرة أن نشاط HIF1A المتوازن بعناية يضبط الحوار بين البويضة وخلايا الحماية الذي يؤسس للنجاح التطوري لاحقاً.
الآثار على تربية الحيوانات وما بعدها
تُظهر هذه الدراسة أن تثبيت مستهدف ولطيف لمستشعر الأكسجين في البويضة خلال نافذة النضج المختبري القصيرة يمكن أن يزيد ويستقر إنتاج الكيسات الأريمية في الأبقار بشكل ملحوظ، دون تغيير في الإخصاب أو الانقسام المبكر. من الناحية التطبيقية، قد يترجم ذلك إلى إنتاج أجنة أكثر موثوقية لبرامج التربية، باستخدام دواء موجه بدلاً من تعديلات خام في مستويات الأكسجين أو مواد كيميائية أكثر سمية. كما تبرز الدراسة درساً أوسع ذو صلة بعلاجات الخصوبة البشرية: محاكاة البيئة الدقيقة منخفضة الأكسجين في المبيض ليست مجرد مسألة خفض أو رفع الأكسجين، بل احترام توازن حساس لجزيئات الإشارة مثل HIF1A. قد يكون ضبط هذا التوازن بدقة، بدلاً من دفعه إلى أقصى الحدود، طريقاً رئيسياً نحو أجنة أكثر صحة.
الاستشهاد: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
الكلمات المفتاحية: إنتاج الأجنة في المختبر, نضج البويضة, إشارة نقص الأكسجة, تثبيت HIF1A, التكاثر البقري