Clear Sky Science · ar
مشتقات البكتين متعددة الوظائف كعوامل مضادة للسرطان في سرطان القولون والمستقيم عبر التخليق والرؤى الحاسوبية وتعديل مسارات الإشارة NRF2/HO-1 وHIF-1α وVEGF/PDGF-D
من ألياف الفاكهة إلى جزيئات مكافحة للسرطان
البكتين هو ألياف طبيعية تُعرف بشكل أساسي بتكثيف المربيات والهلام، لكن هذا المكوّن اليومي في المطبخ قد يكون أيضًا حليفًا هادئًا في مكافحة السرطان. تستكشف هذه الدراسة كيف يمكن للعلماء تعديل بنية البكتين بدقة لابتكار مركبات جديدة تُبطئ نمو خلايا سرطان القولون والمستقيم في المختبر، وفي الوقت نفسه تُخمد الإجهاد التأكسدي الضار وتُقطع الإمداد الدموي الذي تحتاجه الأورام للنمو.
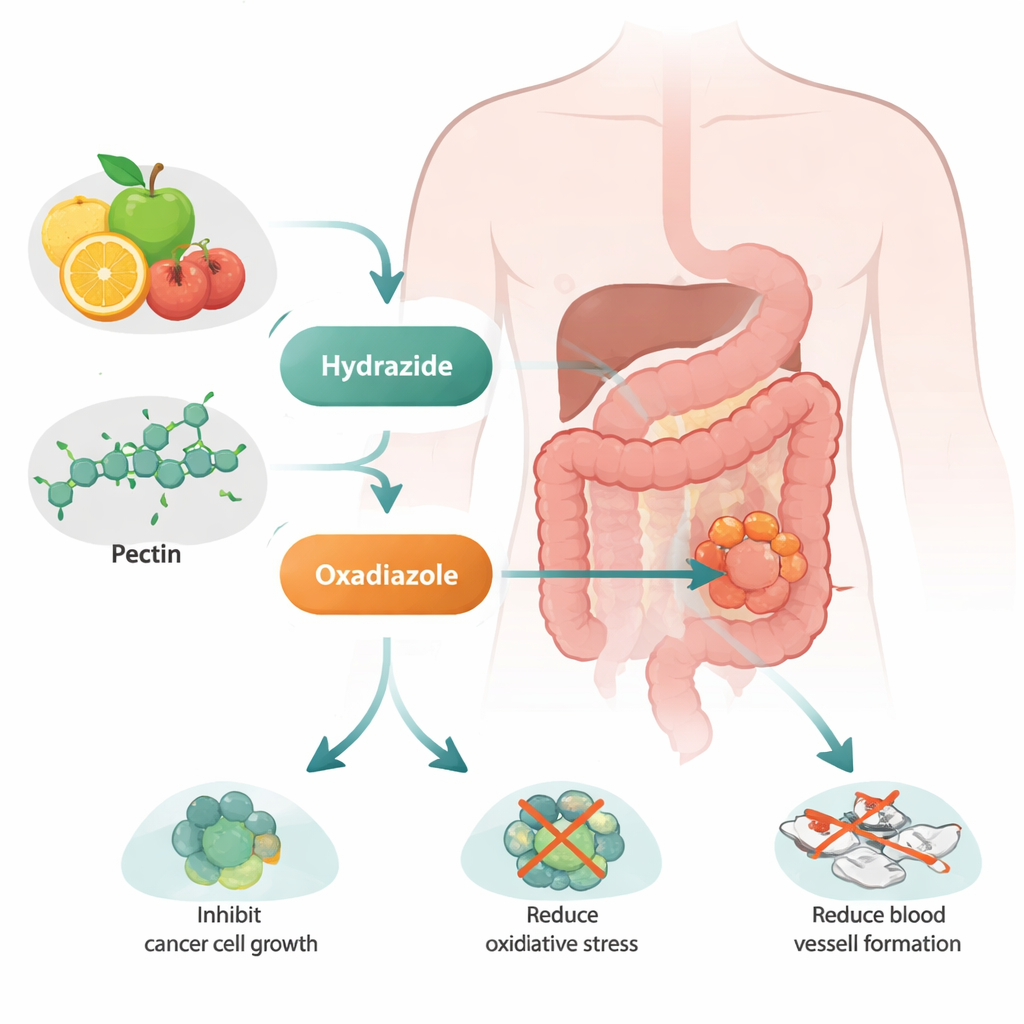
تحويل ألياف شائعة إلى مرشح دوائي ذكي
بدأ الباحثون ببكتين عادي، وهو سلسلة سكرية نباتية موجودة في العديد من الفواكه. باستخدام سلسلة من الخطوات الكيميائية المضبوطة، حوّلوا البكتين إلى شكلين جديدين أطلقوا عليهما «بكتين هيدرازيد» و«بكتين أوكساديازول». وعلى الرغم من أن الأسماء تقنية، فإن الفكرة بسيطة: عبر ربط مجموعات صغيرة تحتوي على النيتروجين والكبريت بالبكتين، أضافوا إلى الجزيء خواصًا إلكترونية وبنائية جديدة قد تجعله أكثر نشاطًا ضد الخلايا السرطانية. أكدت أدوات متقدمة مثل التحليل الطيفي بالأشعة تحت الحمراء والرنين المغناطيسي النووي والمجهر الإلكتروني واختبارات المقاومة للحرارة أن التفاعلات نجحت وأن المواد الجديدة كانت أكثر استقرارًا حراريًا من البكتين الأصلي.
اختبار المركبات الجديدة على خلايا السرطان
لفحص ما إذا كانت هذه الألياف المعدّلة قد تضر الخلايا السرطانية، عرّض الفريق سطرين خلويين بشريين—أحدهما من سرطان الكبد والآخر من سرطان القولون والمستقيم—لجرعات مختلفة من المركبات الجديدة. استخدموا اختبارًا يعتمد على صبغة يقيس عدد الخلايا التي تبقى حية بعد العلاج. أظهر كل من بكتين هيدرازيد وبكتين أوكساديازول فاعلية أكبر من البكتين غير المعدل في تقليل بقاء خلايا سرطان القولون والمستقيم (Caco2)، وكان لبكتين أوكساديازول التأثير الأقوى. أما ضد خلايا سرطان الكبد فكانت المركبات أقل قوة لكنها أظهرت نشاطًا ملحوظًا، مما يشير إلى أن الهيكليات الجديدة واعدة بشكل خاص لاستهداف أورام القولون والمستقيم.
خفض الإجهاد التأكسدي وقطع الإمداد الدموي للورم
لا يتطور السرطان بمعزل؛ بل يقوده الإجهاد الكيميائي والإشارات غير الطبيعية داخل الخلايا. ركز الباحثون على أنواع الأكسجين التفاعلية (ROS)—الجزيئات شديدة التفاعل التي يمكن أن تُتلف الحمض النووي وتدفع نمو الورم—وعلى البروتينات التي تساعد الأورام على التكيّف مع الإجهاد وبناء أوعية دموية جديدة. عندما عوملت خلايا Caco2 بالمشتقات الجديدة من البكتين عند جرعات فعالة، انخفضت مستويات ROS، كما تراجعت كمية إنزيم مضاد الأكسدة المسمى HO‑1. وعلى المستوى الجيني، انخفضت مفاتيح التحكم الرئيسية مثل NRF2 وHIF‑1α، إلى جانب العوامل المحفزة لتكوين الأوعية VEGF وPDGF‑D. بعبارة بسيطة، لم تضر البكتينات المعدّلة الخلايا السرطانية مباشرة فحسب، بل هدّأت أيضًا إشارات الإجهاد الداخلية وخفّضت التعليمات التي تحث الأورام على تكوين أوعية دموية جديدة.
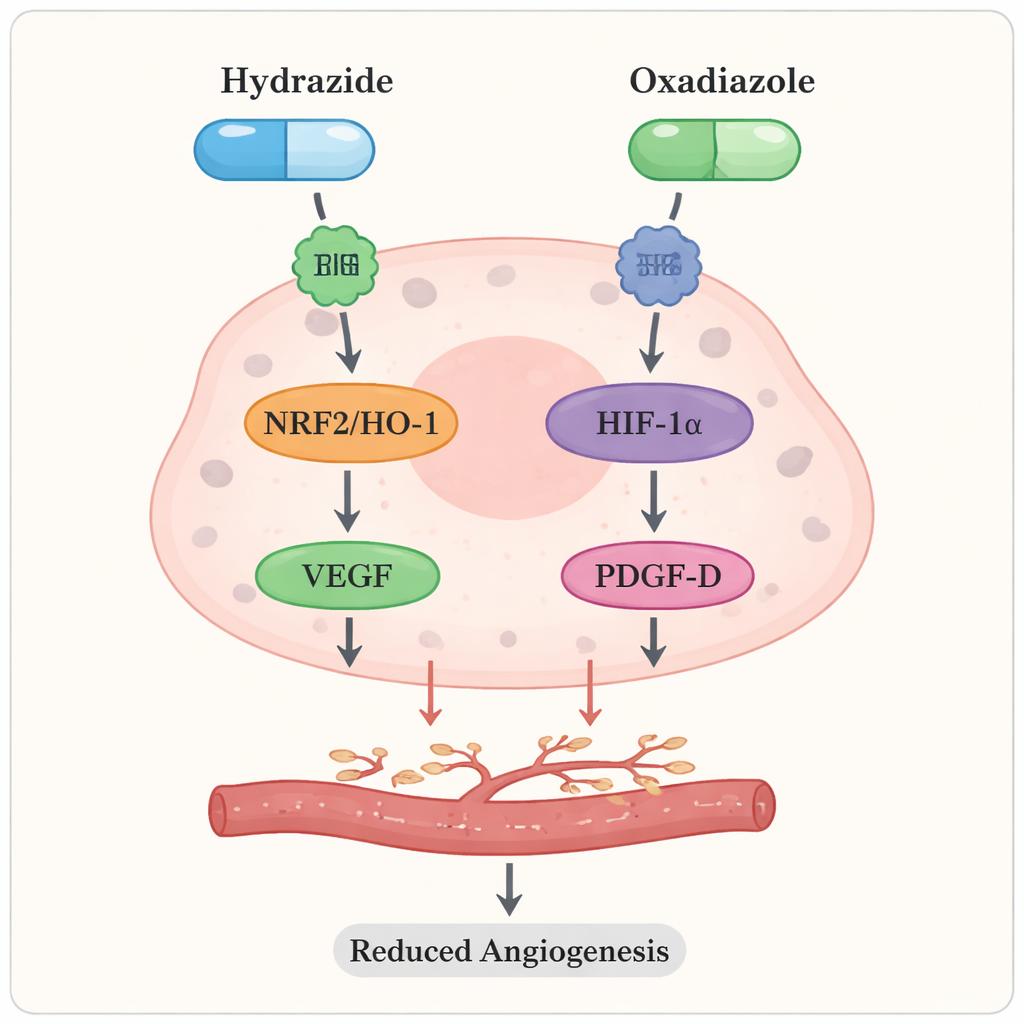
استخدام النماذج الحاسوبية لفهم سبب فعاليتها
للتعمق في أدلة كيفية وسبب نشاط هذه الجزيئات، لجأ الفريق إلى المحاكاة الحاسوبية. قاموا "بتثبيت" البكتين وبكتين هيدرازيد وبكتين أوكساديازول افتراضيًا داخل عدة هياكل بروتينية مرتبطة بنمو السرطان واستجابة الإجهاد وتكوين الأوعية الدموية. عبر جميع هذه الأهداف، بدا أن بكتين أوكساديازول يناسبها أفضل، مكوّنًا أقوى وأكثر التزامات ثباتًا. ودعمت محاكيات طويلة المدى التي تتعقب حركة الذرات على مدى 100 نانوثانية هذه الصورة: فقد تمسّك شكل الأوكساديازول بأهدافه وثبّت أشكالها أكثر من الهيدرازيد أو البكتين غير المعدل. وأظهرت حسابات كيمياء الكم أيضًا أن إضافة حلقات تحتوي على النيتروجين والكبريت غيّرت توزيع الإلكترونات في الجزيء، مما جعله أكثر تفاعلية بطرق تُفيد الارتباط القوي بالشركاء البيولوجيين.
ماذا قد يعني هذا لعلاجات السرطان المستقبلية
تُظهر الدراسة مجتمعة أن أليافًا غذائية مألوفة يمكن تحويلها إلى أكثر من مجرد مكوّن مفيد للأمعاء. عبر إعادة تصميم بنية البكتين بعناية، أنشأ الباحثون مركبات جديدة تهاجم خلايا سرطان القولون والمستقيم من عدة زوايا في آنٍ واحد: تبطئ نمو الخلايا، تقلل الإجهاد التأكسدي الضار، وتضعف الإشارات التي تحفز تكوّن أوعية دموية جديدة. وبينما تظل هذه النتائج قيد الاختبار في ثقافات خلوية ونماذج حاسوبية—ويجب اختبارها في خلايا طبيعية وحيوانات قبل أي استخدام بشري—فإنها تشير إلى بكتين هيدرازيد وخاصة بكتين أوكساديازول كنقاط انطلاق واعدة لتطوير أدوية آمنة ومتعددة الوظائف ضد سرطان القولون والمستقيم.
الاستشهاد: Elsayed, G.H., Fahim, A.M. Multifunctional pectin derivatives as anticancer agents in colorectal cancer via synthesis, computational insights, and modulation of NRF2/HO-1, HIF-1α, and VEGF/PDGF-D signaling pathways. Sci Rep 16, 6542 (2026). https://doi.org/10.1038/s41598-025-32107-6
الكلمات المفتاحية: بكتين, سرطان القولون والمستقيم, الإجهاد التأكسدي, تكوّن الأوعية الدموية, تصميم الأدوية