Clear Sky Science · ar
تصوير حي لديناميكيات الأدينوزين خارج الخلوي في القلب وتعديله الدوائي في نماذج فشل القلب لسمك الزرد
لماذا تهمنا قصة قلب هذا السمك
لا يزال فشل القلب واحداً من الأسباب الرئيسية للوفاة على مستوى العالم، ولا يزال كثير من المرضى يتدهورون رغم أفضل الأدوية المتاحة اليوم. يعرف العلماء أن خلايا القلب المت stressed تطلق إشارات كيميائية "استغاثة" إلى محيطها، لكن كان من الصعب مراقبة هذه الإشارات أثناء عمل القلب. تستخدم هذه الدراسة أسماك الزرد الشفافة، التي تحاكي قلوبها الصغيرة الخصائص الأساسية لقلوب البشر، لمراقبة تلك الإشارات الخطرة في الزمن الحقيقي واختبار طريقة جديدة لكتمها.
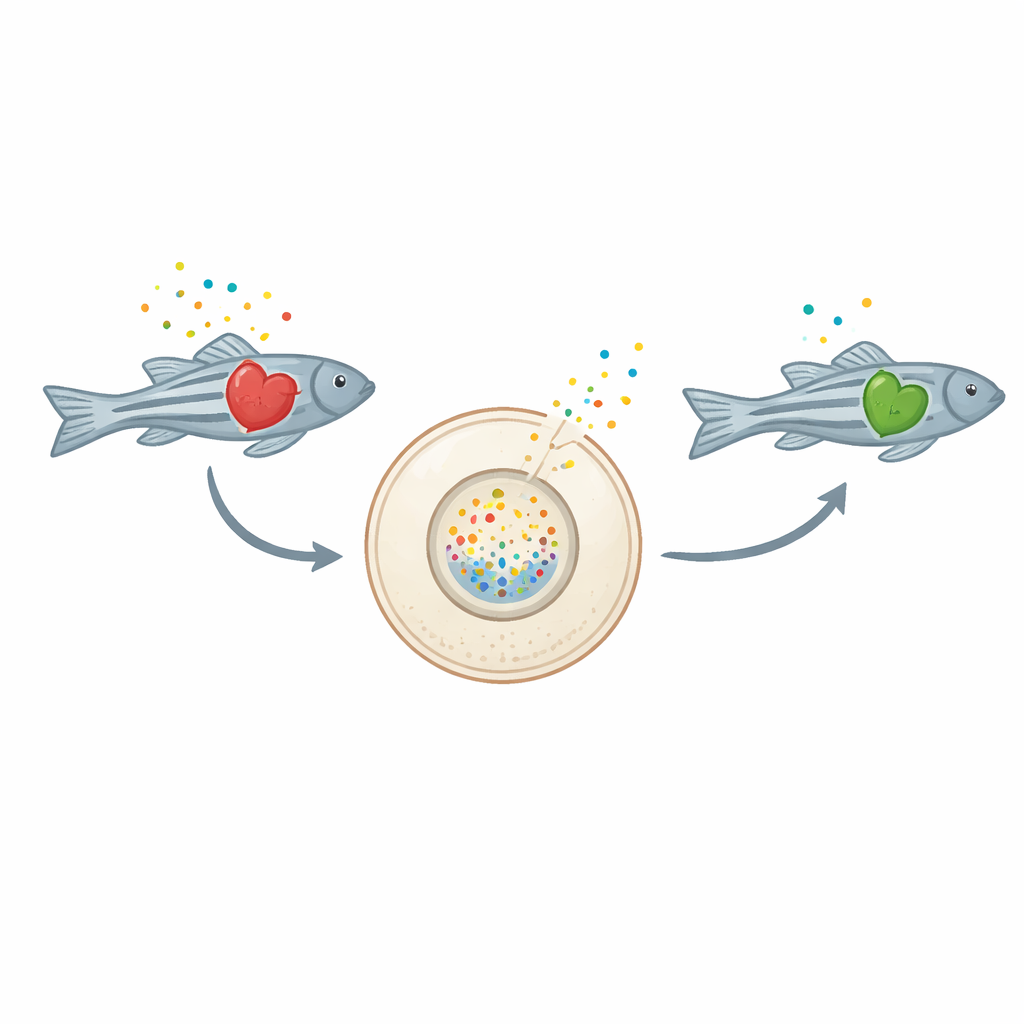
إشارات من قلب يكافح
عندما تتعرض خلايا القلب للضرر، تُطلق جزيئات حاملة للطاقة مثل ATP ومنتج تفككه الأدينوزين إلى الفراغ خارج الخلايا. خارج الخلية، تتوقف هذه الجزيئات عن العمل كوقود وتبدأ في أداء دور رسائل عاجلة يمكن أن تأجج الالتهاب. في فشل القلب المزمن، قد تصبح الاستجابة الالتهابية مفرطة النشاط مما يسبب مزيداً من الضرر للقلب. حتى الآن، لم يكن لدى الباحثين دليل مباشر داخل الجسم يوضح كيف تتصرف هذه الجزيئات مع مرور الوقت في قلب متدهور.
تحويل أسماك الزرد إلى كاميرات كيميائية حية
قام الفريق بتعديل أسماك الزرد بحيث تُنتج خلايا القلب فيها بروتين حساس فلوري خاص يُدعى GRABAdo على سطحها. عندما يتراكم الأدينوزين خارج الخلايا، يتوهج هذا المستشعر باللون الأخضر بشكل أكثر سطوعاً، محولاً كل قلب صغير إلى ما يشبه كاميرا كيميائية حية. ثم حفز الباحثون فشل القلب في أسماك الزرد باستخدام تيرفينادين، وهو دواء معروف بتعطيل إيقاع القلب وإضعاف قدرته على الضخ. مع تطور العلامات الواضحة لفشل القلب — تباطؤ نبض القلب، اتساع وبطء انقباض البطينات، وذمة حول القلب، وتراجع قدرة السباحة — أضاءت مجسات القلب، كاشفة عن ارتفاع ملحوظ في مستويات الأدينوزين خارج الخلايا. وأكدت القياسات الكيميائية لليرقات الكلية أن مستويات الأدينوزين الإجمالية كانت أعلى في القلوب المتدهورة.
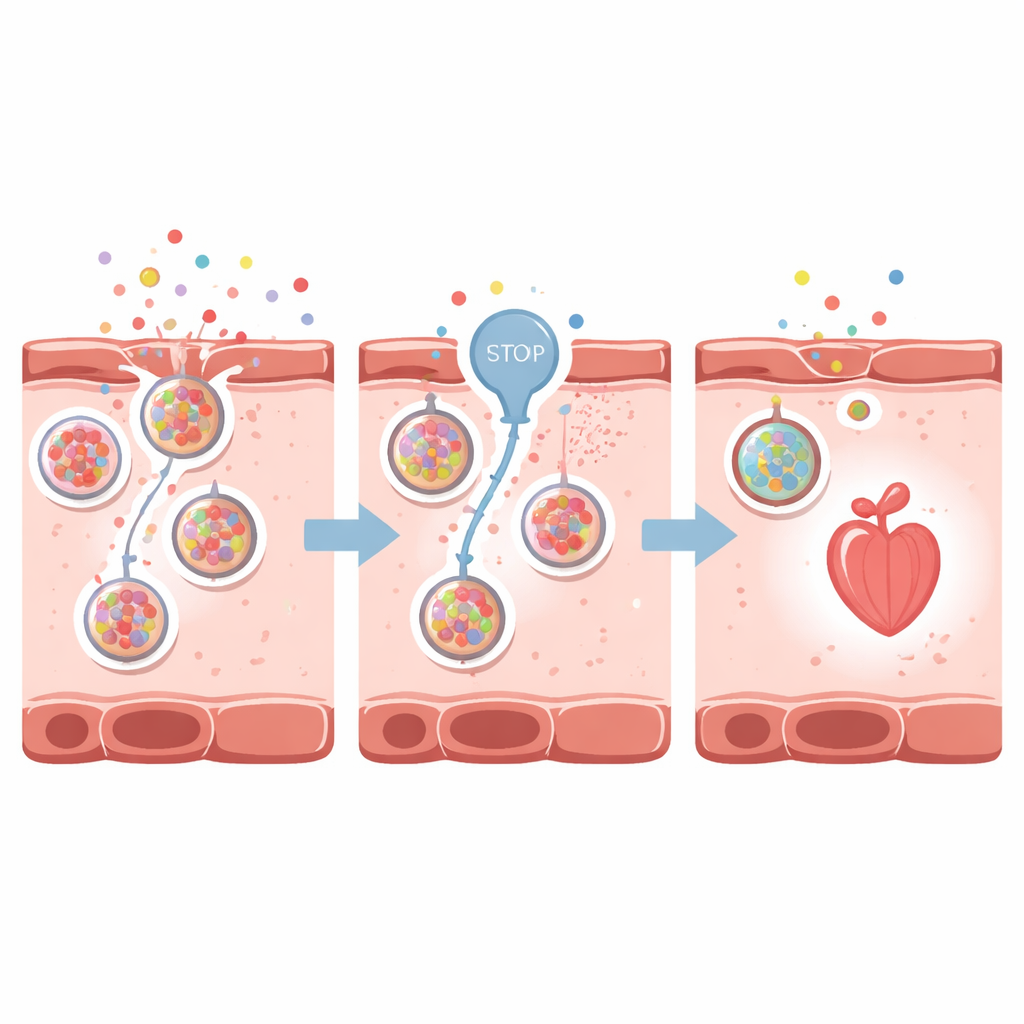
سدّ صمام الإفراز
سأل العلماء بعد ذلك ما إذا كان تخفيض هذه الإشارات التحذيرية يمكن أن يحمي القلب. ركزوا على VNUT، ناقل يحمّل ATP في حويصلات صغيرة داخل الخلية ليُفرَج به خارجها. باستخدام كلودرونات، دواء يثبط VNUT، قللوا من إفراز ATP وبطريقة غير مباشرة من تراكم الأدينوزين حول خلايا القلب. في أسماك الزرد التي أُحدث لها فشل القلب دوائياً، حافظت تثبيط VNUT على شكل القلب، وقلل من اتساع الحجرات، وحسّن معدل النبض وقوة الضخ، وحافظ على تدفق دم أفضل. خفت وهج مجس الأدينوزين، مما يبيّن أن إشارة الاستغاثة كانت أقل خارج الخلايا. ظهرت تأثيرات وقائية مماثلة في أسماك زرد بالغة تعاني من شكل حاد وسريع التطور من فشل القلب.
عدّة رافعات حماية تعمل معاً
يتضمن فشل القلب أكثر من مسار واحد، لذا اختبر الباحثون كيف يتفاعل حجب VNUT مع لاعبين معروفين آخرين. ساعدت الأدوية التي تحجب مستقبلات معينة للأدينوزين ومستقبلات ATP، وكذلك مركب يحد من تسريب ATP السلبي عبر قنوات الغشاء، قلوب أسماك الزرد كلٌ على حدة. عند الجمع مع تثبيط VNUT، أنتجت العديد من هذه العلاجات فوائد تراكمية، مما يوحي بأن خفض إشارات البورينات عند نقاط عدة يمكن أن يكون ذا قوة خاصة. ساعد تثبيط VNUT أيضاً في استعادة توازن الكالسيوم في خلايا القلب، وهو أمر أساسي للنبض الطبيعي، وقلل كل من موت الخلايا ونشاط الجينات المرتبطة بالالتهاب. ترسم هذه النتائج معاً صورة VNUT كمفتاح مركزي يربط بين إفراز ATP والالتهاب واضطراب توازن الكالسيوم والأذى التقدمي للقلب.
من حوض السمك إلى علاجات مستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن الدراسة تصور مباشرة إشارة كيميائية للتوتر ترتفع في القلوب المتدهورة وتُظهر أن حجب إطلاقها يمكن أن يحمي وظيفة القلب في حيوان حي. وعلى الرغم من أن قلوب أسماك الزرد أبسط من القلوب البشرية، إلا أنها تتقاسم بيولوجيا كافية لتكون منصة اختبار قوية لأفكار جديدة. من خلال كشف VNUT كهدف واعد عند تقاطع الالتهاب وعدم الاستقرار الكهربائي، تقترح هذه الدراسة أن علاجات فشل القلب المستقبلية قد تفعل أكثر من مجرد دعم تدفق الدم — قد تكبح أيضاً المحادثات الخلوية الضارة التي تدفع القلب نحو الفشل.
الاستشهاد: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
الكلمات المفتاحية: فشل القلب, إشارة الأدينوزين, نموذج سمك الزرد, الالتهاب, حماية القلب