Clear Sky Science · ar
آلية الكيرسيتين في علاج بطانة الرحم الهاجرة بناءً على دوائيات الشبكة وتسلسل النسخ
لماذا يهم مركب نباتي شائع لصحة المرأة
بطانة الرحم الهاجرة حالة مؤلمة تنمو فيها أنسجة شبيهة ببطانة الرحم في أماكن لا ينبغي أن توجد بها، مما يسبب غالبًا ألمًا مزمنًا وعقمًا. تتطلب العديد من النساء التوفيق بين عمليات جراحية متكررة وعلاجات هرمونية قد تسبّب آثارًا جانبية صعبة. تبحث هذه الدراسة في الكيرسيتين — مركب طبيعي موجود في العديد من الفواكه والخضروات — كخيار أكثر لطفًا وطويل الأمد. يطرح الباحثون سؤالًا بسيطًا بتبعات كبيرة: هل يمكن لهذا المركب النباتي اليومي أن يبطئ بشكل ملموس نمو وانتشار آفات بطانة الرحم الهاجرة؟
مشكلة واسعة الانتشار بحاجة إلى خيارات أفضل
تُقدّر نسبة الإصابة ببطانة الرحم الهاجرة بحوالي 10% من النساء في سن الإنجاب على مستوى العالم. يمكن أن تلتصق الأنسجة المتموضعة بشكل خاطئ بالأعضاء داخل الحوض، وتغزو المناطق المحيطة، وتنزف مرارًا مع كل دورة شهرية. تؤدي هذه التغيرات غالبًا إلى التهاب وتندب والتصاقات — شرائط نسيجية يمكن أن تلصق الأعضاء ببعضها — مما يسبب ألمًا وأحيانًا عقمًا. لا تزال الجراحة الوسيلة الأساسية لتأكيد التشخيص واستئصال الآفات، لكن المرض يعود في كثير من الأحيان. قد تساعد الأدوية الهرمونية، إلا أنها غالبًا ما تكبت المرض بدلًا من علاجه وقد تُحدث آثارًا جانبية يصعب على العديد من المرضى تحملها. وبما أن بطانة الرحم الهاجرة تميل إلى الاستمرار لفترات طويلة، فهناك حاجة ملحة لأدوية آمنة وميسورة التكلفة يمكن استخدامها على مدى سنوات.
نظرة أقرب على إمكانات الكيرسيتين العلاجية
الكيرسيتين صبغة صفراء توجد على نطاق واسع في البصل والتفاح والتوت والعديد من الأطعمة النباتية الأخرى. جذب الانتباه لآثاره المضادة للأكسدة والمضادة للالتهاب، ودُرِسَ لاحقًا لإمكانية فوائده ضد عدة أنواع من السرطان. تتصرف آفات بطانة الرحم الهاجرة في بعض النواحي مثل الخلايا الورمية: تلتصق، تغزو، تشكل أوعية دموية جديدة، وتنتشر محليًا. أظهرت أعمال سابقة أن الكيرسيتين يمكن أن يبطئ نمو خلايا بطانة الرحم الهاجرة ويحفز موتها في أطباق المختبر، لكن المسارات الدقيقة التي يستخدمها داخل الجسم لم تكن مفهومة بالكامل. هدفت الدراسة الحالية إلى رسم خريطة تلك المسارات بتفصيل، مزيجةً بين تحليلات حاسوبية واسعة النطاق وتجارب على عينات أنسجة بشرية، وفئران، وخلايا مزروعة في المختبر.
العثور على "مركز الحركة" الجزيئي
استخدم الفريق أولًا دوائيات الشبكة، وهي طريقة تقارن بين العديد من الأهداف الدوائية المحتملة والجينات المعروفة المرتبطة بالمرض. حددوا 132 هدفًا جزيئيًا يربط الكيرسيتين ببطانة الرحم الهاجرة ووجدوا أن عدة مسارات إشارية خلوية مهمة متورطة، مع بروز مسار واحد على وجه الخصوص: مسار MAPK، الذي يساعد في التحكم بكيفية نمو الخلايا وانقسامها وتحركها. داخل هذه الشبكة، ظهر بروتين سطحي يدعى PDGFRB كنقطة محورية رئيسية. عند فحص الأنسجة من نساء مصابات ببطانة الرحم الهاجرة، وجد الباحثون أن PDGFRB وعددًا من البروتينات الإشارية اللاحقة في سلسلة MAPK كانت أكثر وفرة بكثير في الآفات الشاذة (الموجودة في أماكن خاطئة) مقارنةً ببطانة الرحم الطبيعية، مما يشير إلى أن هذا المسار مفعل في المرض.
اختبار الكيرسيتين في الفئران والخلايا
لمعرفة ما إذا كان الكيرسيتين يستطيع فعلاً تهدئة هذا النظام المفرط النشاط، أنشأ العلماء نموذجًا للفأر لبطانة الرحم الهاجرة عن طريق زرع قطع صغيرة من نسيج الرحم داخل البطن. تلقت الفئران بعد ذلك جرعات منخفضة أو متوسطة أو عالية من الكيرسيتين عن طريق الفم، أو دواءً قياسيًا للمقارنة. على مدى ثلاثة أسابيع، قلّص الكيرسيتين الآفات المزروعة وخفّض درجة الالتصاقات الداخلية، مع تأثير أقوى للجرعات الأعلى. أظهر الفحص المجهري أن الآفات المعالجة احتوت على عدد أقل من الغدد وأكثر ضمورا ونسج داعمة أكثر ارتخاءً. بالتوازي، كشفت اختبارات البروتين أن الكيرسيتين خفّض مستويات PDGFRB والبروتينات الرئيسية ذات الصلة بمسار MAPK: RAS وRAF1 وERK1/2 في هذه الآفات.
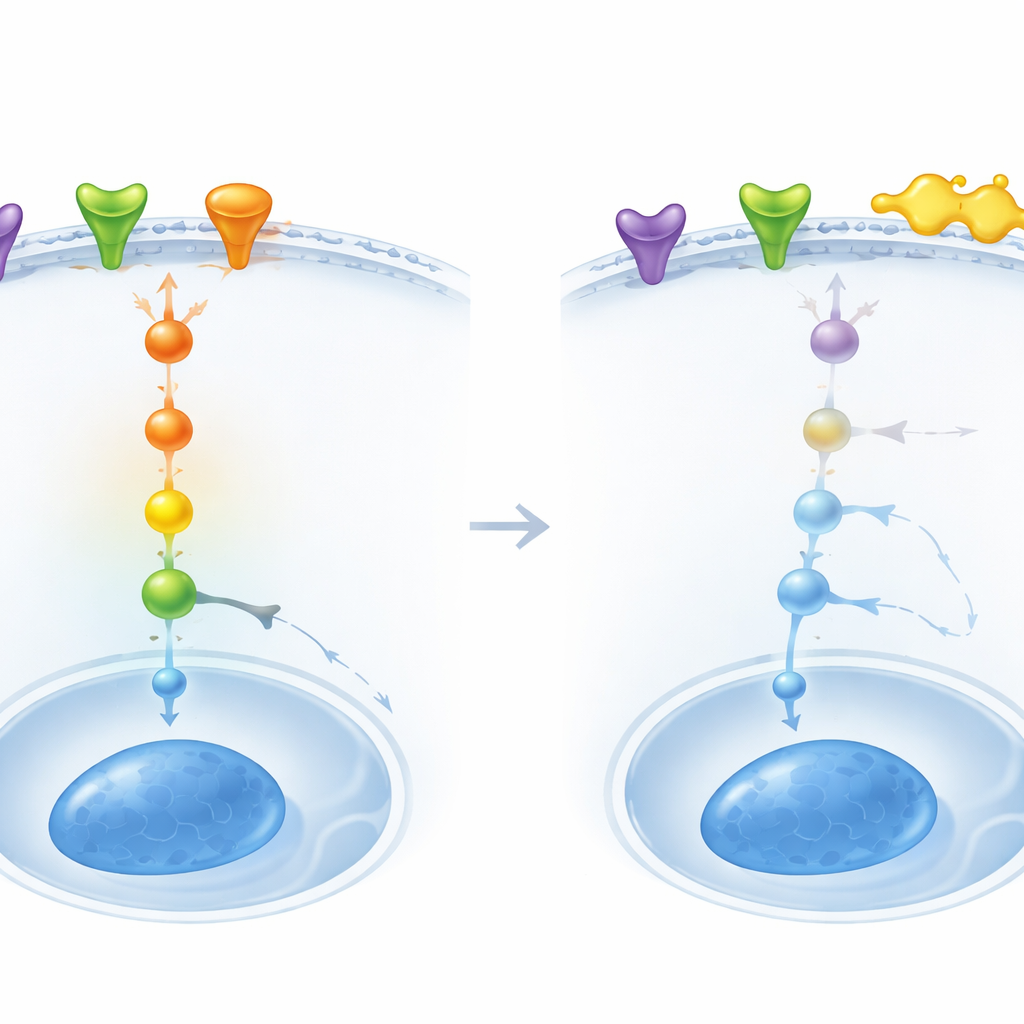
كيف يبطئ الكيرسيتين الخلايا المنحرفة
انتقل الباحثون بعد ذلك إلى زراعة الخلايا لاستكشاف الآلية بعمق أكبر. استخدموا خلايا 12Z المشتقة من آفات بطانة الرحم الهاجرة، وخفضوا عمدًا مستويات PDGFRB باستخدام أدوات جينية. عندما تم تثبيط PDGFRB، أظهرت الخلايا قدرة أقل على النمو، والغزو عبر الأغشية، والهجرة عبر الصحن — وهي ثلاث سلوكيات تدفع تكوّن وانتشار الآفات. أضافت معالجة بالكيرسيتين مزيدًا من الضعف لهذه الصفات. أظهرت دراسات البروتين المفصلة أن فقدان PDGFRB والعلاج بالكيرسيتين خففا من شدة سلسلة الإشارة MAPK داخل الخلايا، ملمّين بأشكال RAS وRAF1 وERK1/2 النشطة التي عادة ما تنقل إشارات قوية "للنمو والحركة".
ماذا يعني هذا للعلاج المستقبلي
مجملاً، تشير النتائج إلى قصة واضحة: في بطانة الرحم الهاجرة، يُعزَّز نشاط PDGFRB وسلسلة الإشارة المرتبطة به، مما يشجع الخلايا على التكاثر والغزو. يبدو أن الكيرسيتين يخفض من هذا النشاط، مصغّرا الآفات في الفئران ومروّضًا السلوك الخلوي العدواني في المختبر عن طريق ضبط مسار PDGFRB–MAPK. وبينما لا تزال هذه الأعمال في مرحلة تجريبية ولا تثبت بعد أن الكيرسيتين وحده يمكنه علاج بطانة الرحم الهاجرة لدى البشر، فإنها توفر أساسًا بيولوجيًا قويًا لدراسات سريرية مستقبلية. وللمرضى، تثير هذه النتائج احتمال أن يصبح مركب طبيعي موجودًا بالفعل في العديد من الأطعمة جزءًا يومًا ما من استراتيجية أكثر أمانًا وطويلة الأمد لإدارة هذا المرض المزمن والمُربك للحياة.
الاستشهاد: Huang, J., Ding, J., Wang, J. et al. Mechanism of quercetin in the treatment of endometriosis based on network pharmacology and transcriptome sequencing. Sci Rep 16, 8503 (2026). https://doi.org/10.1038/s41598-025-07693-0
الكلمات المفتاحية: بطانة الرحم الهاجرة, الكيرسيتين, صحة المرأة, إشارة خلوية, مركبات طبيعية