Clear Sky Science · ar
تحديد وتقييم المستضدات المرتبطة بالبيروبتوزوم للورم لتصميم مرشح لقاح ضد سرطان الرئة
لماذا يهم هذا البحث لمرضى سرطان الرئة
لا يزال سرطان الرئة أكثر أنواع السرطان فتكًا على مستوى العالم، والعلاجات الحالية — الجراحة، والعلاج الكيميائي، والإشعاعي، والمناعي — لا تزال تترك العديد من المرضى دون خيارات طويلة الأمد. تستكشف هذه الدراسة فكرة مختلفة تمامًا: لقاح علاجي مصمم ليس لمنع العدوى، بل لتدريب الجهاز المناعي على التعرف بشكل أفضل على أورام الرئة ومهاجمتها. باستخدام نمذجة حاسوبية متقدمة، يبني المؤلفون ويختبرون بالكامل في الحاسوب لقاحًا بروتينيًا يستهدف جزيئات مرتبطة بنوع من موت الخلية الالتهابي المسمى البيروبتوزوم، فاتحًا طريقًا جديدًا لعلاج سرطان الرئة بدقة واستدامة أكبر.
تحويل مفتاح موت الخلية إلى هدف سرطاني
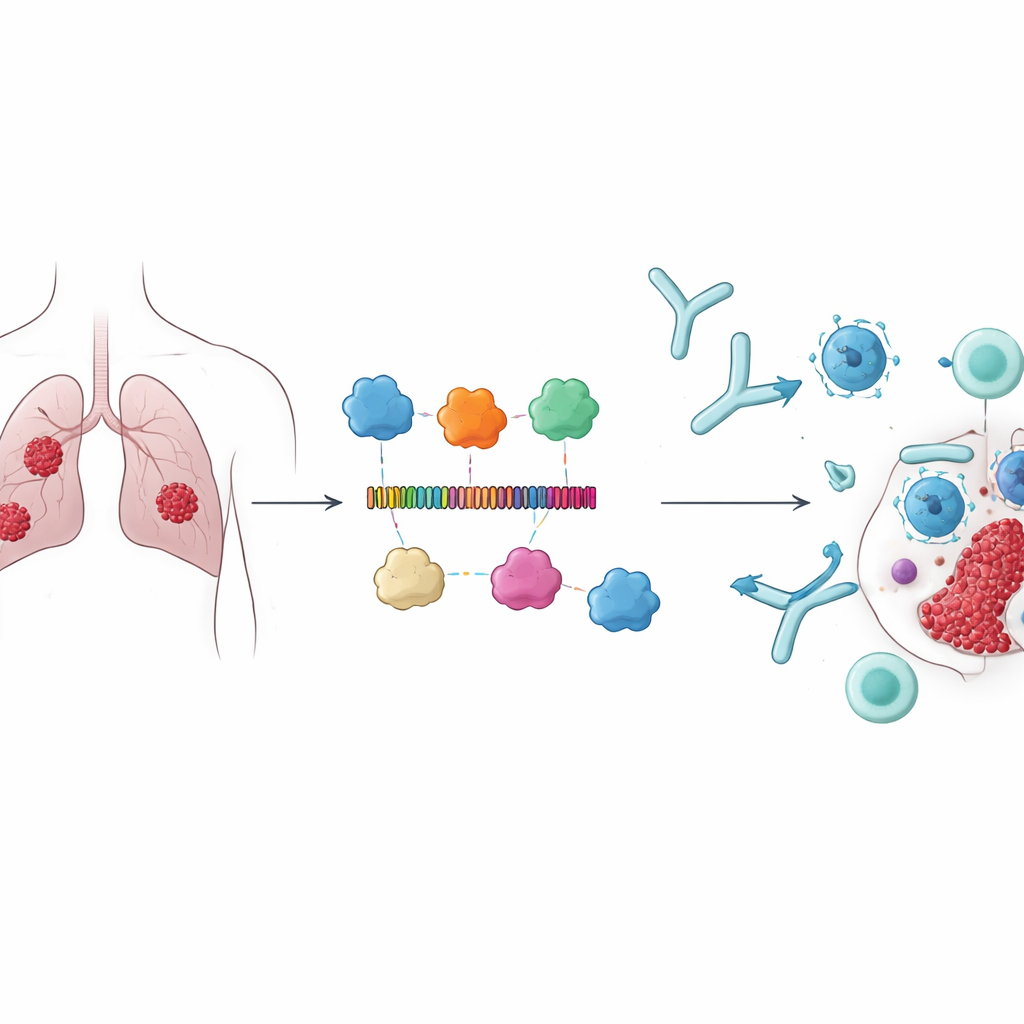
بدلاً من التركيز على العلامات السرطانية التقليدية، اختار الباحثون أربعة بروتينات — CARD8 وNAIP وNLRP1 وNLRP3 — المشاركة في البيروبتوزوم، وهو نوع متفجر من الموت الخلوي المبرمج الذي يمكن أن ينبه الجهاز المناعي. هذه البروتينات نشطة في تنظيم المناعة وقد ارتبطت ببقاء أفضل في سرطان الغدة القيقي للرئة، مما يجعلها أهدافًا جذابة. افترض الفريق أنه إذا أمكن تدريب الجهاز المناعي بدقة للتعرف على مقاطع صغيرة من هذه البروتينات على خلايا الورم، فقد لا يساعد ذلك فقط في تدمير الخلايا السرطانية مباشرةً بل ويعزز أيضًا استجابات مناعية أوسع ضد الورم.
بناء لقاح مخصص قطعة قطعة
باستخدام أدوات المعلوماتية المناعية، مسح المؤلفون البروتينات الأربعة لتحديد مقاطع قصيرة، أو مواقع إبوتوبية، متوقعة أن تتعرف عليها كل من خلايا T وB. من بين مئات المرشحين اختاروا 15 إبوتوبًا حاز على درجات عالية لكونه قابلاً للتعرّف من قبل الخلايا المناعية، مع توقعات بكونه غير سام وغير مسبب للحساسية. ثم ربطت هذه القطع معًا في بروتين طويل واحد، مفصولة "بفواصل" جزيئية مختارة بعناية بحيث تظل كل إبوتوب متاحة. ولتعزيز الاستجابة المناعية أضافوا ثلاثة مكونات معروفة لتحفيز المناعة من بروتينات بكتيرية كمساعدات مناعية. البنية الناتجة، بطول 678 وحدة بناء (أحماض أمينية)، توقعت أن تكون مستقرة، قابلة للذوبان، وعالية المستضدية — وهي خصائص مهمة للقاح قابل للتطبيق العملي.
اختبار الشكل والقوة عبر الحاسوب
نظرًا لأن فعالية اللقاح تعتمد كثيرًا على شكله ثلاثي الأبعاد، قام الفريق ببناء نماذج ثلاثية الأبعاد للبروتين الجديد باستخدام عدة برامج متقدمة لتنبؤ البنى. قاموا بتنقيح هذه النماذج بشكل متكرر وفحصوا جودتها بمقاييس معيارية للبنية، واستقروا على نسخة نهائية استوفت معايير صارمة لهندسة البروتين الواقعية والاستقرار. كما رسموا المناطق السطحية التي ستكون الأكثر سهولة لالتصاق الأجسام المضادة وصمموا "جسور" داخلية جديدة تُدعى روابط ثنائية الكبريت متوقعة أن تزيد من صلابة البروتين واستقراره. لمحاكاة سلوك اللقاح في بيئة مائية مشابهة للجسم، أجروا محاكاة ديناميكا جزيئية مفصلة دامت 100 مليار جزء من الثانية عبر عشر عدة تجارب مستقلة. طوال هذه المحاكاة، ظل البروتين النموذجي مدمجًا وثابتًا من الناحية التركيبية، مما يوحي بأنه سيحافظ على شكله المقصود في ظروف حقيقية.
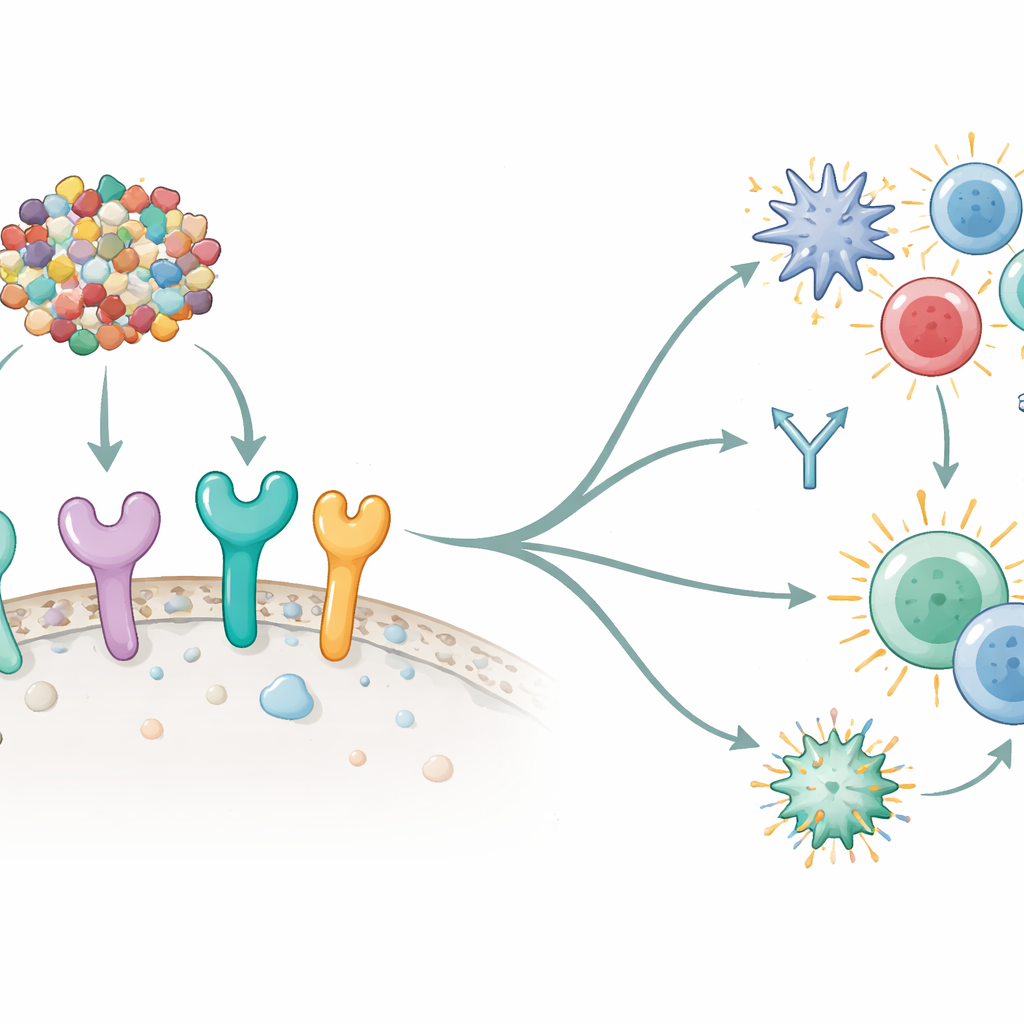
محاكاة استجابة الجهاز المناعي
سأل الباحثون بعد ذلك ما إذا كان لقاحهم، من الناحية النظرية، يمكن أن يتواصل مع أجهزة الإنذار الرئيسية في الجهاز المناعي — مستقبلات شبيهة بالتول (TLRs) الموجودة على أو داخل الخلايا المناعية. أظهرت تجارب التراصف الحاسوبية تفاعلات قوية ومستقرة بين اللقاح وستة أنواع مختلفة من مستقبلات TLR البشرية، لا سيما TLR5 وTLR8 المعروفين بإثارة تسلسلات مناعية قوية. ثم حاكى الفريق جدول تطعيم كامل باستخدام برنامج نمذجة الجهاز المناعي. في هذه التجارب الافتراضية أدت ثلاث جرعات من اللقاح إلى إزاحة سريعة للمستضد المحاكى، وموجات قوية من الأجسام المضادة (وخاصة IgM وIgG1)، وارتفاع في خلايا B الذاكرية طويلة العمر وخلايا T المساعدة. كما ارتفعت جزيئات الإشارة المهمة مثل إنترفيرون غاما والإنترلوكينات، مشيرة إلى تنشيط كل من الذراع الفطرية والتكيفية للمناعة — وهو نوع الاستجابة المتوازنة المطلوبة للحماية المضادة للأورام.
التحضير للإنتاج في العالم الحقيقي
للانتقال من الفكرة إلى الاختبار المخبري، تحقق الفريق مما إذا كان بالإمكان إنتاج اللقاح بكفاءة في عامل بكتيري شائع وهو الإشريكية القولونية. عبر تعديل الشفرة الجينية للقاح دون تغيير البروتين نفسه، حققوا نمطًا مثاليًا لإنتاج البروتين البكتيري وتركيبًا كيميائيًا متوازنًا للحمض النووي. ثم نفذوا خطوة استنساخ افتراضية، مدخلين الجين المحسّن في بلازميد مخبري قياسي يستخدم للتعبير البروتيني. تشير هذه الخطوات إلى أنه، إذا نُقل إلى المختبر، فربما يمكن تصنيع اللقاح على نطاق واسع للدراسات التجريبية.
ماذا قد يعني هذا لرعاية السرطان في المستقبل
بعبارات بسيطة، تقدم هذه العمل مخططًا مُجرَّبًا بالحاسوب لقاحًا لسرطان الرئة يستهدف بروتينات مرتبطة بشكل خاص بنوع التهابي من موت الخلايا الورمية. يبدو التصميم آمنًا ومستقرًا وقادرًا على تحفيز الدفاعات المناعية بشدة في المحاكاة، مع تغطية متوقعة واسعة عبر مجموعات سكانية بشرية. وعلى الرغم من أنه لا يزال نموذجًا رقميًا ويحتاج إلى التحقق منه في الخلايا والحيوانات وفي النهاية لدى البشر، فإن الدراسة توضح كيف يمكن للأدوات الحاسوبية الحديثة أن تضغط سنوات من التجارب والخطأ إلى تصميم متكامل واحد. إذا أكدت التجارب المستقبلية هذه التنبؤات، فقد يكمل مثل هذا اللقاح يومًا ما العلاجات الموجودة، مساعدًا أجهزة المرضى المناعية على التعرف على أورام الرئة ومهاجمتها بشكل أكثر موثوقية.
الاستشهاد: Nguyen, T.L., Kim, H. Identification and evaluation of tumor pyroptosis-associated antigens for design a vaccine candidate against lung cancer. Sci Rep 16, 9559 (2026). https://doi.org/10.1038/s41598-024-84792-4
الكلمات المفتاحية: لقاح سرطان الرئة, البيروبتوزوم, العلاج المناعي متعدد الوبائث, تصميم لقاح بواسطة الحوسبة, الاستجابة المناعية للورم