Clear Sky Science · ar
مجموعة بيانات نصية خلوية مفردة تصوّر الإصابات الدماغية الرضّية والعلاج الجيني المعتمد على NeuroD1 في الفئران
لماذا تهمنا إصابات الدماغ جميعًا
كل عام، يتعرض الملايين لضربات على الرأس نتيجة سقوط أو حوادث أو رياضات أو قتالات. يمكن لهذه الإصابات الدماغية الرضّية أن تترك مشكلات طويلة الأمد في الذاكرة والحركة والمزاج، والعلاجات المتوفرة اليوم تدير الأعراض في الغالب بدلاً من إصلاح الدماغ جوهريًا. تستكشف هذه الدراسة نهجًا واعدًا قائمًا على الجينات في الفئران يهدف ليس فقط إلى الحد من الضرر، بل إلى مساعدة الدماغ على إعادة بناء نفسه من الداخل، وتقوم بتصوير هذه التغيرات خلية بخلية لتشكيل مورد عام للعلاجات المستقبلية.
نظرة داخل الدماغ المصاب
عندما يصاب الدماغ، فإنه لا يتعرض لكدمة بسيطة كما العضلة. تتوالى سلسلة تفاعلات معقدة: تموت الخلايا العصبية، يتعكر تدفّق الدم، وتتدخل خلايا داعمة تُسمى الخلايا النجمية والخلايا المناعية. عادةً ما تساعد الخلايا النجمية على تغذية الخلايا العصبية والحفاظ على توازن الإشارات الدماغية، لكن بعد الصدمة يمكن أن تشكل ندبة كثيفة وتغذي التهابًا طويل الأمد. استخدم المؤلفون جرحًا محكمًا في قشرة المخ للفئران لمحاكاة أشكال معينة من الإصابات المخترقة، ثم فحصوا كيف استجابت كل فئة خلوية رئيسية في النسيج المتأثر عبر الزمن. طبقوا تقنية تُسمى تسلسل الحمض النووي الريبي خلية مفردة، التي تقرأ أي الجينات مفعّلة في عشرات الآلاف من الخلايا الفردية، مما يسمح بتعداد مفصّل لكيفية تغير المجتمع الخلوي للدماغ بعد الإصابة.
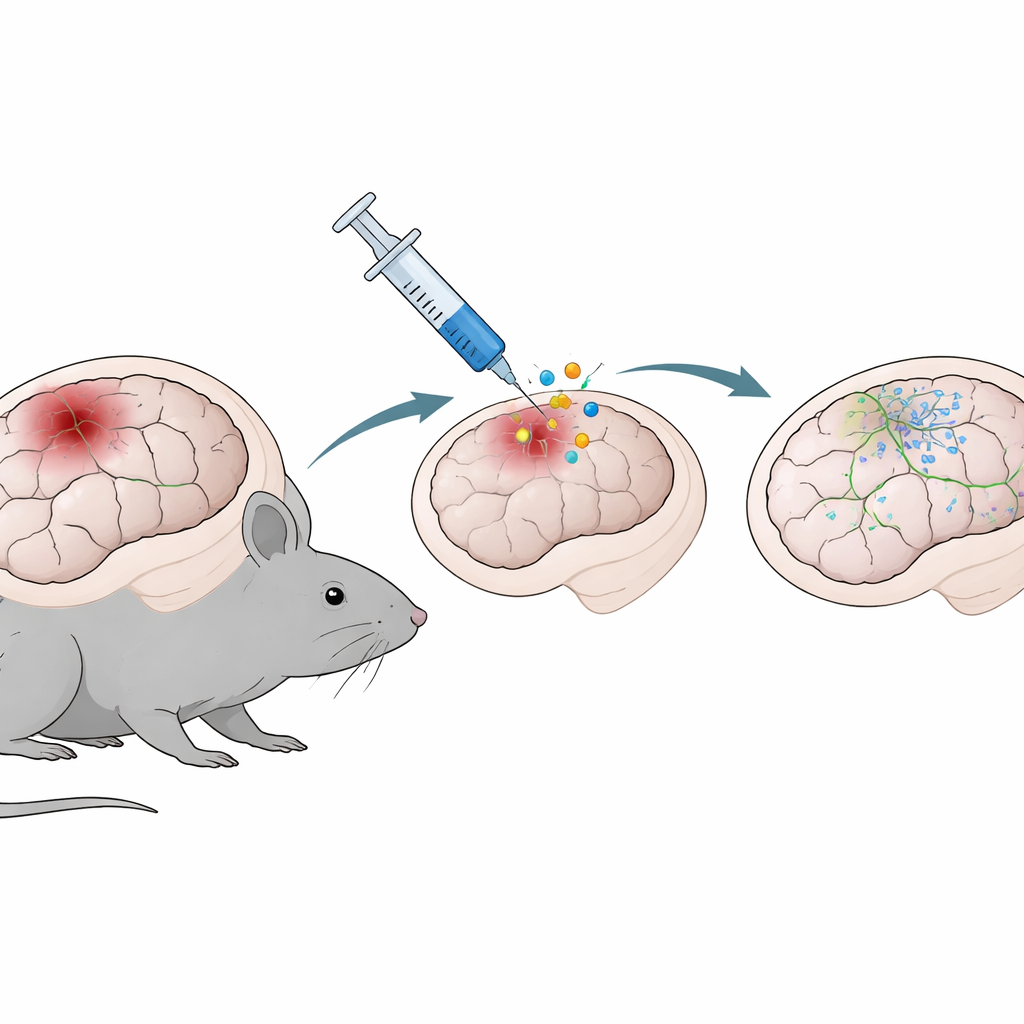
علاج جيني يستقطب خلايا الدعم الدماغية
بما أن الخلايا النجمية وفيرة ومتواجدة مباشرة في موقع الإصابة، فهي أهداف جذابة لاستراتيجيات الإصلاح. اختبر الفريق علاجًا جينيًا قائمًا على NeuroD1، وهو جين معروف بدفع الخلايا نحو حالة شبيهة بالخلايا العصبية. باستخدام ناقل فيروسي غير ضار تم حقنه في المنطقة القشرية المتضررة بعد ثلاثة أيام من الإصابة، سلّموا إما علامة محايدة (GFP) أو NeuroD1 إلى الخلايا النجمية. عندما فُحصت الأدمغة بعد أسبوع وأسبوعين، أظهرت الفئران المتلقية لـ NeuroD1 تجاويف نسيجية أصغر حيث حدث الضرر وعددًا أقل من الخلايا المناعية المنشَّطة المسماة بالميكروغليا حول الآفة. بعبارة أخرى، لم يقتصر تأثير العلاج على تقليل الضرر البنيوي المرئي فحسب، بل هدأ أيضًا الاستجابة الالتهابية المحلية.
تتبُّع أنواع الخلايا خليةً خليةً
لفهم ما يكمن وراء هذه التحسُّنات، قارن الباحثون ثلاث مجموعات من عينات القشرة: فئران سليمة، وفئران مصابة أعطيت الفيروس الضابط، وفئران مصابة أعطيت فيروس NeuroD1. قاموا بتسلسل أكثر من 97,000 خلية فردية إجمالًا وجمّعوها حسب أنماط نشاطها الجيني إلى سكان دماغيين مألوفين، بما في ذلك الخلايا العصبية، والخلايا النجمية، وخلايا النخاع الملينية (الأوليجوديندروسايت) التي تعزل الألياف العصبية، والميكروغليا، والخلايا المبطنة للأوعية الدموية وتجويفات المخ. أدت الإصابة وحدها إلى تحوّل هذا التوازن نحو المزيد من الخلايا النجمية والميكروغليا وأقل من الخلايا العصبية والخلايا المكوِّنة للمايلين، ما يعكس التندب والالتهاب. مع علاج NeuroD1، بدأ هذا الانحراف في الانعكاس: تزايدت نسب الخلايا العصبية والأوليجوديندروسايت والخلايا الطلائية للجسم السنخي، بينما أصبحت الخلايا النجمية والميكروغليا أقل هيمنة في المنطقة المصابة.
العمل الخفي لأنواع فرعية من الخلايا النجمية
لم تكن الخلايا النجمية مجموعة موحدة واحدة. عبر إعادة تحليلها بشكل منفصل، عرّف الفريق سبع مجموعات فرعية متميزة من الخلايا النجمية، لكل منها توقيع جيني وسلوك مختلف عبر الحالات الثلاث. ظهرت بعض المجموعات الفرعية شائعة في النسيج السليم لكنها تكاد تختفي بعد الإصابة، في حين ظهرت أخرى فقط بعد الصدمة. في الأدمغة المصابة والمعالجة بالفيروس الضابط، فعّلت عدة مجموعات نجمية برامج متعلقة ببناء وإعادة تشكيل المشابك — النقاط التي تتواصل عندها الخلايا العصبية — بينما خفّضت تعبير جينات مرتبطة بإنتاج الطاقة في الميتوكوندريا. يشير هذا النمط إلى أنه بعد الإصابة، كانت الخلايا النجمية تدفع اتجاهات توصيل عصبي غير طبيعية مع عمل أيضي منخفض.
كيف يعيد NeuroD1 توازن طاقة الخلايا والاتصال العصبي
أعاد علاج NeuroD1 تشكيل هذه المجموعات الفرعية من الخلايا النجمية في اتجاه مختلف. في عدة مجموعات نجمية مرتبطة بالإصابة، عُززت الجينات المتعلقة بنشاط الميتوكوندريا والتنفس الخلوي والأيض العام للطاقة مرة أخرى، بينما خفّفت الجينات المرتبطة بالبناء المفرط للمشابك وإعادة تشكيل المايلين. بعبارة أخرى، بدا أن NeuroD1 يعيد محركات الطاقة في هذه الخلايا ويهدئ محاولات إعادة التوصيل المفرطة التي قد تسهم في الخلل. تقلّصت بعض الأنواع الفرعية من الخلايا النجمية التي توسعت بشدة بعد الإصابة في وجود NeuroD1، في حين ازداد أخرى المرتبطة بوظائف أكثر صحة. توفر هذه التحولات الدقيقة دلائل حول أي حالات الخلايا النجمية ضارة وأيها قد تدعم الإصلاح.
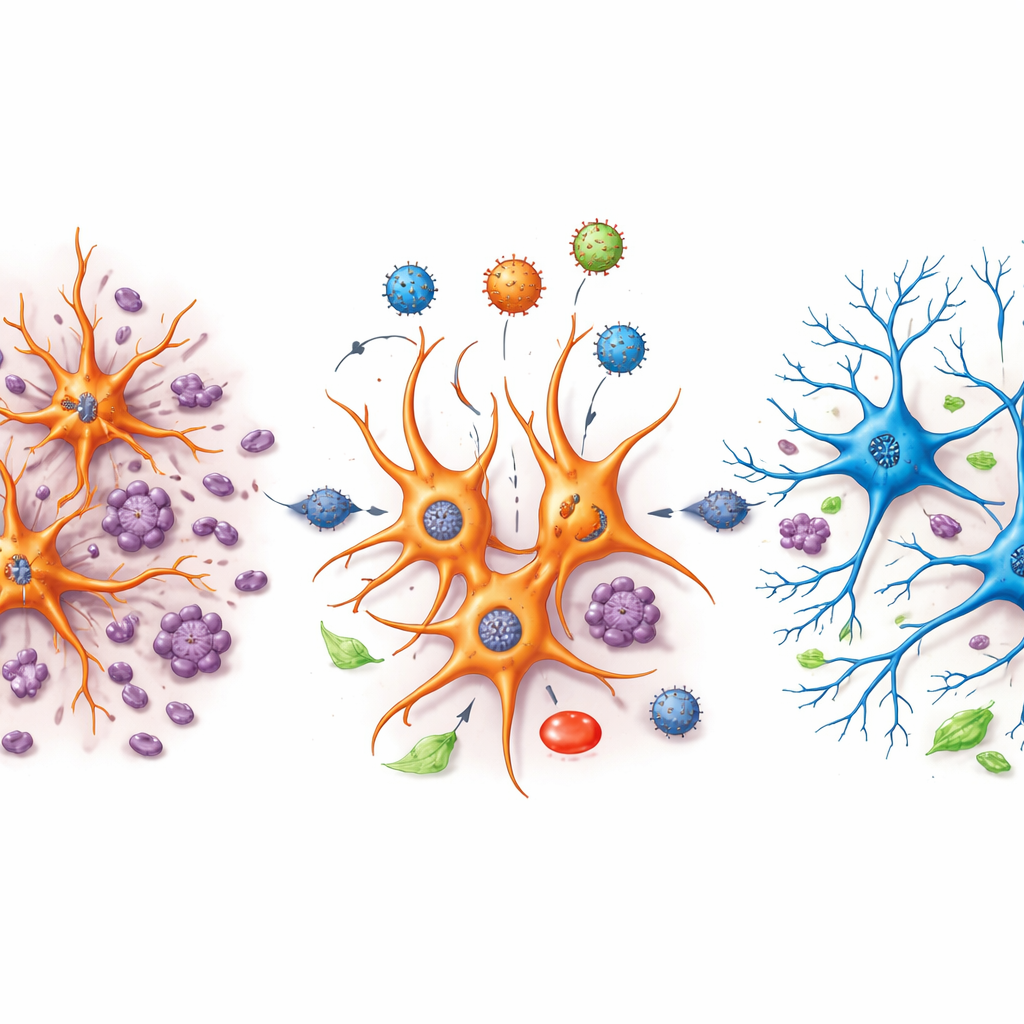
ما الذي يعنيه هذا لإصلاح الدماغ مستقبلاً
هذا العمل لا يقدم بعد علاجًا جاهزًا للإصابات الدماغية البشرية، لكنه يقدم تقدمين مهمين. أولاً، يوضح في دماغ ثديي حي أن علاجًا جينيًا موجَّهًا يمكن أن يقلل فقدان النسيج والالتهاب بينما يدفع مجموعات الخلايا واستخدام الطاقة نحو حالة أكثر صحة. ثانيًا، يوفر مجموعة بيانات خلوية مفردة غنية ومفتوحة يمكن للعلماء الآخرين التنقيب فيها لتحديد أنواع خلايا وجينات ومسارات محددة تدفع الضرر أو التعافي بعد الصدمة. للقراء خارج المختبر، الرسالة الأساسية هي أن خلايا الدعم الخاصة بالدماغ يمكن استقطابها وإعادة برمجتها لمساعدة إعادة بناء الدوائر المصابة، مما يقربنا خطوة نحو علاجات تستعيد الوظيفة الدماغية بدلاً من مجرد تثبيتها بعد ضربة رضّية.
الاستشهاد: Chen, R., Zhang, S., Liu, S. et al. A single-cell transcriptomic dataset profiling traumatic brain injury and NeuroD1-based gene therapy in mice. Sci Data 13, 406 (2026). https://doi.org/10.1038/s41597-026-06788-1
الكلمات المفتاحية: الإصابة الدماغية الرضّية, العلاج الجيني, الخلايا النجمية, تسلسل خلية مفردة, NeuroD1