Clear Sky Science · ar
مجموعة بيانات الأشعة المقطعية مع قياسات RECIST وأقنعة تقسيم شاملة للأورام والعقد اللمفاوية
لماذا هذه المورد لتصوير السرطان مهم
تعتمد رعاية السرطان بشكل متزايد على الصور الطبية لتقرير ما إذا كانت العلاجات فعالة. ومع ذلك، فإن القياسات الدقيقة فتحة بفتحة التي يجريها الأطباء على صور الأشعة المقطعية تستغرق وقتًا طويلاً وقد تختلف من خبير لآخر. يقدم هذا المقال مجموعة جديدة متاحة علنًا من صور الأشعة المقطعية لمرضى السرطان، حيث تم تحديد محيط الأورام والعقد اللمفاوية وقياسها بعناية وفقًا لدليل إكلينيكي مستخدم على نطاق واسع. صممت هذه المجموعة لمساعدة الباحثين في بناء واختبار برامج حاسوبية قد تتولى يومًا جزءًا كبيرًا من هذا العمل الممل وتجعل متابعة علاج السرطان أسرع وأكثر اتساقًا على مستوى العالم.
كيف يتتبع الأطباء الأورام حاليًا
لتقييم ما إذا كان علاج السرطان مفيدًا، يتبع أطباء الأشعة غالبًا معيارًا يسمى RECIST 1.1. عمليًا، يعني هذا اختيار عدد قليل من الأورام «المستهدفة» في صور المريض بالأشعة المقطعية وتسجيل أطول قطر مرئي لكل منها بالمليمترات. مع مرور الوقت، يقارنون مجموع هذه الأقطار مع الصور السابقة ليقرروا ما إذا كان المرض قد تقلص أو ظل مستقرًا أو نما. رغم أن هذا النهج جلب نوعًا من النظام للتجارب السريرية، إلا أنه له عيوب: فهو يعتمد بشكل كبير على الأورام التي يختارها الطبيب، ويستند إلى قياسات أحادية البعد بدلًا من الحجم ثلاثي الأبعاد الحقيقي، وعادة ما يستغرق أكثر من 10 دقائق لكل مريض في كل تقييم. مع تزايد حالات السرطان عالميًا، تضع هذه الحدود ضغوطًا حقيقية على خدمات الأشعة.
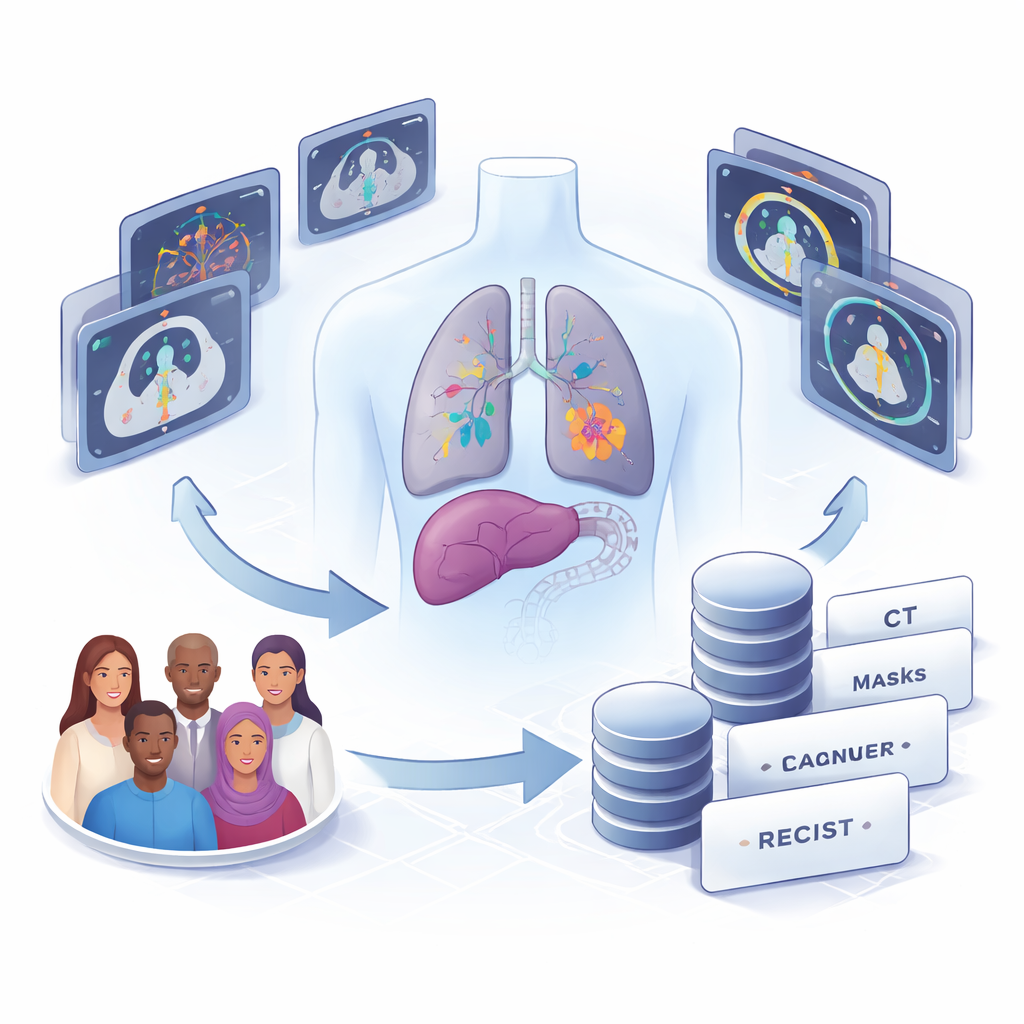
ماذا تحتوي مجموعة بيانات الأشعة المقطعية الجديدة
جمع المؤلفون صور الأشعة المقطعية من 22 بالغًا عولجوا لأنواع متنوعة من السرطانات في المستشفى السريري لجامعة تشيلي، بما في ذلك سرطانات الرئة والكبد والقولون والمستقيم والثدي والمبيض والمعدة والمرارة والمثانة والميلانوما. من 58 سلسلة تصوير صدري وبطني أُجريت بين 2017 و2023، حددوا كل ورم صلب أو عقدة لمفاوية متضخمة قابلة للقياس. في المجموع، رسموا يدويًا 1,246 آفة فردية: 1,148 نقيلة (أورام انتشرت)، 93 عقدة لمفاوية متضخمة، و5 أورام أولية. بالنسبة إلى 82 من هذه الآفات، أدرجوا أيضًا قياسات RECIST الرسمية المسجلة في التقارير السريرية، مما يسمح بالمقارنة جنبًا إلى جنب بين الممارسة الروتينية والأساليب الآلية.
كيف عمل الخبراء والذكاء الاصطناعي معًا
كان رسم مثل هذه المخططات التفصيلية عادة بطيئًا جدًا، لذا استخدم الفريق استراتيجية «الإنسان في الحلقة». رسم أخصائيو الأشعة والمقيمون صناديق ثلاثية الأبعاد تقريبية حول الأورام المشتبه بها، واقترح نموذج قوي للتقسيم يسمى MedSAM حدودًا أولية. ثم صحح المقيمون هذه الحدود، وأجرى أخصائيو الأشعة الكبار مراجعة نهائية. بعد كل دفعة من الصور المكتملة، أعيد تدريب نموذج الذكاء الاصطناعي على المخططات المحسّنة واستخدم لمساعدة الدفعة التالية. مع كل دورة، تقدم أداء النموذج ليقترب مما سيقبله الخبراء البشريون، مما خفف الجهد اللازم للتصحيحات الإضافية مع الحفاظ على الدقة.
ما تكشفه البيانات عن الأورام
لأن كل آفة في الصور تم تخصيصها ثلاثيًا، تمكن المؤلفون من دراسة أحجامها وكثافاتها بتفصيل. كانت معظم الأورام في الرئتين والكبد. ميّزت أورام الرئة بكونها صغيرة الحجم غالبًا لكن أقطارها الطويلة قد تكون نسبياً، في حين أظهرت العقد اللمفاوية أحجامًا أكبر لكن أقطارًا رئيسية أقصر إلى حد ما مقارنة بأورام الكبد. كما فحص الفريق سطوع أو ظلمة هذه المناطق على الأشعة المقطعية، وهي خاصية مرتبطة بكثافة النسيج. أظهرت أورام الرئة، المحاطة بالهواء، أنماط شدة مختلفة جدًا عن أورام الكبد والعقد اللمفاوية، ما يوحي بأن ميزات رقمية بسيطة من صور الأشعة المقطعية قد تساعد في تمييز أنواع الآفات. والأهم، أكدت الدراسة علاقة قوية بين أطول قطر للآفة وحجمها الثلاثي الأبعاد الحقيقي، ما يدعم فكرة أن قواعد مبنية على القطر مثل RECIST يمكن أن تعمل بديلاً عمليًا للقياسات الحجمية الكاملة عند تطبيقها بعناية.
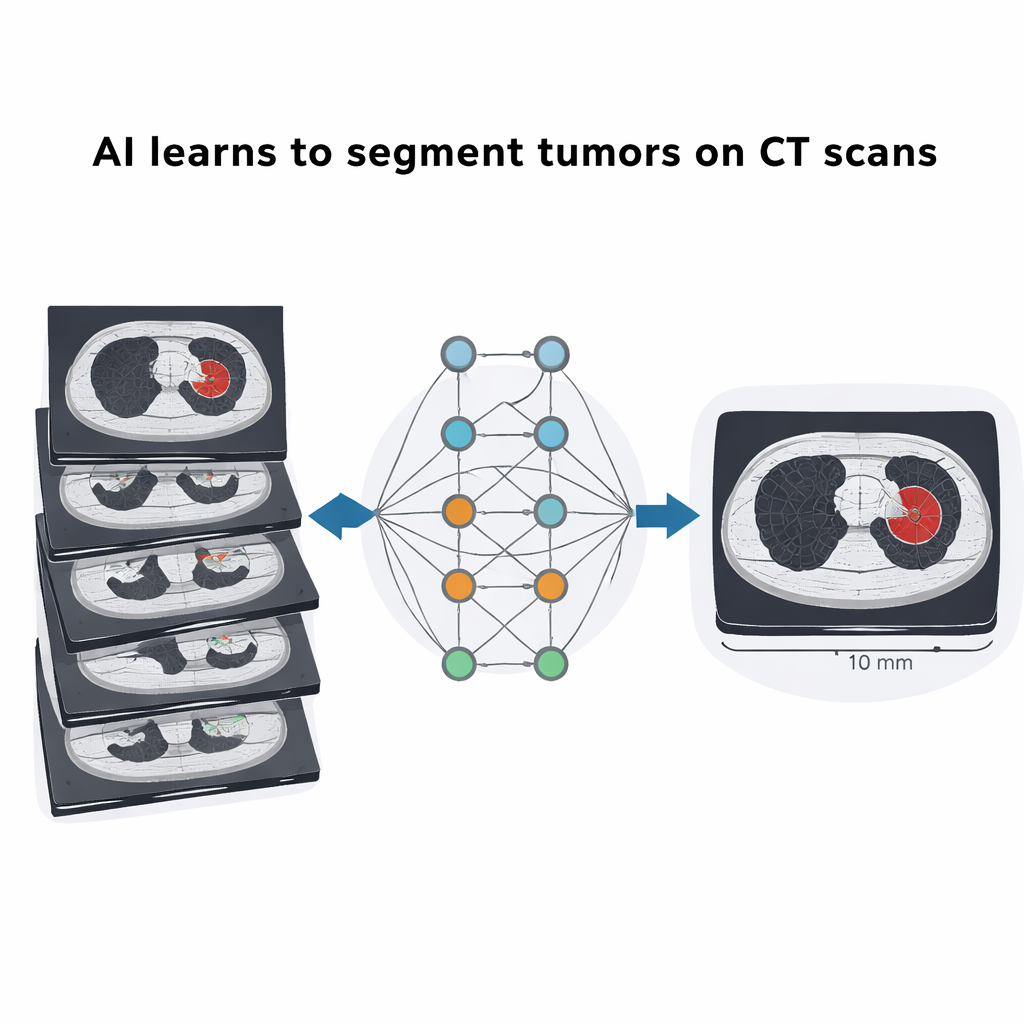
اختبار مجموعة البيانات بواسطة التعلم العميق
لإظهار كيفية استخدام المجموعة، درب الباحثون وحسّنوا نوعين من أنظمة التعلم العميق. أولًا، قاموا بضبط MedSAM ليفصل الأورام تلقائيًا من صناديق تحديد بسيطة، محققين درجات تداخل مع المخططات الخبيرة كانت في نفس نطاق النتائج المبلغ عنها على مجموعات بيانات دولية أكبر بكثير. ثانيًا، عدلوا إطار عمل شائع يسمى nnUNet، انطلقوا من نماذج مدربة على تحديات تصوير رئة وكبد عالمية ثم حسّنوها على هذه البيانات التشيلية الجديدة. بعد الضبط الدقيق، طابقت الأنظمة أو تفوقت على أدائها الأصلي، خصوصًا لأورام الرئة، رغم أن مجموعة المرضى كانت صغيرة نسبيًا. يوضح هذا أن بيانات محلية ممنهجة بعناية يمكن أن تعزز بشكل كبير موثوقية أدوات الذكاء الاصطناعي في بيئة مستشفى محددة.
ما يعنيه هذا لرعاية السرطان في المستقبل
لغير المتخصصين، الرسالة الأساسية هي أن هذه المجموعة أداة تمكينية، وليست منتجًا تشخيصيًا بحد ذاتها. من خلال المشاركة العلنية لصور الأشعة المقطعية التي تم فيها تحديد كل ورم وعقدة لمفاوية مرئية وفي كثير من الحالات قياسها بدقة، يوفر المؤلفون أرضية تدريب واقعية للخوارزميات التي تهدف إلى أتمتة تتبع الأورام. قد تساعد مثل هذه الأدوات أطباء الأشعة على قضاء وقت أقل في القياسات اليدوية ووقتًا أكبر في الأحكام المعقدة، مع تقليل التباين بين المقروئين. وبما أن البيانات تأتي من مستشفى في أمريكا اللاتينية وتم إصدارها بموجب ترخيص متساهل، فإنها تساهم أيضًا في ضمان اختبار الذكاء الاصطناعي الطبي على مرضى أكثر تنوعًا، مما يحسن فرص أن يعمل المراقبة الآلية للسرطان بشكل موثوق للأشخاص حول العالم.
الاستشهاد: Rojas-Pizarro, R., Vásquez-Venegas, C., Pereira, G. et al. A CT Dataset with RECIST Measurements and Comprehensive Segmentation Masks for Tumors and Lymph Nodes. Sci Data 13, 270 (2026). https://doi.org/10.1038/s41597-026-06597-6
الكلمات المفتاحية: تصوير السرطان, صور الأشعة المقطعية, تقسيم الأورام, RECIST, مجموعات بيانات الذكاء الاصطناعي الطبية