Clear Sky Science · ar
استقلاب فيتامين ب2 يعزز استقرار FSP1 لمنع الفيروسوبتوز
كيف يساعد فيتامين شائع الخلايا على اتخاذ قرار بين الحياة والموت
تسير خلايانا باستمرار على حبل مشدود بين البقاء وتدمير الذات. شكل درامي من موت الخلايا، يُسمى الفيروسوبتوز، جذب الانتباه لأنه قادر على قتل الخلايا السرطانية التي تقاوم علاجات أخرى بشكل انتقائي. تكشف هذه الدراسة أن مغذّياً يومياً — فيتامين ب2، أو الريبوفلافين — يلعب دوراً خفياً في إمالة الكفة عبر استقرار بروتين وقائي رئيسي. فهم هذا الرابط المخفي بين النظام الغذائي، واستقلاب الخلايا، وموت الخلايا السرطانية قد يساعد الباحثين على تصميم علاجات أذكى وصياغة نصائح غذائية مستقبلية أدق.
نوع خاص من الصدأ داخل الخلايا
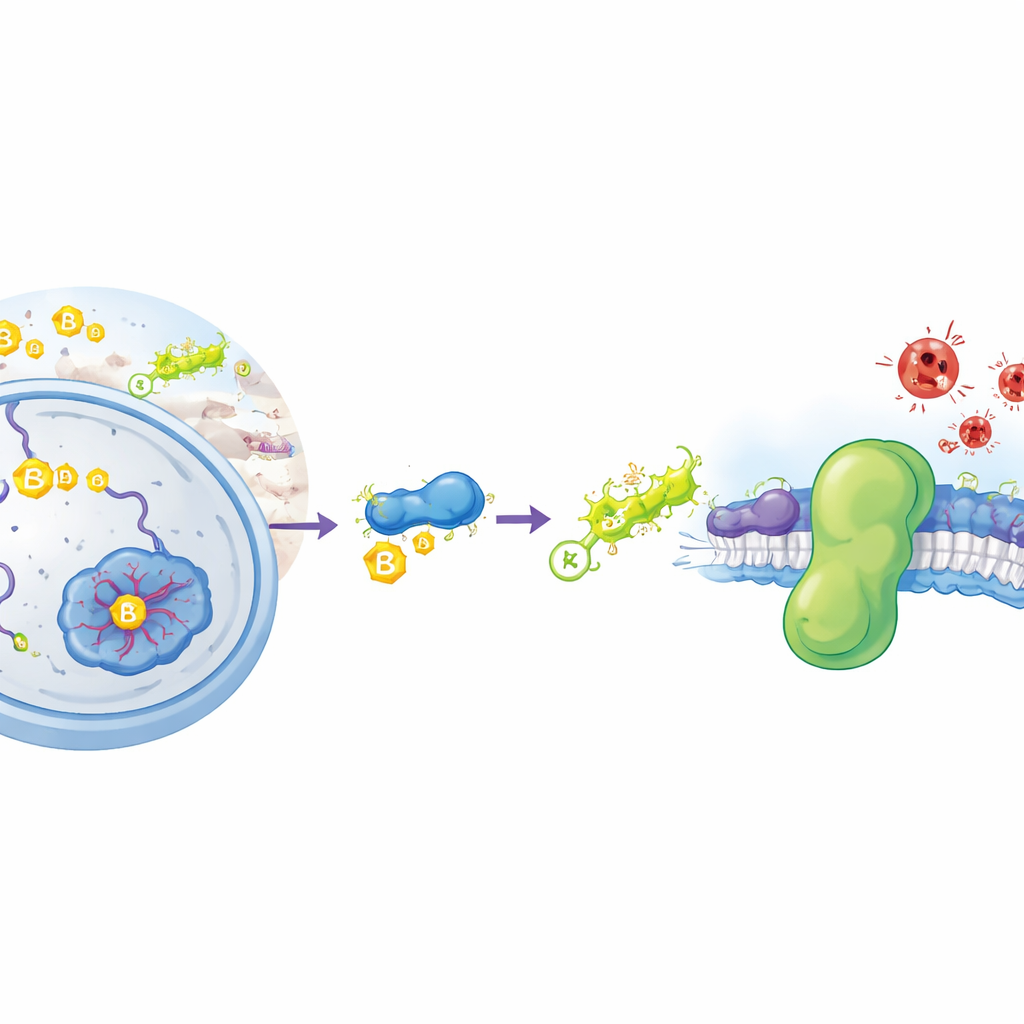
الفيروسوبتوز هو نوع من موت الخلايا مدفوع بعملية كيميائية تشبه صدأ المعادن: الأكسدة غير المنضبطة للدهون في أغشية الخلايا. عندما تتحلل هذه الدهون، تفقد الأغشية تكاملها وتنفجر الخلايا. عادة ما تستخدم خلايانا عدة دفاعات لمنع ذلك. أحد الدروع الرئيسة هو إنزيم يُسمى GPX4، والذي يستخدم جزيئاً صغيراً، الجلوتاثيون، لإزالة سمية بيروكسيدات الدهون. درع آخر موازٍ هو بروتين اسمه FSP1، يجلس على الأغشية الخلوية ويستخدم جزيئات دهنية صغيرة لاعتراض الجذور المدمرة قبل أن تنتشر. غالباً ما ترفع الخلايا السرطانية مستوى FSP1 لتجنب الفيروسوبتوز، مما يجعل هذا البروتين هدفاً بارزاً لأدوية مضادة للسرطان. ومع ذلك، لم يعرف العلماء حتى الآن كيف تتحكم الخلايا في مقدار إنتاج FSP1 ومدة بقائه.
بناء «مقياس وقود» خلوي لمانع الموت
لاكتشاف المديرين الخفيين لـ FSP1، قام الباحثون أولاً بتحوير خلايا سرطان العظم البشرية لحمل جهاز إبلاغ فلوري. وضعوا علامة على بروتين FSP1 الطبيعي بإشارة ضوئية خضراء وربطوه بإشارة زرقاء تبلغ عن مقدار رسالة FSP1 التي تصنعها الخلية. أتاح لهم هذا التصميم الذكي التمييز بين تغيّر النشاط الجيني (الأزرق) وتغيّر استقرار البروتين (الأخضر). ومع وجود هذا النظام ثنائي الألوان، استخدموا CRISPR–Cas9 لتعطيل تقريباً كل جين في الجينوم ثم فرز الخلايا ذات مستويات FSP1 العالية أو المنخفضة. بمقارنة مقاطع الدليل (guide RNAs) التي تزادت في كل مجموعة، رسموا خريطة لمئات الجينات التي إما تعزز أو تقلل FSP1، وتعمل على مستوى ضبط الجين أو تدوير البروتين.
الوظيفة الخفية لفيتامين ب2: صنع مقبض يثبّت البروتين
من بين النتائج اللافتة كان اثنان من الإنزيمات، كيناز الريبوفلافين (RFK) وسينثاز FAD (FLAD1)، اللذان يحولان فيتامين ب2 إلى عامل مساعد يُسمى FAD. FSP1 هو بروتين فلافيني يرتبط عادةً بـ FAD بإحكام لأداء تفاعلاته الكيميائية. عندما تم إزالة RFK أو FLAD1، أو عندما نمت الخلايا في وسط ناقص لفيتامين ب2، هبطت مستويات بروتين FSP1 بشدة رغم أن نشاط جينه بقي مشابهاً. أظهر الفريق أن هذا الفقد جعل الخلايا أكثر عرضة للفيروسوبتوز عندما تم حجب GPX4. ومن المهم أن فيتامين ب2 نفسه لم يتصرف كعامل مضاد للأكسدة الكلاسيكي: في اختبار حساس في أنبوب اختبار فشل في إيقاف أكسدة الدهون، على عكس فيتامين E. بدلاً من ذلك، استعادة إضافة FAD (وبدرجة أقل مسبقه FMN) إلى الخلايا الناقصة كل من مستويات FSP1 والمقاومة للموت الفيروسوبتوزي، بينما لم يكفِ فيتامين ب2 الإضافي وحده إذا كانت إنزيمات المعالجة مفقودة.
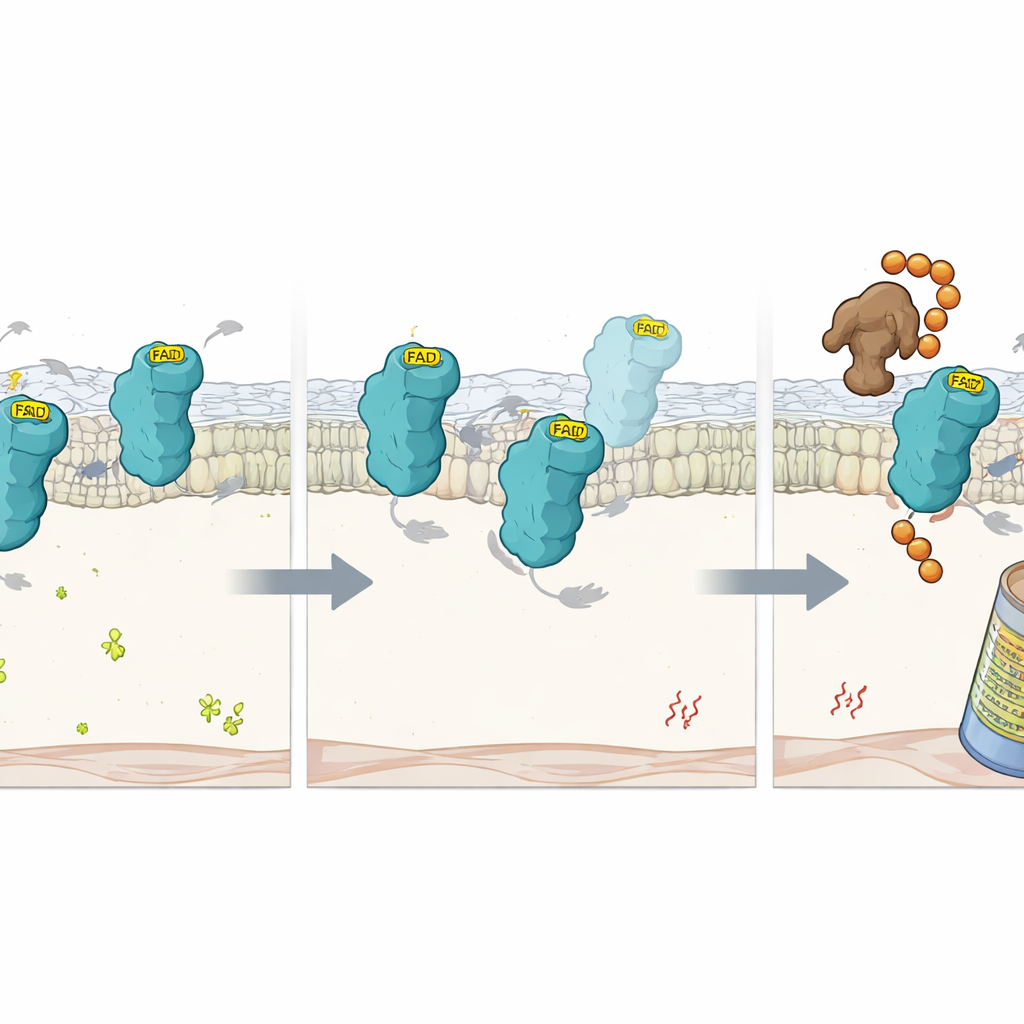
ماذا يحدث عندما يختفي العامل المساعد
للتدقيق أكثر، درس العلماء طفرات دقيقة في FSP1 تُضعف قدرته على الاحتفاظ بـ FAD. هذه البروتينات الطافرة ظلت مطوية بأشكال شبه طبيعية لكنها فقدت FAD والنشاط التحفيزي. داخل الخلايا، تآكلت هذه النسخ أسرع بكثير من FSP1 الطبيعي، ما لم يُمنع البروتيازوم — آلة ت shredding البروتينات في الخلية. هذا يقترح أن ارتباط FAD نفسه يعمل كمقبض يثبت FSP1 ويحميه من أن يُوسم كمعطوب. باستخدام شاشة CRISPR مركزة أخرى تحت ظروف انخفاض FAD، حدد الفريق لِيغاز E3 يُدعى RNF8 كعامل رئيسي يتعرف على FSP1 الخالي من FAD. عندما حُذف RFK، ربط RNF8 سلاسل من وسم اليوبكويتين بالبروتين الفارغ، مستهدفا إياه للتدمير عبر البروتيازوم. إلغاء RNF8 أبطأ تدوير FSP1 في الخلايا الفقيرة بـ FAD، رغم أنه لم يستعد وظيفته الوقائية المفقودة بدون العامل المساعد.
من الدوائر الجزيئية إلى أفكار علاجية للسرطان
بجمع هذه القطع، يقترح المؤلفون نموذجاً بسيطاً لكنه قويًا. فيتامين ب2، بعد تحويله إلى FAD بواسطة RFK وFLAD1، يرتبط بـ FSP1 وهو ضروري لكل من نشاطه الكيميائي وطول عمره. عندما يتعثر إمداد فيتامين ب2 أو معالجةه، لا يستطيع FSP1 المشكل حديثاً تأمين FAD، فيوسم بواسطة RNF8 ويُفكك بسرعة بواسطة البروتيازوم، تاركاً الخلايا أكثر عرضة لضرر الفيروسوبتوز. تشير بيانات السرطان إلى أن الأورام ذات التعبير الأعلى عن RFK أكثر مقاومة لأدوية تحفز الفيروسوبتوز، مما يبرز الصلة العملية لهذا المسار. للقراء غير المتخصصين، الرسالة الأساسية هي أن فيتامين مألوف يفعل أكثر من كونه مضاد أكسدة بسيط: يساعد في تقرير ما إذا كان بروتين مضاد للموت قوي سيصون الحراسة أو يُزال. من خلال ضبط استقلاب فيتامين ب2 أو استقرار FSP1، قد تستغل العلاجات المستقبلية الفيروسوبتوز بشكل أفضل للقضاء على الخلايا السرطانية مع الحفاظ على الأنسجة السليمة.
الاستشهاد: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
الكلمات المفتاحية: الفيروسوبتوز, فيتامين ب2, FSP1, موت الخلايا السرطانية, استقلاب الخلايا