Clear Sky Science · ar
خرائط الهجائن بين العناصر القافزة والجينات، نشأتها ودورها في تعزيز مرونة النسخ
ركاب خفيون في حمضنا النووي
جزء كبير من حمضنا النووي مكوّن من رُكّاب فيروسية قديمة تسمى العناصر المتنقلة — أجزاء من الشفرة الوراثية كانت تقفز عبر الجينومات كطفيلية متسلّقة. تُظهر هذه الدراسة أن بقايا الفيروسات القديمة هذه ليست مجرد خردة صامتة: يمكن أن تندمج في جيناتنا لتكوّن رسائل هجينة، تُسهم في تكيّف الخلايا مع الظروف المتغيرة، وأحيانًا تغذي المرض. من خلال رسم خرائط هذه الهجائن عبر التطور والشيخوخة والسرطان، يكشف المؤلفون عن طريقة مفاجئة يستمر بها الحمض الفيروسي في تشكيل البيولوجيا البشرية اليوم.
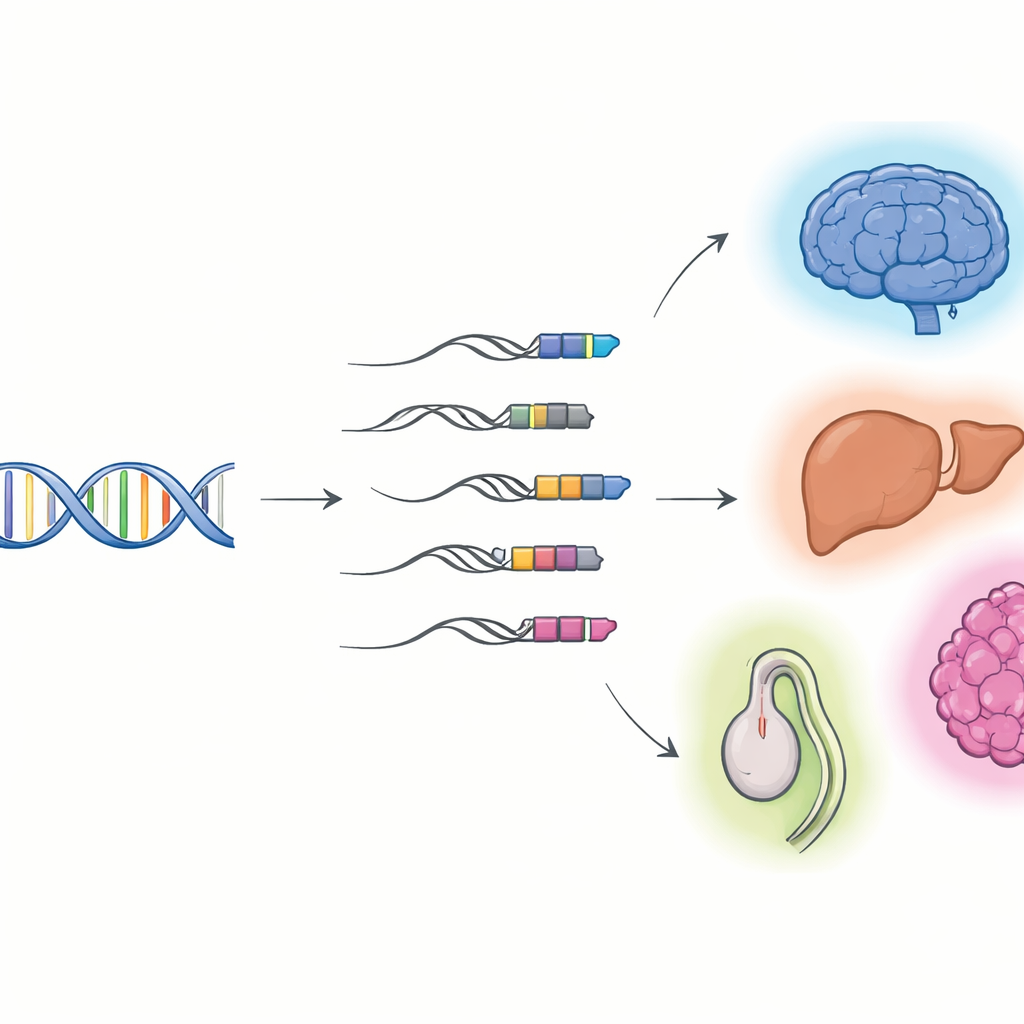
عندما يصبح الحمض الفيروسي جزءًا من جيناتنا
تركّز الباحثون على «هجائن عنصر متنقل–جين»: جزيئات RNA تبدأ في عنصر متنقل ثم تستمر داخل جين مضيف. باستخدام التسلسل طويل القراءة، الذي يمكنه التقاط جزيئات RNA كاملة من الطرف إلى الطرف، وبالدمج مع التسلسل قصير القراءة التقليدي، بنوا فهارس مفصّلة لهذه الهجائن في خلايا وأعضاء الفأر والإنسان. وجدوا آلاف النسخ الهجينة غير المعروفة سابقًا، معظمها RNAs غير مرمّزة بدلًا من مخططات بروتينية. يبدأ الكثير منها في فئة من بقايا الفيروسات تُسمى النهاية الطرفية الطويلة (LTRs)، التي غالبًا ما تجلس في واجهة الجينات ويمكن أن تعمل كمفاتيح تبديل بديلة. تستعمل أنسجة وأعضاء مختلفة مجموعات مختلفة من هذه الهجائن، مع نشاط غني خاصة في الدماغ والكبد والخصية، ويتغير نمط استخدامها مع تطور الأنسجة من المراحل الجنينية إلى البالغة.
الهجائن في الشيخوخة والسرطان
لمعرفة كيف تتصرف هذه الهجائن الفيروسية–المضيفة في مجموعات سكانية حقيقية، استغل الفريق مجموعات بيانات بشرية كبيرة تغطي عشرات الأنسجة من مئات الأشخاص، فضلاً عن عينات أورام. حدّدوا عدة مئات من الهجائن ذات الثقة العالية التي تتكرر عبر الأفراد. يتباين تعبيرها ليس فقط بين الأعضاء ولكن أيضًا مع العمر: في أنسجة مثل الدم والدماغ، تنخفض بعض الهجائن المدفوعة بـLTR في البالغين الأكبر سنًا، بينما تزداد في بعض الأنسجة المحيطية. في أنواع عديدة من السرطان، ترتفع هذه الهجائن القائمة على LTR على نطاق واسع في الأورام مقارنة بالأنسجة الطبيعية المجاورة، والمرضى الذين تعبر أورامهم عن مزيد منها يميلون إلى نتائج أسوأ. في مجموعات بيانات لأشخاص مقاومين للعلاج الكيميائي أو المناعي، تقع الجينات المتأثرة بإكسونات جديدة مدفوعة بـLTR غالبًا في مسارات مرتبطة بكيفية عمل تلك الأدوية، ما يوحي بأن هجائن العناصر المتنقلة قد تساعد الأورام على إعادة توصيل نفسها تحت ضغط العلاج.
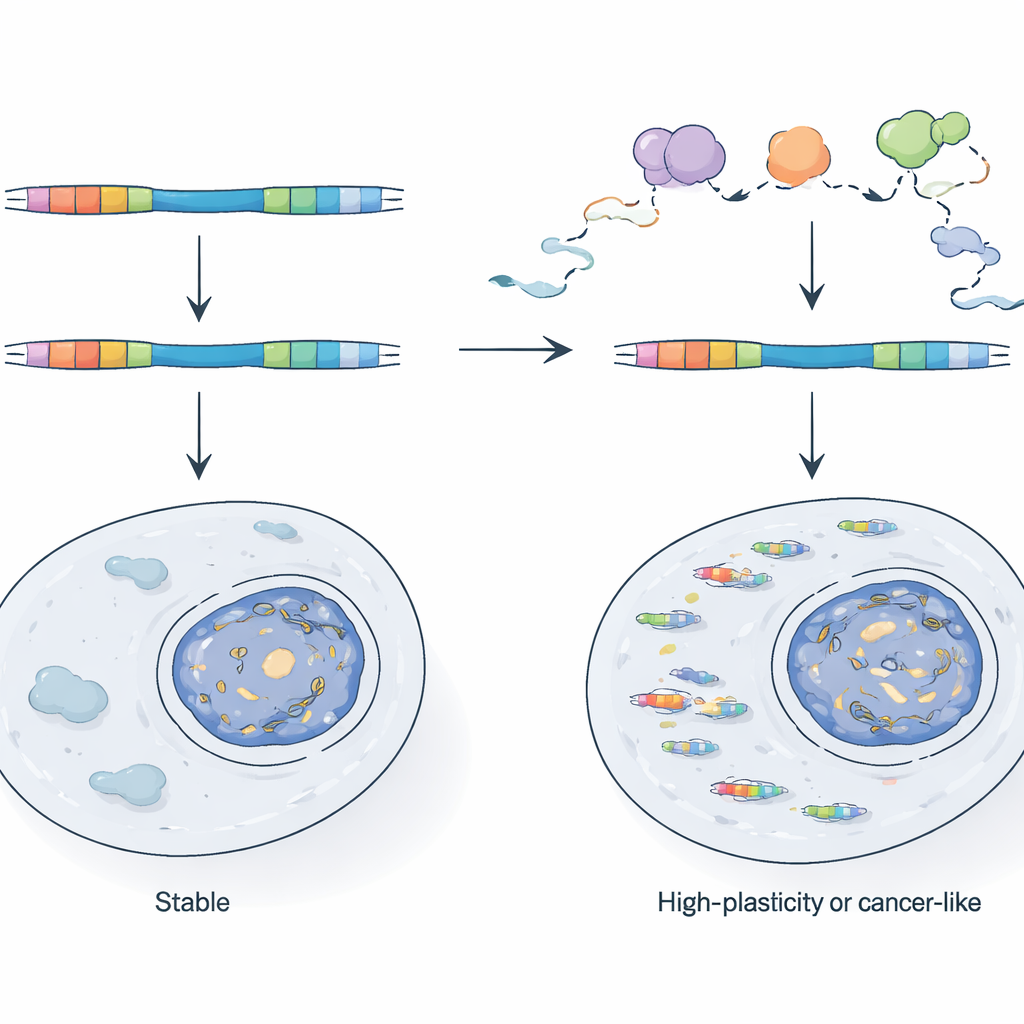
كيف تُبقي الخلايا الهجائن الفيروسية تحت السيطرة
بالنظر إلى فعاليتها، لماذا لا تُغرق هجائن العناصر المتنقلة الخلايا الطبيعية؟ يبيّن المؤلفون أن الخلايا تعتمد على نظام رقابة نوعية للـRNA، يتمحور حول مركب الإكسوسوم النووي، ليتفقد ويُدمر العديد من هذه النسخ أثناء إنتاجها. عندما يعطّلون وراثيًا مركبًا رئيسيًا من الإكسوسوم في خلايا جذعية فأرية، تصبح محفزات LTR أكثر نشاطًا بكثير وتزداد RNAs الهجينة. بالمقارنة بين الـRNA المُنتَج حديثًا والـRNA المستقر، يوضحون أن بعض الـLTRs تُحجز عادةً لأن نسخها تُتلف بسرعة، بينما تُسيطر أخرى على مستوى تكرار بدء النسخ. تميل هذه LTRs النشطة إلى الجلوس في مناطق جينومية بالفعل قابلة للوصول وغالبًا ما تكون متَرجمة، ما يشير إلى أن القرب من جين نشط أو نسخ مضاد قد يساعد قطعة فيروسية على الهروب من الصمت اللاجيني التقليدي.
التوصيل الإحصالي، مرونة الخلايا الجذعية، و"مفتاح رئيسي" فيروسي
تتعقد القصة عندما تتعرّض آلية الربط (splicing) في الخلية للاختلال. يقوم المؤلفون بتقليل عدد عدة عوامل ربط أساسية أو يثبّطون جزيئيًا المسبك المسؤول عن الربط ولاحظوا نتيجة مشتركة مع فقد الإكسوسوم: زيادة قوية في الهجائن المدفوعة بـLTR وفي الجينات القصيرة الفقيرة بالإنترونات. من بين الفائزين MERVL، فيروس رترووني داخلي نشط في مراحل مبكرة جدًا لأمشاج الفأر. عندما تُرفَع كمية سلسلة MERVL الداخلية وعوامل النسخ التالية، تتحول الخلايا الجذعية إلى حالة أقرب إلى "شمولية القدرة"، تشبه الخلايا الجنينية المبكرة القادرة على تكوين جميع الأنسجة. وبالمقابل، يؤدي تدهور RNA المERVL باستخدام أوليغونوكليوتيدات مضادة إلى إضعاف هذا التحول وتقليل نشاط محفزات LTR، مما يشير إلى أن MERVL يعمل كمفتاح رئيسي يمكنه تشغيل شبكة أوسع من هجائن العناصر المتنقلة ومرونة حالة الخلية.
الابتكار الفيروسي عبر التطور
عبر النظر في العديد من الجينومات الثديية، يتتبع الفريق متى بدأت عائلات مختلفة من العناصر المتنقلة في التبرع بإكسونات للجينات المضيفة. في كل من البشر والفئران، تكون عائلات LTR الناشئة نسبيًا أكثر ميلًا لتكوين هجائن باتجاه "الحس" (sense) التي يمكن قراءتها كجزء من النسخ المضيفة. يوحي هذا النمط بأن موجات جديدة من إدخالات العناصر المتنقلة قد زوّدت مرارًا المادة الخام لشبكات تنظيم الجينات عبر الزمن التطوري. بدل أن تكون ضارة ببساطة، يمكن اختبار هذه الإدخالات بواسطة آليات النسخ والتحلل في الخلية: معظمها يُسكت أو يُتلف، لكن أقلية تجد نفسها في المكان والسياق المناسب لتُستغل كعناصر تنظيمية مفيدة أو بدايات جينية جديدة.
لماذا تهمنا هذه البقايا الفيروسية
لهذا العمل رسالة واضحة لغير المتخصص: جزء كبير كان يُستهان به من جينومنا يشكل بنشاط كيفية قراءة الجينات، وكيفية تغير هوية الخلايا، وكيف تتقدم الأمراض. يمكن تحويل تسلسلات فيروسية قديمة إلى "بوابات" بديلة للجينات، منتجة RNAs هجينة عادة ما يراقبها نظام تنظيف خلوي. عندما يضعف هذا النظام أو يتعطل الربط العادي، يمكن أن تنتشر هذه الهجائن، دافعة الخلايا الجذعية إلى حالات أكثر مرونة أو مساعدة الأورام على التكيّف والمقاومة. على مدى ملايين السنين، عبث التطور باستمرار بهذه القطع الفيروسية، محوّلًا الكثير منها من طفيليات جينومية إلى لبِنات لبنية تنظيمية معقدة — تاركًا لنا نسخة من النسخيات (transcriptome) أكثر مرونة وديناميكية مما قد توحي به قائمة بسيطة من الجينات.
الاستشهاد: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
الكلمات المفتاحية: العناصر المتنقلة, النسخ الهجينة, مراقبة الحمض النووي الريبي, مرونة الخلايا الجذعية, تطور السرطان