Clear Sky Science · ar
تكيّف استيراد البروتين الميتوكوندري مع الإجهاد عبر تحلل DNAJC15 بواسطة OMA1
كيف تتعامل خلايانا عندما تتعرّض مصانعها للطاقة للإجهاد
تعتمد كل خلية في جسمك على هياكل صغيرة تُدعى الميتوكوندريا لتحويل الغذاء إلى طاقة قابلة للاستخدام. مثل المصانع المصغّرة، تستورد الميتوكوندريا باستمرار أجزاء جديدة—بروتينات مصنوعة في أماكن أخرى من الخلية—لتبقي آلتها تعمل. تكشف هذه الورقة كيف أن الخلايا، عند تعرض الميتوكوندريا للإجهاد أو الضرر، تقلّ عمدًا من نشاط خط استيراد البروتينات هذا. من خلال ذلك، تحمي نفسها من التحميل الزائد وتنسّق استجابة إجهاد أوسع تشمل ليس الميتوكوندريا فحسب، بل أيضًا حجرة رئيسية أخرى وهي الشبكة الإندوبلازمية.
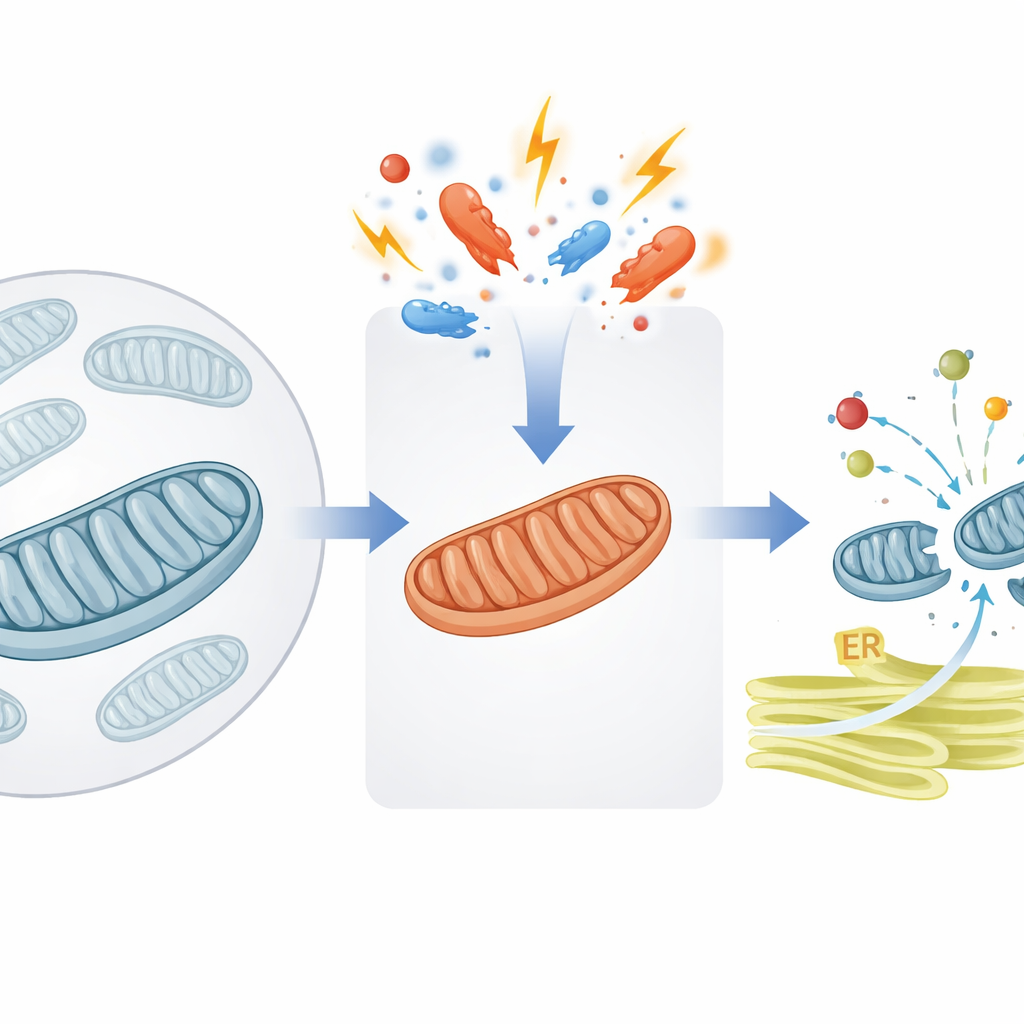
صمام أمان لحركة البروتينات الميتوكوندرية
تعتمد الميتوكوندريا على آلاف البروتينات التي تُبنى أولًا في الحجرة الرئيسية للخلية ثم تُرسَل إلى داخلها. يركّز المؤلفون على بوابة حاسمة في الغشاء الداخلي للميتوكوندريا، يدعمها بروتين مساعد يُدعى DNAJC15. في الظروف الطبيعية، يساعد DNAJC15 على سحب «حزم» البروتين الجديدة عبر قناة الاستيراد وإدخالها إلى جوف الميتوكوندريا، حيث يصبح العديد منها جزءًا من الآلة المنتجة للطاقة المعروفة بالفوسفورية التأكسدية (OXPHOS). تُظهر الدراسة أنه عندما تتعرض الميتوكوندريا للإجهاد—مثل تعرّض إنتاج الطاقة للخلل أو تغير خصائص الغشاء—تُفعَّل خلية مفاتيح جزيئية تغيّر كمية البروتين التي تقبل العضية استيرادها.
OMA1: القاطع المنشّط بالإجهاد
في قلب هذا المفتاح يوجد إنزيم حساس للإجهاد يدعى OMA1، موضوعة في الغشاء الداخلي للميتوكوندريا. عندما تواجه الميتوكوندريا مشاكل، ينشط OMA1 ويقطع DNAJC15 عند موقع محدد قرب بدايته. ينتج عن هذا القطع نسخة أقصر من DNAJC15 تتعرّض بسرعة للتفكك بواسطة مجمّع إنزيمي ميتوكوندري آخر يُسمى بروتياز m-AAA. نتيجة لذلك، يُفقد الشكل الكامل والطويل لـ DNAJC15 القادر على دعم الاستيراد. يبيّن المؤلفون أن الخلايا التي تفتقر إلى DNAJC15، أو تلك التي يتعرّض فيها DNAJC15 للتدمير السريع بعد تنشيط OMA1، تملك قدرة منخفضة على إدخال بروتينات جديدة إلى الميتوكوندريا، خاصة تلك اللازمة لبناء وصيانة مركبات الفسفورية التأكسدية.
تباطؤ تجميع الطاقة ليتوافق مع حالة الميتوكوندريا
باستخدام قياسات شاملة للبروتينات وتجارب استيراد، وجد الفريق أن DNAJC15 مهم بشكل خاص لتزويد جوف الميتوكوندريا ببروتينات تشارك في التعبير الجيني وتركيب سلسلة التنفس. عندما يغيب DNAJC15، تتراكم هذه البروتينات ببطء أكبر داخل الميتوكوندريا، وتنخفض قدرة العضيات على استهلاك الأكسجين وتغذية إنتاج الطاقة—كما تقاس في ميتوكوندريا معزولة—خاصة بالنسبة للمركب I في سلسلة التنفس. مكوّن آخر من قناة الاستيراد، TIMM17A، يعمل جنبًا إلى جنب مع DNAJC15: يؤدي فقدان كليهما إلى عيوب قوية في مستويات بروتينات الريبوزوم الميتوكوندري ومكونات OXPHOS. تقترح هذه النتائج مجتمعة أن تدمير DNAJC15 بوساطة OMA1 هو وسيلة لوقف مؤقت لبناء آلات الطاقة الجديدة حتى تتعافى العضية.
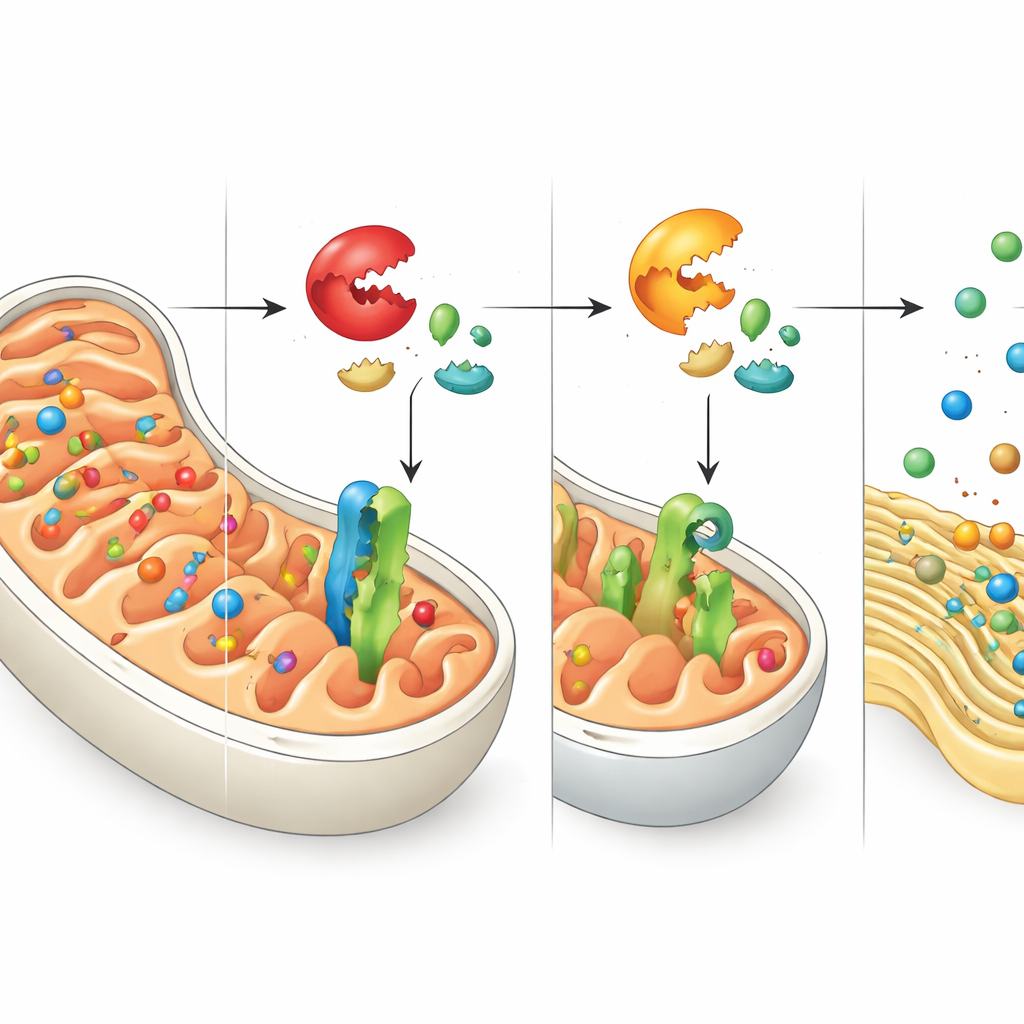
حزم مُشوّهة ونداء مساعدة من الشبكة الإندوبلازمية
إيقاف عمل DNAJC15 لا يمنع الخلية من صنع بروتينات ميتوكوندرية—إنما يمنعها أساسًا من الوصول إلى وجهتها المقصودة. تتبّع المؤلفون مصير هذه البروتينات العالقة ووجدوا أن العديد منها ينتهي في الشبكة الإندوبلازمية (ER)، شبكة الأغشية التي تساعد عادةً في طي ومعالجة مجموعات مختلفة من البروتينات. تستقر هذه البروتينات الميتوكوندرية الضالة في أغشية الشبكة الإندوبلازمية، مما يزعزع توازن مراقبة الجودة في الشبكة نفسها. استجابةً لذلك، تُفعّل الخلية برنامجًا وقائيًا يعرف باستجابة البروتين غير المطوي (UPR)، وبشكل خاص عبر فرع يتحكم فيه المستشعر ATF6. تعزّز هذه الاستجابة قدرة الشبكة الإندوبلازمية على معالجة البروتينات غير المطوية أو المحوّلة الخطأ، مكشوفةً تنسيقًا وثيقًا بين أنظمة إجهاد الميتوكوندريا وER.
تباطؤ منسّق لحماية الخلية
تجمع الدراسة صورة لنظام فرامل مدمج لتكوين الميتوكوندريا. عندما تتعرض الميتوكوندريا للإجهاد، يقوم OMA1 بتقليم وبتؤديكًا بتدمير DNAJC15، مما يقلّل تدفق البروتينات الجديدة المتعلقة بالطاقة إلى العضيات المتضررة. تُخزّن بعض هذه البروتينات مؤقتًا في الشبكة الإندوبلازمية، التي تطلق بدورها استجابة وقائية. من خلال ربط قدرة الاستيراد الميتوكوندرية بصحة العضية، وبإشراك الشبكة الإندوبلازمية كموقع احتياطي للبروتينات الزائدة، تستطيع الخلايا تجنّب سد الميتوكوندريا التالفة وكسب وقت لإصلاحها أو إزالتها بالكامل. للملاحظ العادي، تُظهر هذه العمل إلى أي مدى تتكامل أنظمة مراقبة الجودة داخل الخلية: حتى أصغر الأخطاء في حجرة واحدة تُحس وتُعاد معالجتها من قبل حجرات أخرى للحفاظ على إنتاج الطاقة—وبالتالي الحياة—على المسار الصحيح.
الاستشهاد: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
الكلمات المفتاحية: إجهاد ميتوكوندري, استيراد البروتينات, مراقبة جودة خلوية, الفوسفورية التأكسدية, الشبكة الإندوبلازمية