Clear Sky Science · ar
AF2BIND: التنبؤ بمواقع ارتباط الجزيئات الصغيرة باستخدام تمثيل الأزواج في AlphaFold2
البحث عن أهداف دوائية في بحر من البروتينات
تعمل الأدوية الحديثة غالباً عن طريق الالتصاق بتجاويف وثنايا صغيرة على أسطح البروتينات داخل خلايانا. ومع ذلك، وحتى مع وجود قواعد بيانات ضخمة لهياكل البروتين الحالية، لا يزال من الصعب بشكل مفاجئ التنبؤ مسبقاً بالمواقع التي قد يلتصق بها جزيء صغير — محتمل أن يكون دواءً. تقدّم هذه الدراسة أداة حاسوبية بسيطة لكنها قوية تسمى AF2BIND، تستخلص معلومات من الطبقات الداخلية لـ AlphaFold2، النموذج الرائد لتوقع بنية البروتينات، لتسليط الضوء على مواقع محتملة لارتباط الأدوية عبر آلاف البروتينات البشرية. هدفها هو تضييق نطاق البحث عن أدوية جديدة وكشف بقع وظيفية مخفية تتغاضى عنها الأساليب التقليدية.
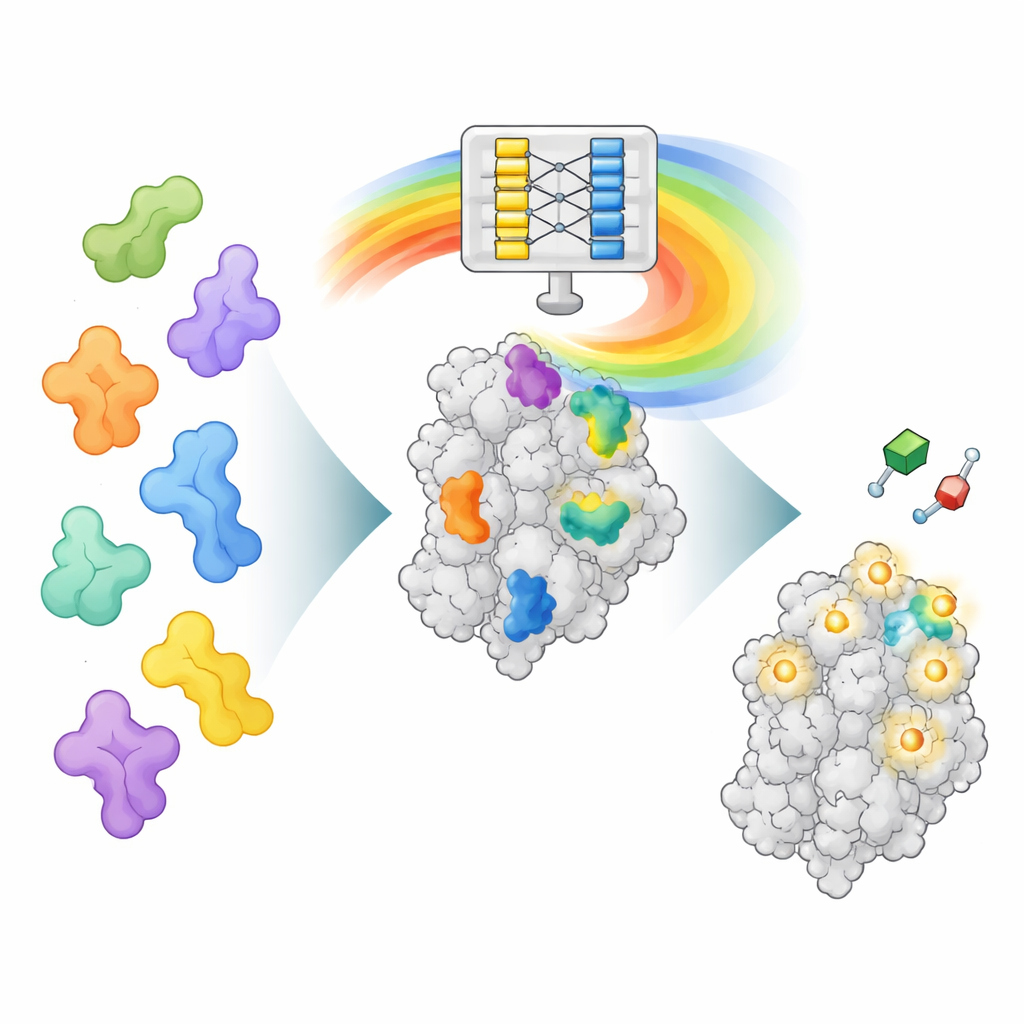
طريقة جديدة لقراءة «عقل» AlphaFold
تم تدريب AlphaFold2 على توقع كيفية طي سلسلة الأحماض الأمينية إلى بروتين ثلاثي الأبعاد، وليس على العثور على مواقع ارتباط الأدوية. ومع ذلك، أثناء تعلمه لطي البروتينات، اكتسب أيضاً أنماطاً غنية حول كيفية تفاعل أجزاء البروتين المختلفة. تستغل AF2BIND إحدى طبقات البيانات الداخلية هذه، المسماة تمثيل الأزواج، التي تُشفّر كيفية ارتباط كل زوج من مواقع الأحماض الأمينية في الفراغ. يقدم المؤلفون إلى AlphaFold2 سلسلة البروتين مع هيكله الخلفي، ويضيفون أيضاً 20 حمضاً أمينياً إضافياً، واحداً من كل نوع، كسلاسل «طُعم» منفصلة. ثم يحسب AlphaFold2 كيفية تفاعل البروتين مع كل بقايا طُعم. تصبح أنماط التفاعل هذه مدخلاً إلى نموذج انحدار لوجستي بسيط يقدّر، لكل موضع في البروتين، احتمال كونه جزءاً من موقع ارتباط بجزيء صغير.
تحويل الإشارات المخفية إلى تنبؤات عملية
تطلب تدريب AF2BIND مجموعة مُحكَمة بعناية تضم نحو 1900 بنية بروتين–الليجاند حيث ارتبطت جزيئات صغيرة بدليل تجريبي عالي الجودة. بذل الباحثون جهوداً كبيرة لتجنّب «الغش» عبر التشابه: قسموا بياناتهم بحيث لا تشارك البروتينات في مجموعة الاختبار شكل الطي العام أو التسلسل أو حتى شكل جيب الارتباط مع تلك المستخدمة للتدريب. على هذا المعيار الصارم، تفوّق تمثيل الأزواج من AF2 على العديد من التضمينات البديلة للشبكات العصبية، بما في ذلك تلك المعتمدة فقط على التسلسل أو على تصميم تسلسلي مشروط بالهيكل. باستخدام ميزات الأزواج وحدها، استعاد AF2BIND نحو ثلثي البقايا المعروفة للارتباط في التنبؤات الأعلى تقييماً وأظهر أداءً قوياً عبر مقاييس التصنيف القياسية، مع بقاءه متيناً تجاه تغيّرات متوسطة في شكل البروتين وتوجيهات السلاسل الجانبية.
قراءة الأدلة الكيميائية من بقايا الطُعم
بما أن AF2BIND نموذج خطي بسيط، فإن قراراته شفافة بشكل غير معتاد بالنسبة لنظام ذكاء اصطناعي حديث. يساهم كل من الأحماض الأمينية العشرين للطُعم بمقدار قابل للقياس إلى درجة النقاط النهائية للارتباط في موضع بروتيني معيّن. من خلال فحص هذه المساهمات عبر نحو 2000 مركب بروتين–ليجاند، وجد المؤلفون أن تركيبات طُعم معينة تتفاعل بقوة أكبر مع الليجانديات الزيتية الغنية بالكربون، بينما تضيء تركيبات أخرى لليجاندات الأكثر قطبية والمحبّة للماء. بعبارة أخرى، يعمل نمط تفعيل الطُعم كالبصمة الكيميائية الأولية لنوع الجزيئات الصغيرة التي يفضّلها جيب معيّن. يشير ذلك إلى أن نهجاً شبيهاً بـ AF2BIND قد لا يكتفي مستقبلاً بالإشارة إلى مكان ارتباط الدواء فحسب، بل قد يوحي أيضاً بنوع الكيمياء الأنسب له.
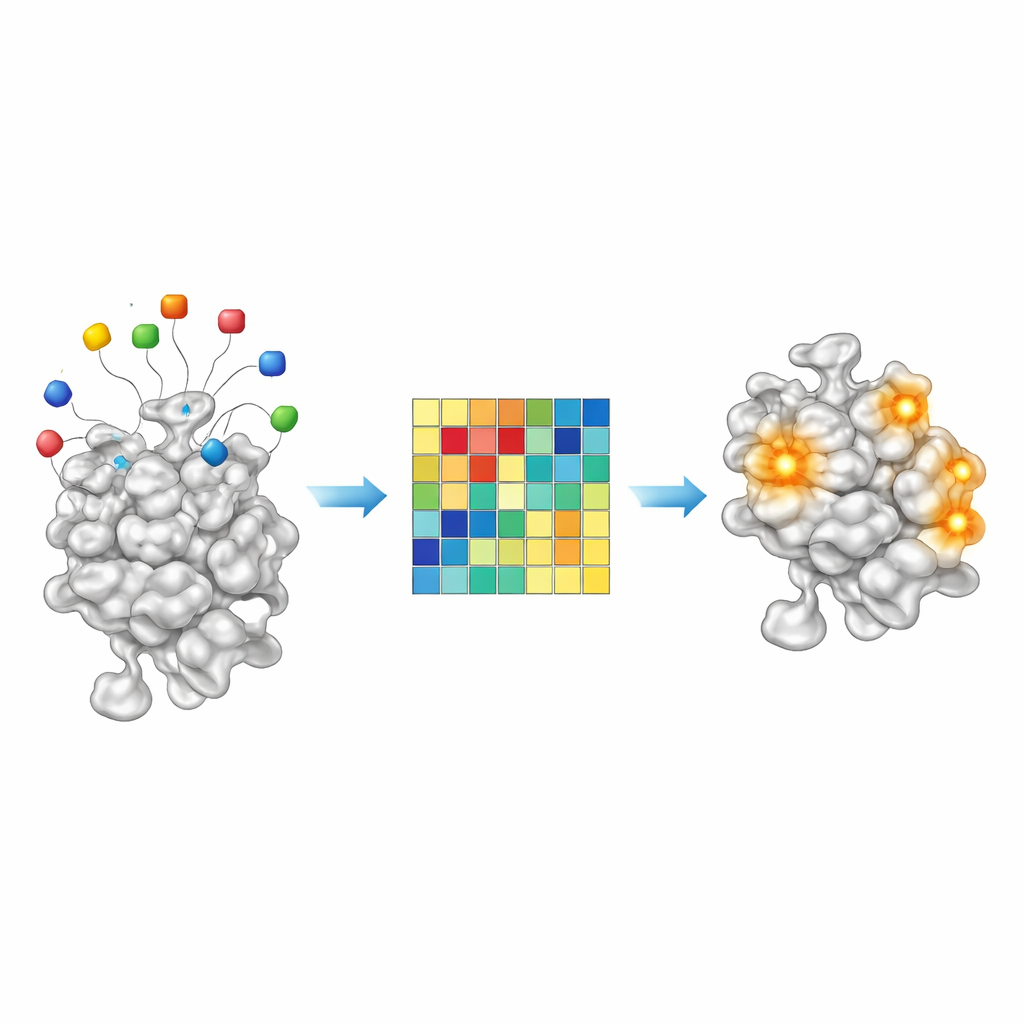
مسح البروتيوم البشري بحثاً عن جيوب جديدة
مسلحين بالنموذج المدرب، أطلق الفريق AF2BIND على هياكل البروتيوم البشري المتوقعة بواسطة AlphaFold. بعد إزالة المناطق منخفضة الثقة وتقسيم البروتينات الكبيرة جداً إلى قطع هيكلية قابلة للإدارة، جمعوا البقايا عالية الدرجات القريبة في مواقع ترشيحية لارتباط. توقّع AF2BIND أكثر من 20,000 موقع من هذا النوع في أكثر من 13,000 بروتين. ومن اللافت أن غالبية هذه المواقع لم تتداخل مع الجيوب المستنتجة بواسطة طرق تعتمد على النماء المشترك مثل AlphaFill، التي تنسخ الليجاندات من هياكل بلورية ذات صلة، ولا مع أداة اكتشاف الجيوب الشائعة P2Rank. العديد من المواقع الفريدة لـ AF2BIND أضحلت أقل عمقاً أو أكثر انتشاراً من الجيوب المضمّنة الكلاسيكية وغالباً ما تتزامن مع مناطق ترتبط بالببتيدات أو الرنا أو الحمض النووي أو بروتينات أخرى — واجهات قد تظل قابلة للاستهداف بواسطة جزيئات صغيرة.
دلالات لاكتشاف الأدوية والمرض
لتقييم مدى وعد هذه المواقع المقترحة لتصميم الدواء، استخدم المؤلفون أداة مستقلة تقيم «قابلية الدواء» استناداً إلى حجم الجيب واحتوائه والبيئة الكيميائية. في المتوسط، سجّلت مواقع AF2BIND درجات أعلى من عتبة شائعة للأهداف الدوائية الجذابة، بما في ذلك تلك الموجودة في بروتينات مرتبطة بأمراض وراثية. عند مطابقتها مع تجارب كيموبرتوماتيكس التي تميّز السيستئين التفاعلية في الخلايا، فسّر كل من AF2BIND وP2Rank معاً ما يقرب من نصف المناطق القابلة للترابط الملاحَظة، حيث كشف كل منهما حالات لم تلتقطها الأخرى. تُظهر هذه العمل أن التمثيلات الداخلية التي تتعلمها شبكات التنبؤ بالهياكل يمكن إعادة توظيفها لرسم خرائط لمواقع ارتباط محتملة على نطاق واسع، دون معرفة مسبقة بأي ليجاند محدد. للقراء غير المتخصصين، الرسالة الأساسية هي أن نفس اختراقات الذكاء الاصطناعي التي تتنبأ بأشكال البروتينات بدأت تكشف أين وكيف قد تتمكن الأدوية من الإمساك بتلك الأشكال، مما قد يسرّع البحث عن علاجات جديدة ويسلّط الضوء على نقاط ضبط خفيّة في بروتيناتنا.
الاستشهاد: Gazizov, A., Lian, A., Goverde, C. et al. AF2BIND: predicting small-molecule binding sites using the pair representation of AlphaFold2. Nat Methods 23, 626–635 (2026). https://doi.org/10.1038/s41592-026-03011-2
الكلمات المفتاحية: مواقع ارتباط البروتين, اكتشاف الأدوية, AlphaFold2, علم الأحياء الحاسوبي, المعلوماتية الحيوية الهيكلية