Clear Sky Science · ar
DECODE: إطار فكّ اختلاط عام قائم على التعلم العميق لبيانات الأومكس المختلفة
لماذا تهمّ هذه الدراسة
تغرق الطب الحيوي الحديث في قياسات أنسجتنا: أي الجينات نشطة، وما البروتينات الموجودة، وأي الجزيئات الصغيرة تزود خلايانا بالطاقة. ومع ذلك تُجرى معظم هذه القياسات على عينات مخلوطة، حيث تتداخل أنواع عديدة من الخلايا معًا. الدراسة وراء DECODE تقدّم إطار عمل قويًا قائمًا على الذكاء الاصطناعي يمكنه فصل هذه الإشارات، ويخبرنا أي الخلايا والحالات الخلوية حاضرة، حتى عبر أنواع بيانات مختلفة جدًا. هذه القدرة قد تسرّع البحث في السرطان والمناعة والأمراض الأيضية مع تحقيق استفادة أفضل من عينات البنوك الحيوية الموجودة.
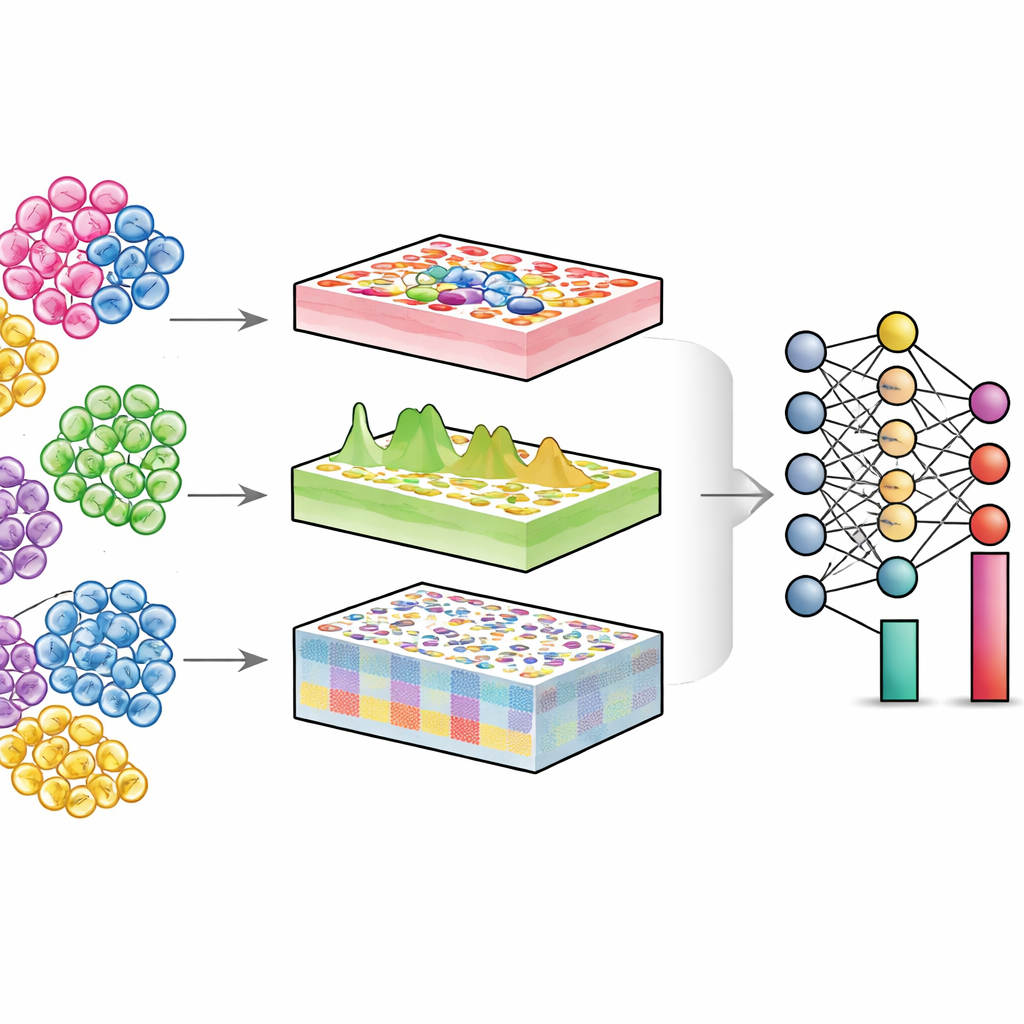
إلقاء نظرة داخل الأنسجة المختلطة
كل عضو يشكّل مجتمعًا من أنواع خلوية مختلفة — خلايا مناعية، خلايا بنيوية، خلايا جذعية والمزيد. في الصحة والمرض، ما يتغير غالبًا ليس فقط ما تفعله كل خلية، بل كم عدد كل نوع وما هي الحالة التي تكون فيها. تتيح تقنيات الخلايا الأحادية قياس الخلايا منفردة مباشرةً، لكنها مكلفة ومعقدة تقنيًا، خصوصًا في مجموعات مرضى كبيرة أو عينات مخزّنة قديمة. بالمقابل، تختلط التجارب التقليدية "الكتلية" آلاف أو ملايين الخلايا وتقرأ إشارة متوسّطة. تحاول خوارزميات فكّ الاختلاط عكس هذا المزج: بالنظر إلى بيانات الكتل ومرجع من الخلايا الأحادية، تُقدّر نسبة كل نوع خلية في النسيج.
حدود الأدوات المتخصّصة
أدوات فكّ الاختلاط الحالية مُصمَّمة في الأغلب لنوع قياس واحد، مثل نشاط الجينات (النسخومية) أو البروتينات (البروتيوميات). غالبًا ما تفترض سلوكيات إحصائية محددة لا تنطبق على أنواع بيانات أخرى، وتواجه صعوبة عندما تحتوي العينة الكتلية على أنواع خلايا مفقودة من بيانات المرجع. التأثيرات الدفعاتية القوية — اختلافات في المتبرعين أو الأجهزة أو حالات الصحة — يمكن أن تغبّش الإشارات البيولوجية كذلك. ومن الجدير بالذكر أنه لم تكن هناك طريقة عملية للأيضيات، دراسة الجزيئات الصغيرة الأقرب غالبًا إلى الأعراض السريرية. كنتيجة لذلك، اضطر العلماء الذين يحلّلون مجموعات بيانات متعددة الأومكس إلى استخدام عدة أدوات متخصصة، لكل منها خصائصه، مما صعّب مقارنة النتائج عبر الدراسات وأنواع البيانات.
محرك فكّ اختلاط شامل
يتعامل DECODE مع هذه التحديات باعتبار فكّ الاختلاط مشكلة تعلم عميق مرنة يمكنها معالجة الجينات والبروتينات والأيضيات بطريقة موحّدة. أولًا، يصنّع "أنسجة مزيفة" عن طريق خلط ملفات تعريف الخلايا الأحادية رقميًا بنسب عشوائية، مكوّنًا مجموعة تدريب غنية حيث تكون التركيبة الحقيقية معروفة. مرحلة التعلم التنافسي تعلّم بعد ذلك مُشفرًا ليطبّق كلًا من الأنسجة الحقيقية والأنسجة المزيفة إلى تمثيل مشترك تُقلَّل فيه الاختلافات التقنية بينما تُحافظ الأنماط البيولوجية ذات المعنى. بعدها، يتعلم وحدة خاصة لإزالة الضوضاء، موجهة بتعلّم تبايني، فصل الإشارات النسيجية الحقيقية عن الضوضاء الاصطناعية. تجعل هذه الخطوة DECODE قويًا أمام أنواع الخلايا المفقودة في بيانات المرجع وأمام أخطاء القياس. أخيرًا، تُمرَّر الميزات المنقّاة إلى وحدة فكّ الاختلاط التي تُقدّر إما الوفورات المطلقة أو النسبية لأنواع وحالات الخلايا، اعتمادًا على مدى اكتمال المرجع.
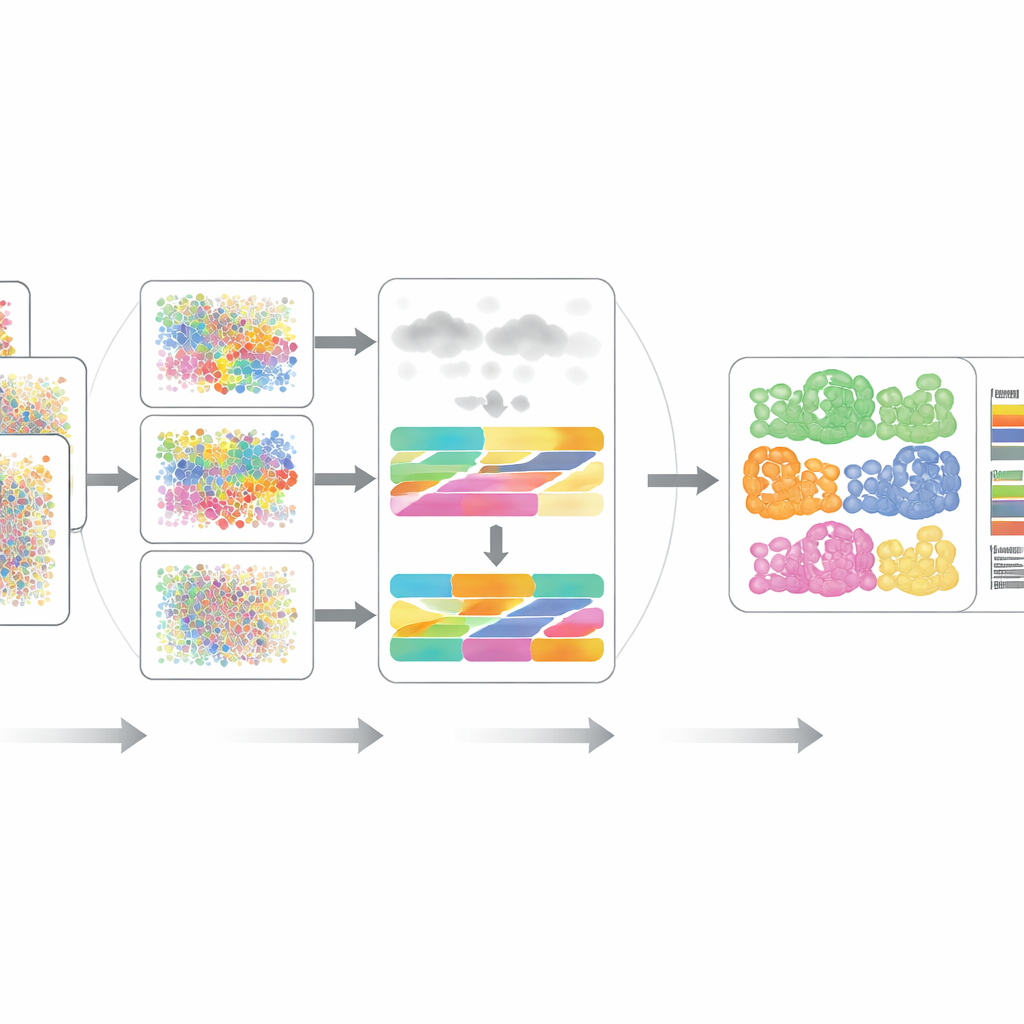
اختبار DECODE
قيّم المؤلفون DECODE بدقّة عبر 15 مجموعة بيانات تغطي سبع سيناريوهات واقعية، بما في ذلك متبرعون مختلفون، حالات مرضية، ظروف صحية، منصات تجريبية وحتى قياسات ذات دقة مكانية. عبر النسخومية والبروتيوميات، طابق DECODE عمومًا أو تفوّق على أدوات متقدمة من حيث الدقة مع الحفاظ على زمن حساب وذاكرة معقولين. والأهم من ذلك، كان DECODE الطريقة الوحيدة التي قدمت نتائج موثوقة على بيانات الأيضيات، حيث الخصائص تكون أقل وعدد أنواع الخلايا قد تبدو متشابهة مضللة. كما برهن الإطار على قدرة جيدة في تتبّع حالات الخلايا — مثل التقدّم على مسار تطوري، مراحل دورة الخلية، أو الاستجابات للعلاج الدوائي — وليس مجرد الأنواع الخلوية الثابتة.
متين في بيانات العالم الحقيقي المزعجة والناقصة
غالبًا ما تحتوي الأنسجة الحقيقية على أنواع خلايا لا تُلتقط في مراجع الخلايا الأحادية المعملية، ويمكن أن تشوّه الضوضاء التجريبية العديد من الميزات دفعة واحدة. لمحاكاة هذه المشكلات، أضاف الباحثون أنواع خلايا مجهولة وقدموا عدة أشكال من الضوضاء والبيانات الناقصة عبر النسخومية والبروتيوميات والأيضيات. في معظم الحالات، بقي DECODE الطريقة الأكثر دقة وفي الأيضيات كان الوحيد الذي لم يتعطل. كما أظهروا أن DECODE يعطي إجابات متسقة للغاية عند تطبيقه على قياسات الجين والبروتين المتطابقة من عينات خلايا الدم نفسها، وهو متطلب أساسي لمقارنة تغيّرات أنواع الخلايا عبر طبقات الأومكس في مجموعات كبيرة.
رؤى بيولوجية جديدة من مجموعات متعددة الأومكس
مزوّدين بهذه الأداة الموحدة، أعاد الفريق فحص مجموعات بيانات أمراض معقّدة. في سرطان الثدي، دمجوا مجموعات بيانات نسخومية وبروتيومية ليُظهروا كيف تتحوّل الخلايا المناعية والخلايا الداعمة المصلية بين الأورام غير الناقلة للانتشار، والأورام الأولية الناقلة للانتشار، ونقائل الدماغ. أنماط مثل زيادة وفرة الخلايا التائية والخلايا الشبيهة بالأوعية المحيطية في الآفات غير الناقلة للانتشار، وزيادة الخلايا البائية في المراحل المتقدمة، تتوافق مع دراسات بيولوجية سابقة وتمدّها. في كبد الفأر، دمج DECODE مجموعات نسخومية وبروتيومية وأيضية لتتبّع كيف تتغيّر الخلايا الكبدية، والخلايا البطانية، والخلايا المناعية المقيمة تحت أنظمة غذائية ونماذج مرضية كبدية مختلفة، معيدًا إنتاج اتجاهات معروفة مثل ارتفاع نسب خلايا كوبفر في حالات الالتهاب.
ما يعنيه ذلك للمستقبل
بالنسبة للقارئ العادي، الرسالة الأساسية أن DECODE يعمل كموشور ذكي لبيانات الطب الحيوي: بالنظر إلى قياسات مخلوطة من أنسجة، يمكنه فصل مساهمات أنواع وحالات خلوية متعددة، ويقوم بذلك بشكل موثوق عبر عدة أنواع من القراءات الجزيئية. هذا يمكّن العلماء من استخلاص معلومات أكثر بكثير من مجموعات متعددة الأومكس والبنوك الحيوية الموجودة دون جمع بيانات أحادية الخلية جديدة لكل مشروع. ومع أن الطريقة لا تزال تعتمد على جودة واتساع مراجع الخلايا الأحادية المتاحة، ولا تزال مصادر الأيضيات محدودة، فإن DECODE يشكّل خطوة مهمة نحو التفسير الروتيني على مستوى الخلية للدراسات البشرية واسعة النطاق، مع فوائد محتملة لفهم آليات المرض وتوجيه الطب الدقيق.
الاستشهاد: Zhao, T., Liu, R., Sun, Y. et al. DECODE: deep learning-based common deconvolution framework for various omics data. Nat Methods 23, 596–608 (2026). https://doi.org/10.1038/s41592-026-03007-y
الكلمات المفتاحية: فكّ اختلاط متعدد الأومكس, مرجع خَليوي أحادي الخلية, التعلم العميق في علم الأحياء, تحليل الأيضيات, تكوّن أنواع الخلايا