Clear Sky Science · ar
مؤشرات متعددة الألوان من الجيل التالي لتصوير النورإبينفرين داخل الأحياء
رؤية رسول دماغي خفي
النورإبينفرين هو مادة كيميائية في الدماغ تشكل بهدوء طرق استيقاظنا، وقدرتنا على الانتباه، تكوين الذكريات والاستجابة للضغط. حتى وقت قريب، كان بإمكان العلماء فقط إلقاء نظرة محدودة على نشاطه باستخدام أدوات بطيئة أو غير دقيقة. تعرض هذه الورقة زوجًا جديدًا من العلامات المتوهجة التي تتيح للباحثين مشاهدة ارتفاع وانخفاض النورإبينفرين في الدماغ الحي، في الوقت الحقيقي وبتفصيل دقيق. قد تعمق هذه التطورات فهمنا للنوم والقلق والتعلم والأمراض التنكسية العصبية.
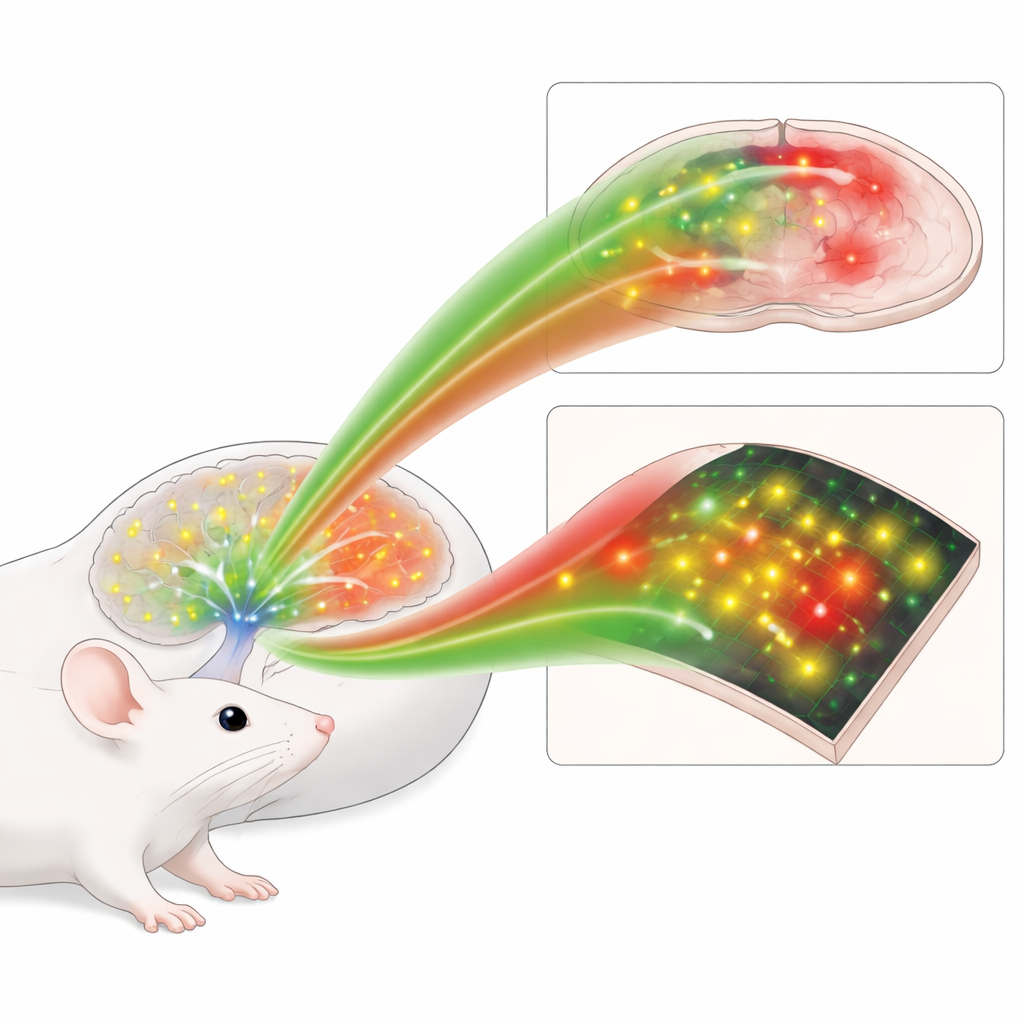
لماذا كان تتبع هذه الإشارة صعبًا جدًا
يُفرَز النورإبينفرين بواسطة مجموعة صغيرة من خلايا جذع الدماغ ترسل أليافًا عبر الدماغ، وتغيّر كيفية عمل الدوائر بدلاً من مجرد تشغيلها أو إيقافها. طرق القياس الكلاسيكية، مثل المجسات الكيميائية الصغيرة أو الخلايا المزروعة التي تستجيب للنورإبينفرين، إما تُطمس الأحداث على مدى ثوانٍ عديدة أو لا تميّزه بوضوح عن جزيئات قريبة. استراتيجية أحدث تستخدم مستقبلات سطحية خلوية معدلة تضيء عند ارتباطها بالنورإبينفرين، مما يسمح بقراءة ضوئية. لكن الإصدارات الأولى كانت باهتة نسبيًا، خصوصًا في الجزء الأحمر من الطيف، ولم تكن مرنة بما يكفي للتجارب التي تتطلب الجمع بين عدة ألوان في آن واحد.
بناء مراقبين أخضر وأحمر أكثر إشراقًا
قام المؤلفون بصياغة مؤشرات محسّنة باللونين الأخضر والأحمر، أطلقوا عليهما nLightG2 وnLightR2، عن طريق دمج أجزاء من مجسّات الدوبامين والنورإبينفرين السابقة واختبار العشرات من الطفرات بشكل منهجي. أدت هذه التعديلات إلى جعل المستشعرات أكثر إشراقًا عند وجود النورإبينفرين، دون تغيير كبير في توهجها الأساسي. في زراعات الخلايا، أظهرت الأدوات الجديدة استجابات أكبر بعدة أضعاف للنورإبينفرين مقارنةً بالإصدارات السابقة، واستجابت في غضون عشرات الملّي ثانية وتراجعت خلال أقل من ثانية. كما تكاد لا تستجيب لمواد كيميائية دماغية أخرى، مثل الدوبامين، ولم تُفعّل مسارات الإشارة الداخلية للخلايا، وهو فحص أمان مهم لضمان أنها مراقبون لا مشاركون.
إثبات قوتها في نسيج الدماغ
بعد ذلك، أدخل الفريق المستشعرات في شرائح من دماغ الفأر واستخدم مجهر الفوتون المزدوج، القادر على الرؤية عميقًا داخل النسيج، لمقارنة التصاميم القديمة والجديدة. عندما بُخّ النورإبينفرين على النسيج، أو عندما حُفّزت الألياف المحلية كهربائيًا لإطلاقه طبيعياً، أنتجت nLightG2 وnLightR2 ومضات أكبر بكثير وأسهل في الاكتشاف مقارنة بالمستشعرات السابقة. أدت الأداتان الخضراء والحمراء أداءً سريعًا بشكل مماثل، ما يعني أن اختيار اللون لم يعد يتطلب التضحية بالسرعة. سمحت هذه الحساسية الأعلى للباحثين برسم خريطة لكيفية انتشار النورإبينفرين في الفضاء، بدلًا من معرفة أنه أُطلِق في مكان ما ضمن مجال الرؤية فحسب.
مراقبة حالات الدماغ، الخوف والملاحة في الفعل
تكمن الوعدة الحقيقية لهذه الأدوات في الحيوانات الحية. باستخدام ألياف بصرية رفيعة جدًا، جمع المؤلفون مؤشر النورإبينفرين الأحمر مع مستشعر كالسيوم أخضر يخبر عن إطلاق النبضات العصبية. في مركز النوم في الدماغ، رصدوا أن دفعات النشاط في خلايا منتجة للنورإبينفرين أثناء النوم العميق تلتها عن كثب زيادات في مستويات النورإبينفرين المحلية، حدثًا بعد حدث. في اللوزة الدماغية، وهي منطقة مهمة للعاطفة، كشف المستشعر الأخضر للنورإبينفرين أن نغمة غير مؤذية باتت تحفز ارتفاعًا مستمرًا في النورإبينفرين بعد أن اقترنت بصدمة خفيفة، مما يعكس تقوية ذكريات الخوف. في الحصين، الذي يساعد في رسم خرائط المكان، صُوّر المستشعر الأحمر مع مستشعر كالسيوم أخضر للخلايا النجمية بينما ركضت الفئران عبر ممر افتراضي للحصول على مكافآت مائية. هنا، ارتبط نشاط الخلايا النجمية بالقرب من موقع المكافأة ارتباطًا وثيقًا بتدفقات محلية من النورإبينفرين، مما يوحي بحوار بين هذا المركب والخلايا الداعمة أثناء التجارب المجزية.
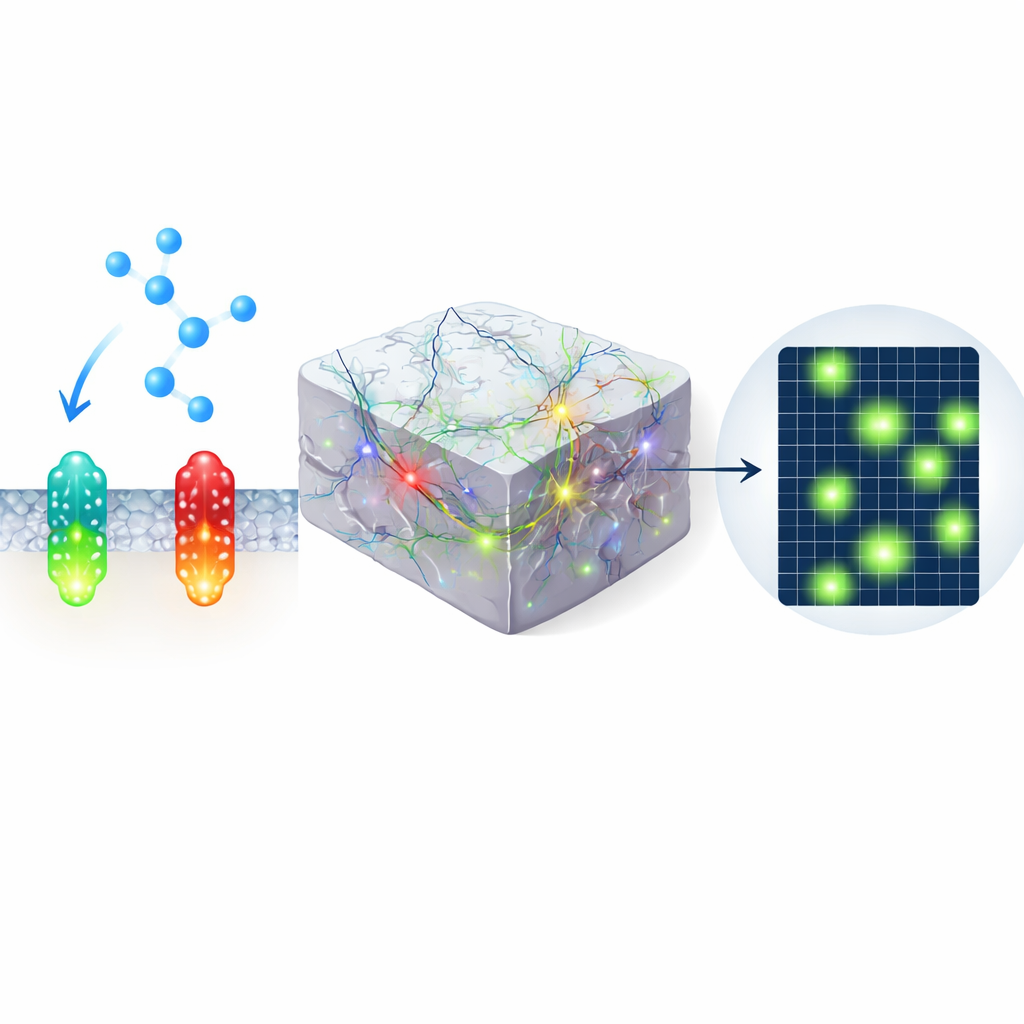
كشف جيوب نشاط دقيقة في القشرة البصرية
في مجموعة أخرى من التجارب، عبّر المؤلفون عن المستشعر الأخضر في القشرة البصرية لفئران مستيقظة وصوروه باستخدام مجهر الفوتون المزدوج بينما شاهدت الحيوانات مؤثرات مُقْبِلة وتبدّلَت بين الراحة والجري. بدلًا من غمرة إشارة ناعمة، وجدوا بقعًا قصيرة ومحددة للغاية من زيادة التألق—نطاقات دقيقة—منتشرة عبر مجال الرؤية. استجابت بعض النطاقات الدقيقة بشكل مفضّل للتهديد البصري، وبعضها للحركة، وأخرى أضاءت عفويًا. كانت هذه الأنماط غير مرئية إلى حد كبير عند استخدام مستشعر أخضر أقدم أو ضابط غير رابط مطفَّر، مما يؤكد الحساسية المحسنة لـ nLightG2 ويقترح أن النورإبينفرين يشكّل نشاط الدماغ بشكل أكثر دقة مما كان يُقدَّر سابقًا.
ماذا يعني هذا لبحوث الدماغ
معًا، تُظهر هذه النتائج أن nLightG2 وnLightR2 تشكّلان مجموعة أدوات قوية لمراقبة النورإبينفرين في الدماغ الحي، عبر مقاييس تتراوح من نطاقات دقيقة مفردة إلى حالات سلوكية كاملة. وبما أنهما يأتيان بألوان مميزة ويمكن دمجهما مع مرافقات فلورية أخرى، يمكن للعلماء الآن تتبّع النورإبينفرين بالتوازي مع الإشارات الكهربائية أو إشارات الكالسيوم في أنواع خلوية محددة، أثناء النوم أو التعلم أو الضغط. قد توضح هذه القدرة على رؤية متى وأين يعمل هذا المُعدّل العصبي الرئيسي كيف يدعم الانتباه والذاكرة الصحية، وكيف يساهم اختلاله في حالات مثل القلق والاكتئاب والأمراض التنكسية العصبية.
الاستشهاد: Rohner, V.L., Curreli, S., Lamothe-Molina, P.J. et al. Next-generation multicolor indicators for in vivo imaging of norepinephrine. Nat Methods 23, 636–652 (2026). https://doi.org/10.1038/s41592-026-03006-z
الكلمات المفتاحية: النورإبينفرين, التحكم العصبي, مستشعرات مشفرة وراثيًا, تصوير فوتون مزدوج, النوم والتعلم